1.Tính toán và hoàn thành nội dung bảng sau”
| n(mol) | m(g) | V(l) | Số phân tử | |
| H2 | 0,25 | |||
| O2 | 3,2 | |||
| N2 | 4,48 | |||
| CO2 | 3.1023 |
T là một pentapeptit mạch hở. Đốt cháy hoàn toàn một lượng T bằng O 2 , thu được C O 2 , H 2 O v à N 2 ; trong đó số mol O 2 phản ứng bằng số mol C O 2 tạo thành. Thủy phân hoàn toàn 0,04 mol T bằng dung dịch HCl dư, cô cạn dung dịch sau phản ứng chỉ thu được m gam muối của một amino axit (no, mạch hở, phân tử chứa một nhóm amino và một nhóm cacboxyl). Giá trị của m là
A. 20,76.
B. 23,66.
C. 25,10.
D. 22,22.
Chọn đáp án C
Cách 1:: Biến đổi peptit – quy về đipeptit giải đốt cháy kết hợp thủy phân
☆ đốt đipeptit C 2 n H 4 n N 2 O 3 + 15 m o l O 2 → t 0 12 m o l C O 2 + 12 m o l H 2 O + ? N 2 .
(giả thiết cho tỉ lệ 5 : 4 nên cho O2 là 15 mol thì tương ứng n C O 2 = n H 2 O = 12 mol).
bảo toàn O có n đ i p e p t i t = (12 × 3 – 15 × 2) ÷ 3 = 2 mol ⇒ n = 12 ÷ 4 = 3
⇒ cho biết α–amino axit là Alanin: C 3 H 7 N O 2
⇒ thủy phân 0,04 mol Q 5 + HCl (vừa đủ) + H 2 O → 0,2 mol C 3 H 7 N O 2 . H C l
⇒ m = 0,2 × (89 + 36,5) = 25,1 gam. Chọn đáp án C. ♣.
Cách 2: Giải theo công thức tổng quát của peptit:
Amino axit dạng: C n H 2 n + 1 N O 2 n ≥ 2 ⇒ công thức của tetrapeptit Q là C 4 n H 8 n – 2 N 4 O 5 .
Phương trình cháy: C 4 n H 8 n – 2 N 4 O 5 + 6 n – 3 O 2 → 4n C O 2 + 4 n – 1 H 2 O + 2 N 2 .
⇒ 6n – 3 = 5 4 × 4n ⇒ n = 3 ⇒ amino axit là Ala ⇒ m = 0,04 × 5 × 125,5 = 25,1 gam.
Q là một tetrapeptit mạch hở. Đốt cháy hoàn toàn một lượng Q bằng O 2 , thu được C O 2 , H 2 O v à N 2 ; trong đó số mol O 2 phản ứng bằng số mol C O 2 tạo thành. Thủy phân hoàn toàn 0,03 mol Q bằng dung dịch KOH vừa đủ, chỉ thu được m gam muối của một amino axit (no, mạch hở, phân tử chứa một nhóm amino và một nhóm cacboxyl). Giá trị của m là
A. 15,78.
B. 13,32.
C. 13,86.
D. 15,24.
Chọn đáp án D
Cách 1:: Biến đổi peptit – quy về đipeptit giải đốt cháy kết hợp thủy phân
☆ đốt đipeptit C2nH4nN2O3 + 15 mol O2 → t 0 12 mol CO2 + 12 mol H2O + ? N2.
(giả thiết cho tỉ lệ 5 : 4 nên cho O 2 là 15 mol thì tương ứng n C O 2 = n H 2 O = 12 mol).
bảo toàn O có n đ i p e p t i t = (12 × 3 – 15 × 2) ÷ 3 = 2 mol ⇒ n = 12 ÷ 4 = 3
⇒ cho biết α–amino axit là Alanin: C 3 H 7 N O 2
⇒ thủy phân 0,03 mol Q 4 + KOH (vừa đủ) → 0,12 mol C 3 H 6 N O 2 N a . . .
⇒ m = 0,12 × (89 + 38) = 15,24 gam. Chọn đáp án D. ♠.
Cách 2: Giải theo công thức tổng quát của peptit:
Amino axit dạng: C n H 2 n + 1 N O 2 n ≥ 2 ⇒ công thức của tetrapeptit Q là C 4 n H 8 n – 2 N 4 O 5 .
Phương trình cháy: C 4 n H 8 n – 2 N 4 O 5 + 6 n – 3 O 2 → 4n C O 2 + 4 n – 1 H 2 O + 2 N 2 .
⇒ 6n – 3 = 5 4 × 4n ⇒ n = 3 ⇒ amino axit là Ala ⇒ m = 0,03 × 4 × 127 = 15,24 gam
Tính số mol ứng với: 32g CuO; 4,958 lít khí O2(đktc); 1,5.1023 phân tử H2O, 50g CaCo3 a) Tìm thể tích khí (ở đkc) ứng với: 0,5 mol khí CO2; 3.1023 phân tử N2 b) Tìm khối lượng của 4,958 lít khí O2 (ở đkc), của 0,5 mol Al2(SO4)3 c) Tính số nguyên tử, phân tử của: 0,5 mol Cu; 2g MgO; 12,395 lít khí SO2 (đkc) d) Tính thành phần % về khối lượng của các nguyên tố trong Fe2O3, CaCO3
tính
m của 2,24 l so2
v của 4,4 g co2 và 3,2 g o2
mol của 1,5.1023phân tử n2
làm hộ nha nhanh lên mai mình kiểm tra học kì rồi
- n SO2=2,24/22,4=0,1(mol)
m SO2=0,1.64=6,4(g)
-n CO2=4,4/44=0,1(mol)
n O2=3,2/32=0,1(mol)
n hh=0,1+0,1=0,2(mol)
V hh=0,2.22,4=4,48(l)
-n N2=\(\frac{1,5.10^{23}}{6.10^{23}}=0,25\left(mol\right)\)
Mai mk cx thi học kì nè!
Bài 1: Khí oxi chiếm bao nhiêu phần trăm theo thể tích và theo khối lượng trong mỗi hỗn hợp sau:
a. 0,75 mol O2 ; 1,25 mol N2 ; 0,3 mol CO2.
b. 3.1023 phân tử CO2 ; 6.1023 phân tử O2 ; 9.1023 phân tử N2.
c. 2 lít CO2 ; 4 lít O2 ; 6 lít N2.
Bài 2: Hãy giải thích vì sao ban đêm ngủ trong phòng có nhiều cây xanh lại cảm thấy mệt mỏi? Em hãy đưa ra biện pháp thích hợp để đảm bảo sức khỏe cho con người?
Bài 2 :
- Vì vào ban đêm, hoa hoặc cây xanh ngừng quang hợp nhưng vẫn diễn ra quá trình hô hấp, cây xanh sẽ hấp thụ khí oxi trong không khí để phân giải chất hữu cơ, sản sinh ra năng lượng cần cho các hoạt động sống của cây. Cùng với đó, cây thải ra hơi nước và khí Cacbonic. Ban đêm, con người và cây xanh sẽ đồng thời hấp thu khí oxi và thải khí cacbonic.
- Một số biện pháp đảm bảo sức khỏe :
+, Chỉ mang vào phòng ngũ những cây nhỏ vừa không nên mang cây quá to .
+, Chỉ nên mang cây vào trong phòng vào ban ngày ban đêm nên bỏ ra ngoài .
+, Để căn phòng thoáng khí, nhiều ánh sáng khi cho cây vào phòng ngủ .
+, .....
Sử dụng công thức:
\(\%V_{O2}=\frac{V_{O2}}{V_{hh}}.100\%=\frac{n_{O2}}{n_{hh}}.100\%;m=n.M;n=\frac{N}{6.10^{23}};n=\frac{V}{22,4}\)
a, Khi đó:
\(V_{O2}=\frac{0,75}{0,75+1,25+0,3}.100\%=32,6\%\)
\(m_{O2}=0,75.32=24\left(g\right)\)
\(m_{N2}=1,25.28=35\left(g\right)\)
\(m_{CO2}=0,3.44=13,2\left(g\right)\)
b, c, Chuyển chất khí thành số mol rồi làm tương tự như ý a nhé!
b, \(n_{CO2}=\frac{3.10^{23}}{6.10^{23}}=0,5\left(mol\right)\)
\(n_{O2}=\frac{6.10^{23}}{6.10^{23}}=1\left(mol\right)\)
\(n_{N2}=\frac{9.20^{23}}{6.10^{23}}=1,5\left(mol\right)\)
c, \(n_{CO2}=\frac{2}{22,4}\left(mol\right);n_{O2}=\frac{4}{22,4}\left(mol\right);n_{N2}=\frac{6}{22,4}\left(mol\right)\)
Câu 2: Hãy tính:
a/ Thể tích ở 200C và 1atm của: 0,2 mol CO; 8 g SO3 ; 3.1023 phân tử N2
b/ Khối lượng của: 0,25mol Fe2O3; 0,15mol Al2O3 ; 3,36 lit khí O2 (đktc) c/ Số mol và thể tích của hỗn hợp khí(đktc) gồm có: 8g SO2 ; 4,4g CO2 và 0,1g H2
a)
- \(V_{CO}=n.24=0,2.24=4,8\left(l\right)\)
- \(n_{SO_3}=\dfrac{m}{M}=\dfrac{8}{80}=0,1\left(mol\right)\)
`=>` \(V_{SO_3}=n.24=0,1.24=2,4\left(l\right)\)
- \(n_{N_2}=\dfrac{\text{Số phân tử}}{6.10^{23}}=\dfrac{3.10^{23}}{6.10^{23}}=0,5\left(mol\right)\)
`=>` \(V_{N_2}=n.24=0,5.24=12\left(l\right)\)
b)
- \(m_{Fe_2O_3}=n.M=0,25.160=40\left(g\right)\)
- \(m_{Al_2O_3}=n.M=0,15.102=15,3\left(g\right)\)
- \(n_{O_2}=\dfrac{V_{\left(\text{đ}ktc\right)}}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
`=>` \(m_{O_2}=n.M=0,15.32=4,8\left(g\right)\)
c)
Ta có: \(\left\{{}\begin{matrix}n_{SO_2}=\dfrac{m}{M}=\dfrac{8}{64}=0,125\left(mol\right)\\n_{CO_2}=\dfrac{m}{M}=\dfrac{4,4}{44}=0,1\left(mol\right)\\n_{H_2}=\dfrac{m}{M}=\dfrac{0,1}{2}=0,05\left(mol\right)\end{matrix}\right.\)
`=>` \(n_{hh}=n_{SO_2}+n_{CO_2}+n_{H_2}=0,125+0,1+0,05=0,275\left(mol\right)\)
`=>` \(V_{hh\left(\text{đ}ktc\right)}=n_{hh}.22,4=0,275.22,4=6,16\left(l\right)\)

Trao đổi khí là quá trình sinh vật lấy O2 hoặc CO2 từ môi trường vào cơ thể, đồng thời thải ra môi trường khí CO2 hoặc O2. Phân tích hình ảnh trên sau đó hoàn thành nội dung bảng theo mẫu.
Cho hỗn hợp E gồm peptit X mạch hở (tạo thành từ Gly, Ala) và este Y (tạo thành từ axit cacboxylic no, đơn chức, mạch hở và metanol). Đốt cháy hoàn toàn m gam E cần 15,68 lít O2 (đktc). Mặt khác, thủy phân hoàn toàn m gam E trong dung dịch NaOH vừa đủ thu được 24,2 gam hỗn hợp muối (trong đó số mol muối natri của Gly lớn hớn số mol muối natri của Ala). Đốt cháy hoàn toàn 24,2 gam muối trên cần 20 gam O2 thu được H2O, Na2CO3, N2 và 18,7 gam CO2. Tỉ lệ số mol Gly : Ala trong X là
A. 3 : 1
B. 2 : 1
C. 3 : 2
D. 4 : 3
Đáp án A
→ n O 2 ( C H 3 O H ) = 15 , 68 22 , 4 - 20 32 = 0 , 075
→ n C H 3 O H = 0 , 05 → n Y = 0 , 05
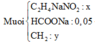
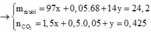
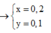
n G l y > n A l a → n A l a ∈ ( 0 ; 0 , 1 )
→ C H 3 C O O N a
→ n A l a = 0 , 05 → n G l y = 0 , 15
→ n G l y : n A l a = 3 : 1
Cho hỗn hợp E gồm peptit X mạch hở (tạo thành từ Gly, Ala) và este Y (tạo thành từ axit cacboxylic no, đơn chức, mạch hở và metanol). Đốt cháy hoàn toàn m gam E cần 15,68 lít O2 (đktc). Mặt khác, thủy phân hoàn toàn m gam E trong dung dịch NaOH vừa đủ thu được 24,2 gam hỗn hợp muối (trong đó số mol muối natri của Gly lớn hớn số mol muối natri của Ala). Đốt cháy hoàn toàn 24,2 gam muối trên cần 20 gam O2 thu được H2O, Na2CO3, N2 và 18,7 gam CO2. Tỉ lệ số mol Gly : Ala trong X là
A. 3 : 1.
B. 2 : 1.
C. 3 : 2.
D. 4 : 3