Đốt cháy hoàn toàn 10,8 gam kim loại A (hóa trị III) trong không khí thu được 20,4 gam sản phẩm. Biết A phản ứng với oxi trong không khí.
a/ Tìm kim loại A.
b/ Tính thể tích không khí đã phản ứng (biết O2 chiếm 20% thể tích không khí).
Đốt cháy 4,8 gam kim loại B (chưa biết) có hóa trị II trong không khí dư thu được 8 gam oxit (là hợp chất của B và O).
a) Viết PTHH.
b) Tính khối lượng oxi đã phản ứng.
c) Tính thể tích không khí (đktc) cần cho phản ứng trên.
d) Xác định kim loại B.
e) Tìm B nếu đề bài không cho dữ kiện hóa trị của B
\(a.PTHH:2B+O_2\overset{t^o}{--->}2BO\left(1\right)\)
b. Áp dụng ĐLBTKL, ta có:
\(m_B+m_{O_2}=m_{BO}\)
\(\Leftrightarrow m_{O_2}=8-4,8=3,2\left(g\right)\)
c. Ta có: \(n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,1.22,4=2,24\left(lít\right)\)
Mà: \(V_{O_2}=\dfrac{1}{5}.V_{kk}\)
\(\Leftrightarrow V_{kk}=2,24.5=11,2\left(lít\right)\)
d. Theo PT(1): \(n_B=2.n_{O_2}=2.0,1=0,2\left(mol\right)\)
\(\Rightarrow M_B=\dfrac{4,8}{0,2}=24\left(\dfrac{g}{mol}\right)\)
Vậy B là magie (Mg)
\(e.PTHH:2xB+yO_2\overset{t^o}{--->}2B_xO_y\left(2\right)\)
Theo PT(2): \(n_B=\dfrac{2x}{y}.n_{O_2}=\dfrac{2x}{y}.0,1=\dfrac{0,2x}{y}\left(mol\right)\)
\(\Rightarrow M_B=\dfrac{4,8}{\dfrac{0,2x}{y}}=\dfrac{4,8y}{0,2x}=12.\dfrac{2y}{x}\left(mol\right)\)
Biện luận:
| 2y/x | 1 | 2 | 3 |
| MB | 12 | 24 | 36 |
| loại | Mg | loại |
Vậy B là kim loại magie (Mg)
Vì thể tích khí oxi chiếm 1/5 thể tích không khí nhé
: Đốt cháy 10,8 gam một kim loại M hóa trị III trong không khí thu được 20,4 gam oxit.
1. Xác định tên kim loại M.
2. Tính thể tích không khí cần dùng để đốt cháy hết lượng kim loại trên (đktc).
3. Tính thể tích dung dịch HCl 2M cần dùng để hòa tan hết lượng oxit tạo thành.
4. Tính thể tích dung dịch NaOH 25% (D=1,25 g/ml) cần dùng để hòa tan hết lượng oxit tạo thành.
a, PT: \(4M+3O_2\underrightarrow{t^o}2M_2O_3\)
Ta có: \(n_M=\dfrac{10,8}{M_M}\left(mol\right)\)
\(n_{M_2O_3}=\dfrac{20,4}{2M_M+16.3}\left(mol\right)\)
Theo PT: \(n_M=2n_{M_2O_3}\Rightarrow\dfrac{10,8}{M_M}=2.\dfrac{20,4}{2M_M+16.3}\)
\(\Rightarrow M_M=27\left(g/mol\right)\)
→ M là Nhôm (Al)
b, Ta có: \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{3}{4}n_{Al}=0,3\left(mol\right)\) \(\Rightarrow V_{O_2}=0,3.22,4=6,72\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=33,6\left(l\right)\)
c, PT: \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,2\left(mol\right)\)
\(n_{HCl}=6n_{Al_2O_3}=1,2\left(mol\right)\)
\(\Rightarrow V_{ddHCl}=\dfrac{1,2}{2}=0,6\left(l\right)\)
d, PT: \(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
Theo PT: \(n_{NaOH}=2n_{Al_2O_3}=0,4\left(mol\right)\)
\(\Rightarrow m_{NaOH}=0,4.40=16\left(g\right)\Rightarrow m_{ddNaOH}=\dfrac{16}{25\%}=64\left(g\right)\)
\(\Rightarrow V_{ddNaOH}=\dfrac{64}{1,25}=51,2\left(ml\right)\)
Đốt cháy hoàn toàn 6,2 gam photpho trong không khí. Lượng khí oxi đã phản ứng với photpho vừa đủ để tác dụng với 32 gam kim loại R. Hãy xác định R (biết R ko có hóa trị quá III). Help me!!!!
nP = 6,2/31 = 0,2 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
Mol: 0,2 ---> 0,25
4R + nO2 -> (t°) 2R2On
Mol: 1/n <--- 0,25
M(R) = 32(1/n) = 32n (g/mol)
Xét:
n = 1 => Loại
n = 2 => R = 64 => R là Cu
n = 3 => Loại
Vậy R là Cu
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị hai không đổi trong hợp chất) trong hỗn hợp khí C l 2 v à O 2 . Sau phản ứng thu được 23,0 gam chất rắn và thể tích hỗn hợp khí đã phản ứng là 5,6 lít (đktc). Kim loại M là
A. Mg
B. Ca
C. Be
D. Cu
Chọn A
Cách 1:
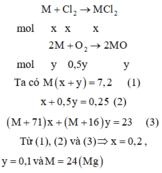
Cách 2:
Gọi số mol của Cl2 và O2 phản ứng lần lượt là x và y mol
→ nkhí = 0,25 mol → x + y = 0,25 (1)
Bảo toàn khối lượng có mkhí= 23 – 7,2= 15,8 gam
→ 71x + 32y = 15,8 (2)
Từ (1) và (2) → x = 0,2 và y = 0,05
Bảo toàn electron có:
2.nM = 2.nCl2 + 4.nO2 → nM= 0,3 → MM = 7,2 : 0,3 = 24 (g/mol)
Vậy kim loại M là Mg.
Đốt cháy hoàn toàn 3,6 gam kim loại M (có hóa trị II không đổi trong hợp chất) trong hỗn hợp khí Cl 2 và O 2 . Sau phản ứng thu được 11,5 gam chất rắn và thể tích hỗn hợp khí đã phản ứng là 2,8 lít (đktc). Kim loại M là
A. Be
B. Cu
C. Ca
D. Mg
Nếu đốt cháy hết 12 gam kim loại Mg trong không khí thu được 20 gam hợp chất magie oxit (MgO). Biết rằng magie cháy là xảy ra phản ứng với khí oxi trong không khí. a) Viết và cân bằng phương trình hóa học xảy ra. b) Tính thể tích không khí đã tham gia phản ứng (đktc) , biết thể tích O 2 bằng 1/5 thể tích không khí.
\(a,PTHH:2Mg+O_2\xrightarrow{t^o}2MgO\\ b,BTKL:m_{O_2}=m_{MgO}-m_{Mg}=20-12=8(g)\\ \Rightarrow V_{O_2}=\dfrac{8}{32}.22,4=5,6(l)\\ \Rightarrow V_{kk}=\dfrac{5,6}{\dfrac{1}{5}}=28(l)\)
1 mẩu kim loại Mg có lẫn tạp chất trơ( không tham gia phản ứng). đốt cháy 20 gam kim loại đó trong không khí sau khi phản ứng hoàn toàn thu được 32 g Magie oxit .Giả sử oxi chiếm 20% thể tích không khí còn lại là Nitơ
a Tính thể tích không khí đủ dùng để đốt cháy( điều kiện tiêu chuẩn)
b tính phần trăm theo khối lượng của Mg trong mẩu kim loại nói trên
a)a)nMgO=\(\dfrac{32}{40}\)=0,8(mol)
PT:2Mg+O2to→2MgO
⇒nO2=\(\dfrac{0,8}{2}\)=0,4(mol)
⇒VO2=0,4.22,4=8,96(l)
⇒Vkk=8,96:20%=44,8(l)
b)b)nMg=nMgO=0,8(mol)
⇒mMg=24.0,8=19,2(g)
%mMg=\(\dfrac{19,2}{20}\).100%=96%
a) Số mol magie oxit là 32/40=0,8 (mol).
2Mg (0,8 mol) + O2 (0,4 mol) \(\underrightarrow{t^o}\) 2MgO (0,8 mol).
Thể tích không khí đủ dùng để đốt cháy là:
V=0,4.22,4:20%=44,8 (lít).
b) Khối lượng kim loại Mg đã phản ứng là 0,8.24=19,2 (g).
Phần trăm theo khối lượng của Mg trong mẩu kim loại nói trên:
%mMg=19,2/20=96%.
PTHH: 2Mg + O2 → 2MgO nMg = \(\dfrac{7,2}{24}\) = 0,3 (mol)
theo PT: cứ 2 mol Mg tham gia phản ứng tác dụng 1 mol O2
vậy cứ 0,3 mol Mg tham gia phản ứng tạo ra n mol O2
=> nO2 = \(\dfrac{0,3.1}{2}\) = 0,15 (mol)
=> VO2 (đktc) = 0,15 . 22,4 = 3,36 (l)
theo PT: cứ 2 mol Mg tham gia phản ứng tác dụng 2 mol MgO
vậy cứ 0,3 mol Mg tham gia phản ứng tạo ra n mol MgO
=> nMgO = \(\dfrac{0,3.2}{2}\) = 0,3 (mol)
=> mMgO = 0,3 . 40 = 12 (g)
\(\begin{array}{l} PTHH:2Mg+O_2\xrightarrow{t^o} 2MgO\\ n_{Mg}=\dfrac{7,2}{24}=0,3\ (mol)\\ Theo\ pt:\ n_{O_2}=\dfrac{1}{2}n_{Mg}=0,15\ (mol)\\ \Rightarrow V_{O_2}=0,15\times 22,4=3,36\ (l)\\ Theo\ pt:\ n_{MgO}=n_{Mg}=0,3\ (mol)\\ \Rightarrow m_{MgO}=0,3\times 40=12\ (g)\end{array}\)
Trong phòng thí nghiệm, bạn Minh nung 63,2 gam KMnO4.
a/ Tính thể tích khí oxi thu được ở đktc biết hiệu suất phản ứng đạt 90%.
b/ Lượng oxi thu được ở câu a vừa đủ để đốt cháy 6,48 gam kim loại R hóa trị III. Tìm kim loại R.
\(n_{KMnO_4}=\dfrac{63,2}{158}=0,4\left(mol\right)\\
pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,4 0,2
=> \(V_{O_2\left(lt\right)}=0,2.22,4=4,48\left(l\right)\\
V_{O_2\left(tt\right)}=\dfrac{90.4,48}{100}=4,032\left(l\right)\)