Cho 1,2 lít hỗn hợp Axetilen và metan đi qua bình đựng 320 gam dung dịch nước Brom 15%
a viết phương trình
b Xác định phần trăm thể tích các khí trong hỗn hợp (các thể tích khí đo ở điều kiện tiêu chuẩn)
dẫn 5,6 hỗn hợp gồm metan và Axetilen qua bình đựng dung dịch brom dư thấy khối lượng bình brom tăng lên 3,9 gam còn Nếu đốt cháy hoàn toàn hỗn hợp cần phải đựng dùng thì 10,64 lít oxi ở điều kiện tiêu chuẩn
tính phần thể tích các khí trong hh02: Dẫn 5,6 lít hỗn hợp khí metan CH 4 và axetilen C 2 H 2 (ở đktc) đi qua dung dịch brom dư, thấy có 32 gam brom phản ứng. a. Viết phương trình phản ứng xảy ra. b. Tính thành phần phần trăm theo thể tích các khí có trong hỗn hợp. c. Tính thể tích khí oxi ở đktc cần dùng để đốt cháy hoàn toàn hỗn hợp trên. Cho biết: C = 12, H = 1, Br = 80
n Br2=\(\dfrac{32}{160}\)=0,2 mol
C2H2+2Br2->C2H2Br4
0,1------0,2 mol
=>%VC2H2=\(\dfrac{0,1.22,4}{5,6}\).100=40%
=>%VCH4=100-40=60%
=>n CH4=\(\dfrac{5,6-0,1.22,4}{22,4}\)=0,15 mol
CH4+2O2-to>CO2+2H2O
0,15----0,3
C2H2+\(\dfrac{5}{2}\)O2-to>2CO2+H2O
0,1-----0,25 mol
=>VO2=(0,3+0,25).22,4=12,32l
Cho 4,48 lít khí gồm metan và etilen đi qua dung dịch brom dư, thấy dung dịch nhạt màu và còn 1,12 lít khí thoát ra. Các thể tích khí đo ở điều kiện tiêu chuẩn. Thành phần phần trăm thể tích của khí metan trong hỗn hợp là:
A. 25% ; B. 50% ; C. 60% ; D. 37,5%
Hãy chọn đáp án đúng
- Đáp án A
- Khi cho hỗn hợp khí (gồm CH4 và C2H4 ) đi qua dung dịch brom thì C2H4 sẽ phản ứng hết với dung dịch brom, CH4 không tác dụng sẽ đi ra khỏi bình.
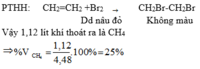
Một hỗn hợp A gồm etan (C2H6), etilen, axetilen, hiđro. Tỉ khối của hỗn hợp A so với CO2 là 0,4. Cho 11,2 lít hỗn hợp A đi qua dung dịch Br2 dư thấy khối lượng bình Br2 tăng thêm m gam. Hỗn hợp khí B thoát ra khỏi bình Br2 có thể tích 6,72 lít, trong đó khí có khối lượng phân tử nhỏ hơn chiếm 11,765% về khối lượng. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn.
a. Viết các phương trình hóa học xảy ra.
b. Tính phần trăm thể tích các khí trong B.
c. Tính m gam.
a. Phương trình phản ứng :
C2H2 + 2Br2 → C2H2Br4 (1)
C2H4 + Br2 → C2H4Br2 (2)
b. Hỗn hợp khí B gồm có H2, C2H6. Gọi x, y ( mol ) lần lượt là số mol của H2 và C2H6 có trong 6,72 lít hỗn hợp B.
nB = x + y = 6,72 : 22,4 = 0,3 mol (I)
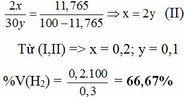
% V(C2H6) = 100% – 66,67% = 33,33%
c. nA = 11,2 : 22,4 = 0,5 mol , M A = 0,4 . 44 = 17,6 g/ mol
mA = 0,5 . 17,6 = 8,8 gam
mB = 0,2 . 2 + 0,1 . 30 = 3,4 gam
Vậy khối lượng bình Br2 tăng: m = mA – mB = 8,8 – 3,4 = 5,4 gam.
Dẫn 6,72 lít khí ở điều kiện tiêu chuẩn gồm metan và etilen đi qua bình dung dịch nước brom đã làm mất màu hoàn toàn dung dịch chứa 6gam brom . Tính thành phần , phần trăm về thể tích mỗi chất có trong hỗn hợp
Ta có: \(n_{Br_2}=\dfrac{6}{160}=0,0375\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,0375\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,0375.22,4}{6,72}.100\%=12,5\%\\\%V_{CH_4}=87,5\%\end{matrix}\right.\)
Cho 16,8 lít hỗn hợp gồm khí metan và axetilen đi qua dung dịch Brom 10%, sau phản ứng thu được 138,4 gam C2H2Br4
a. Viết phương trình
b. Tính khối lượng dung dịch Brom đã dùng
c. Tính thành phần phần trăm theo thể tích của mỗi khí trong hỗn hợp đầu
C2H2+2Br2-to>C2H2Br4
0,4-------0,8----------0,4 mol
n C2H2Br4=\(\dfrac{138,4}{346}=0,4mol\)
=>m Br2= 0,8.160=128g
=>m ddBr2=1280g
=>%mC2H2=\(\dfrac{0,4.22,4}{16,8}.100=53,3\%\)
=>%m CH4=100-53,3=46,7%
cho 2,24 lít hỗn hợp khí metan và axetilen (đo đktc) vào dung dịch brom dư thấy khối lượng nước brom tăng lên 0,78 gam. Tính phần trăm thể tích mỗi khí có trong hỗn hợp.
\(m_{tăng}=m_{C_2H_2}=0,78\left(g\right)\\PTHH:C_2H_2+2Br_2\rightarrow C_2H_2Br_4\\ n_{C_2H_2}=\dfrac{0,78}{26}=0,03\left(mol\right)\\ n_{hh.khí}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\\Rightarrow n_{CH_4}=0,1-0,03=0,07\left(mol\right)\\ n.tỉ.lệ.thuận.với.V\\ \%V_{CH_4}=\dfrac{0,07}{0,1}.100\%=70\%;\%V_{C_2H_2}=100\%-70\%=30\%\)
cho 4,48l khí hỗn hợp gồm metan và etilen đi qua bình đựng nước brom dư . cân lại bình đựng dung dịch brom thấy khối lượng tăng 1,4g . biết thể tích các khí đo ở đktc . tính thành phần % mà khi trong hỗn hợp
\(m_{bìnhtăng}=m_{anken}=m_{etilen}=1,4g\)
\(\Rightarrow n_{C_2H_4}=\dfrac{1,4}{28}=0,05mol\)
\(n_{hh}=\dfrac{4,48}{22,4}=0,2mol\)
\(\Rightarrow n_{metan}=n_{hh}-n_{eilen}=0,2-0,05=0,15mol\)
\(\%V_{metan}=\dfrac{0,15}{0,2}\cdot100\%=75\%\)
\(\%V_{etilen}=100\%-75\%=25\%\)
Dẫn 2,8 lít khí (ở đktc) hỗn hợp khí metan và etilen đi qua bình đựng dung dịch brom dư thấy có 4 gam brom đã phản ứng. Thành phần phần trăm về thể tích các khí trong hỗn hợp lần lượt là
A. 50% và 50%
B. 40% và 60%
C. 30% và 70%
D. 80% và 20%
\(n_{hh.khí}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ n_{Br_2}=\dfrac{4}{160}=0,025\left(mol\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí metan không tác dụng với dd Br2
\(n_{C_2H_4}=n_{Br_2}=0,025\left(mol\right)\)
Vì số mol tỉ lệ thuận với thể tích. Nên:
\(\%V_{C_2H_4}=\%n_{C_2H_4}=\dfrac{0,025}{0,125}.100=20\%\\ \Rightarrow\%V_{CH_4}=100\%-20\%=80\%\)
Vậy chọn D
Chúc em học tốt và có được POP!
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(n_{Br_2}=\dfrac{4}{160}=0,025mol\)
\(V_{Br_2}=0,025.22,4=0,56l\)
\(\%V_{C_2H_4}=\dfrac{0,56.100}{2,8}=20\%\)