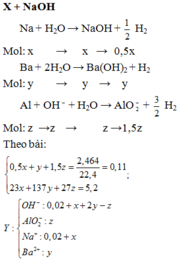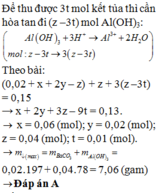cho 6,5 g hỗn hợp kẽm vào 200 ml dd hcl 2m thu được bao nhiêu lít khí ở đktc ? Gấp ạ

Những câu hỏi liên quan
Bài 1. Cho 2,9 gam hỗn hợp B gồm Ba và BaO vào nước thu được 224 ml khí H2 ở đktc. Tính % khối lượng các chất trong B và khối lượng Ba(OH)2 thu được.Bài 2: Cho 6,5 gam kẽm tác dụng với 200 gam dung dịch HCl 7,3%.a. Tính khối lượng chất dư.b. Tính thể tích khí hidro thoát ra ở điều kiện tiêu chuẩn.c. Tính nồng độ phần trăm các chất trong dung dịch thu được sau phản ứn
Đọc tiếp
Bài 1. Cho 2,9 gam hỗn hợp B gồm Ba và BaO vào nước thu được 224 ml khí H2 ở đktc. Tính % khối lượng các chất trong B và khối lượng Ba(OH)2 thu được.
Bài 2: Cho 6,5 gam kẽm tác dụng với 200 gam dung dịch HCl 7,3%.
a. Tính khối lượng chất dư.
b. Tính thể tích khí hidro thoát ra ở điều kiện tiêu chuẩn.
c. Tính nồng độ phần trăm các chất trong dung dịch thu được sau phản ứn
Bài 1 :
224ml = 0,224l
\(n_{H2}=\dfrac{0,224}{22,4}=0,01\left(mol\right)\)
Pt : \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2|\)
1 2 1 1
0,01 0,01 0,01
\(BaO+H_2O\rightarrow Ba\left(OH\right)_2|\)
1 1 1
0,01 0,01
\(n_{Ba}=\dfrac{0,01.1}{1}=0,01\left(mol\right)\)
\(m_{Ba}=0,01.137=1,37\left(g\right)\)
\(m_{BaO}=2,9-1,37=1,53\left(g\right)\)
0/0Ba = \(\dfrac{1,37.100}{2,9}=47,24\)0/0
0/0BaO = \(\dfrac{1,53.100}{2,9}=52,76\)0/0
Có : \(m_{BaO}=1,53\left(g\right)\)
\(n_{BaO}=\dfrac{1,53}{153}=0,01\left(mol\right)\)
\(n_{Ba\left(OH\right)2\left(tổng\right)}=0,01+0,01=0,02\left(mol\right)\)
⇒ \(m_{Ba\left(OH\right)2}=0,02.171=3,42\left(g\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
Bài 2:
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(m_{HCl}=200.7,3\%=14,6\left(g\right)\Rightarrow n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,1 0,2 0,1 0,1
Ta có: \(\dfrac{0,1}{1}< \dfrac{0,4}{2}\) ⇒ Zn pứ hết, HCl dư
\(m_{HCldư}=\left(0,4-0,2\right).36,5=7,3\left(g\right)\)
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c, \(m_{dd.sau.pứ}=6,5+200-0,1.2=206,3\left(g\right)\)
\(C\%_{HCldư}=\dfrac{7,3.100\%}{206,3}=3,54\%\)
\(C\%_{ZnCl_2}=\dfrac{0,1.136.100\%}{206,3}=6,59\%\)
Đúng 3
Bình luận (0)
Bài 1.
\(n_{H_2}=\dfrac{0,224}{22,4}=0,01mol\)
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
0,01 0,01 ( mol )
\(m_{Ba}=0,01.137=1,37g\)
\(\%m_{Ba}=\dfrac{1,37}{2,9}.100=47,24\%\)
\(\%m_{BaO}=100\%-47,24\%=52,76\%\)
\(m_{BaO}=2,9-1,37=1,53g\)
\(n_{BaO}=\dfrac{1,53}{153}=0,01mol\)
\(BaO+H_2O\rightarrow Ba\left(OH\right)_2\)
0,01 0,01 ( mol )
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
0,01 0,01 ( mol )
\(m_{Ba\left(OH\right)_2}=\left(0,01+0,01\right).171=3,42g\)
Bài 2.
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(m_{HCl}=200.7,3\%=14,6g\)
\(n_{HCl}=\dfrac{14,6}{36,5}=0,4mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 < 0,4 ( mol )
0,1 0,2 0,1 0,1 ( mol )
\(m_{HCl\left(dư\right)}=\left(0,4-0,2\right).36,5=7,3g\)
\(V_{H_2}=0,1.22,4=2,24l\)
Đúng 1
Bình luận (0)
Cho 21,1 gan hỗn hợp gồm zn và zno tác dụng với dd hcl dư, thu được 4,48 lít khí(đktc).a)tính phần trăm kl mỗi chất có trong hỗn hợp.b)phải dùng bao nhiêu ml dd hcl 2M đủ để hòa tan hết hỗn hợp trên.
Xem chi tiết
pthh: Zn+HCl→ZnCl2+H2 (1)
ZnO+HCl→ZnCl2+H2O (2)
theo bài ra số mol của H2=0,2 (mol)
theo pt1 ta có nZn=nH2=0,2 (mol)
⇒ mZn=0,2 .65=13 (g)→mZnO=21,1-13=8,1 (g) →nZnO=0,1 (mol)
%Zn=13.100%/21,1=61,61%
%ZnO=38,39%
Theo pt 1 nHCl=2nZn=0,4(mol) (3)
Theo pt2 nHCl=2nZnO=0,4 (mol) (4)
Từ 3,4 ⇒nHCl=0,8 (mol)
V HCl=0,4 (lít)=400ml
Đúng 2
Bình luận (1)
Cho m(g) hỗn hợp gồm 2 kim loại nhôm và kẽm vào dd HCL dư thì thu được 4,48 lít khí(đktc).Mặt khác chom (g) hỗn hợp 2 kim loại này vào dd HNO3 đặc nguội thì thu được 2,24 lít khí(đktc) màu nâu đỏ. 1.Viết phương trình phản ứng xảy ra. 2.Tính khối lượng hỗn hợp đầu.
1)
Zn + 2HCl --> ZnCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
Zn + 4HNO3 --> Zn(NO3)2 + 2NO2 + 2H2O
2)
TN2:
\(n_{NO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Zn + 4HNO3 --> Zn(NO3)2 + 2NO2 + 2H2O
_____0,05<--------------------------0,1
=> nZn = 0,05 (mol)
TN1:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
____0,05--------------------->0,05
2Al + 6HCl --> 2AlCl3 + 3H2
0,1<-----------------------0,15
=> m = 0,05.65 + 0,1.27 = 5,95(g)
Đúng 0
Bình luận (0)
hỗn hợp X gồm 3 kim loại Al,Fe,Cu cho m (g) X vào CuSO4 dư sau phản ứng thu được 35,2 g kim loại , nếu hòa tan m(g) X vào 500 ml dd HCl 2M thì thu được 8,96 (lít) khí (ở đktc) ,dung dịch Y và thu được a(g) chất rắn.tìm a
Để hoà tan 6,5 g kẽm cần dùng bao nhiêu ml dung dịch HCl 2M ? tính C(M) của dd thu được
Đọc tiếp
Để hoà tan 6,5 g kẽm cần dùng bao nhiêu ml dung dịch HCl 2M ? tính C(M) của dd thu được
Zn+2HCl->ZnCl2+H2
0,1----0,2----0,1
n Zn =0,1 mol
VHCl=\(\dfrac{0,2}{2}=0,1l=100ml\)
=>CM dd =\(\dfrac{0,1}{0,1}=1M\)
Đúng 2
Bình luận (0)
Cho 14,3 g hỗn hợp A gồm Al Zn Mg tác dụng vừa đủ với V(ml) dd HCl 2M, sau phản ứng người ta thu được dd B và 11,2L khí H2 ở (đktc)
a) tính V
b) Cô cạn dung dịch B Hỏi thu được bao nhiêu gam hỗn hợp muối khan
c) Tính thành phần % của hỗn hợp A theo khối lượng biết tỉ lệ mol của Mg và Al 1:1
d) Cho dung dịch xút (dư) vào dd B ta được kết tủa C. Lọc kết tủa C (đem nung đến khối lượng không đổi ta được m(g) chất rắn D tính m
Giúp mình vớiii
Đọc tiếp
Cho 14,3 g hỗn hợp A gồm Al Zn Mg tác dụng vừa đủ với V(ml) dd HCl 2M, sau phản ứng người ta thu được dd B và 11,2L khí H2 ở (đktc) a) tính V b) Cô cạn dung dịch B Hỏi thu được bao nhiêu gam hỗn hợp muối khan c) Tính thành phần % của hỗn hợp A theo khối lượng biết tỉ lệ mol của Mg và Al 1:1 d) Cho dung dịch xút (dư) vào dd B ta được kết tủa C. Lọc kết tủa C (đem nung đến khối lượng không đổi ta được m(g) chất rắn D tính m Giúp mình vớiii
Hỗn hợp X gồm Mg, Al, Zn. Cho 6,5 gam hỗn hợp X vào 200 ml dung dịch
B
a
(
O
H
)
2
0,5M và KOH 1M, kết thúc phản ứng thu được 4,256 lít khí
H
2
(đktc). Nếu cho 13 gam hỗn hợp X tác dụng với một lượng dung dịch
H
2
S
O
4
loãng đến khi ngừng...
Đọc tiếp
Hỗn hợp X gồm Mg, Al, Zn. Cho 6,5 gam hỗn hợp X vào 200 ml dung dịch B a ( O H ) 2 0,5M và KOH 1M, kết thúc phản ứng thu được 4,256 lít khí H 2 (đktc). Nếu cho 13 gam hỗn hợp X tác dụng với một lượng dung dịch H 2 S O 4 loãng đến khi ngừng thoát khí thu được 4,032 lít H 2 (đktc) và chất rắn không tan Y. Cho Y vào 200 ml dung dịch chứa AgNO3 1M và C u N O 3 2 2M, sau khi phản ứng xảy ra hoàn toàn thu được 34,4 gam chất rắn X. Thành phần phần trăm số mol của Zn trong X là
A. 40%
B. 26,31%
C. 21,05%
D. 30,25%
Hòa tan hoàn toàn 5,2 gam hỗn hợp X gồm Na, Ba và Al vào 200 mL dung dịch NaOH 0,1M, thu được 2,464 lít khí
H
2
(đktc) và dung dịch Y. Cho từ từ dung dịch HCl 2M vào Y, khi hết 50 mL thu được 2a gam kết tủa, còn khi hết 75 mL thì thu được 3a gam kết tủa. Nếu sục từ từ khí
C
O
2
vào Y thì thu được tối đa bao nhiêu gam kết tủa? A. 7,06 gam B. 6,24 gam C. 6,69 gam D. 7,84 gam
Đọc tiếp
Hòa tan hoàn toàn 5,2 gam hỗn hợp X gồm Na, Ba và Al vào 200 mL dung dịch NaOH 0,1M, thu được 2,464 lít khí H 2 (đktc) và dung dịch Y. Cho từ từ dung dịch HCl 2M vào Y, khi hết 50 mL thu được 2a gam kết tủa, còn khi hết 75 mL thì thu được 3a gam kết tủa. Nếu sục từ từ khí C O 2 vào Y thì thu được tối đa bao nhiêu gam kết tủa?
A. 7,06 gam
B. 6,24 gam
C. 6,69 gam
D. 7,84 gam
Câu 12: Cho 9,2 gam hỗn hợp Mg và Fe vào 200 ml dung dịch HCL. Sau phản ứng thu được 5,6 lít khí ở đktc. a./ Tỉnh thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu. b./ Tính nồng độ mol của dd HCl đã dùng Cho biết: Zn = 65 Cl = 35.5 Mg = 24 Al = 27 , Mg = 24 Fe = 56
a, Ta có: 24nMg + 56nFe = 9,2 (g) (1)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
BT e, có: 2nMg + 2nFe = 2nH2 = 0,5 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,15\left(mol\right)\\n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,15.24}{9,2}.100\%\approx39,13\%\\\%m_{Fe}\approx60,87\%\end{matrix}\right.\)
b, BTNT H, có: \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\Rightarrow C_{M_{HCl}}=\dfrac{0,5}{0,2}=2,5\left(M\right)\)
Đúng 3
Bình luận (0)