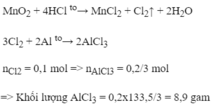cho 30,45g MnO2 với V đe HCL 1M đặc nóng . a) tính khối lượng khí Clo thu được và V . b) lấy toàn bộ khí clo thu được phản ứng hoàn toàn 25.2g Fe , tính khối lượng muối thu được

Những câu hỏi liên quan
Câu 1: cho 2,24 lít khí clo phản ứng với Na. Tính khối lượng muối thu được( Na=23, Cl=35,5)
Câu 2: Hòa tan hoàn toàn 1,45g hỗn hợp 3 kim loại Zn,Mg, Fe bằng dung dịch HCl dư thấy thoát ra 0,896 lít khí (đktc). Tính khối lượng muối khan thu được sau phản ứng.
Câu 1:
PTHH: \(Na+\dfrac{1}{2}Cl_2\xrightarrow[]{t^o}NaCl\)
Ta có: \(n_{NaCl}=2n_{Cl_2}=2\cdot\dfrac{2,24}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow m_{NaCl}=0,2\cdot58,5=11,7\left(g\right)\)
Đúng 2
Bình luận (0)
Câu 2:
Ta có: \(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\) \(\Rightarrow m_{H_2}=0,04\cdot2=0,08\left(g\right)\)
Bảo toàn nguyên tố: \(n_{HCl}=2n_{H_2}=0,08\left(mol\right)\) \(\Rightarrow m_{HCl}=0,08\cdot36,5=2,92\left(g\right)\)
Bảo toàn khối lượng: \(m_{muối}=m_{KL}+m_{HCl}-m_{H_2}=4,29\left(g\right)\)
Đúng 3
Bình luận (0)
Câu 2 :
nH2 = 0.896 / 22.4 = 0.04 (mol)
nHCl = 2nH2 = 0.04 * 2 = 0.08 (mol)
mHCl = 0.08 * 36.5 =2.92 (g)
BTKL :
mM = mKl + mHCl - mH2 = 1.45 + 2.92 - 0.04*2 = 4.29 (g)
Đúng 2
Bình luận (0)
nung nóng 22,12 gam KMnO4 và 18,375 gam KClO3, sau một thời gian thu được chất rắn X gồm 6 chất có khối lượng 37,295 gam. Cho X tác dụng với dung dịch HCl đặc dư, đun nóng. Toàn bộ lượng khí clo thu được cho phản ứng hết với m gam bột Fe đốt nóng được chất nóng Y. Hòa tan hoàn toàn Y vào nước được dung dịch Z. thêm AgNO3 dư vào dung dịch Z đến khi phản ứng hoàn toàn được 204,6 gam kết tủa. Giá trị m là A. 22,44 B. 28,0 C. 33,6 D. 25,2
Đọc tiếp
nung nóng 22,12 gam KMnO4 và 18,375 gam KClO3, sau một thời gian thu được chất rắn X gồm 6 chất có khối lượng 37,295 gam. Cho X tác dụng với dung dịch HCl đặc dư, đun nóng. Toàn bộ lượng khí clo thu được cho phản ứng hết với m gam bột Fe đốt nóng được chất nóng Y. Hòa tan hoàn toàn Y vào nước được dung dịch Z. thêm AgNO3 dư vào dung dịch Z đến khi phản ứng hoàn toàn được 204,6 gam kết tủa. Giá trị m là
A. 22,44
B. 28,0
C. 33,6
D. 25,2
Chọn đáp án B
Ta có
![]()
=0,2
![]()
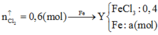
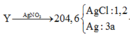
![]()
=>a=0,1(mol)
![]()
Đúng 0
Bình luận (0)
cho 5 ,4 gam al tác dụng với dung dịch hcl phản ứng xảy ra hoàn toàn . Dẫn toàn bộ lượng khí thu được qua CuO nung nóng .
a.viết phương trình hóa học của phản ứng xảy ra .tính khối lượng muối thu được saub phản ứng
b. tính khối lượng Cu qua phản ứng
a) nAl=0,2(mol)
PTHH: 2 Al + 6 HCl -> 2 AlCl3 + 3 H2
H2 + CuO -to-> Cu + H2O
nAlCl3= nAl= 0,2(mol)
=> mAlCl3= 133,5. 0,2= 26,7(g)
b) nCu= nH2= 3/2 . 0,2=0,3(mol)
=> mCu= 0,3.64=19,2(g)
(Qua phản ứng nghe kì á, chắc tạo thành chứ ha)
<3
Đúng 4
Bình luận (0)
Câu 8: Hỗn hợp X gồm Fe và Cu
* Cho a gam hỗn hợp X tác dụng hoàn toàn với khí clo dư thu được 59,5 gam muối
* Cho a hỗn hợp X tác dụng hoàn toàn với dung dịch HCL 36,5% thu được 25,4 gam muối
a: Tính giá trị a(g) và % khối lượng mỗi muối sau phản ứng
b: Tính thể tích dung dịch HCL 36,5%(D=1,25g/ml) cần dùng
a) Gọi x,y lần lượt là số mol Fe, Cu trong hhX (x,y>0) (mol)
- Khi cho X t/d hoàn toàn với khí Clo dư:
\(2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ Cu+Cl_2\rightarrow\left(t^o\right)CuCl_2\\ \Rightarrow162,5x+135y=59,5\left(1\right)\)
- Khi cho X tác dụng hoàn toàn với dd HCl 36,5%. Cu sẽ không tác dụng mà chỉ có Fe tham gia phản ứng.
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ m_{FeCl_2}=127x=25,4\left(g\right)\left(2\right)\\ \left(1\right),\left(2\right)\Rightarrow\left\{{}\begin{matrix}162,5x+135y=59,5\\127x=25,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,2\end{matrix}\right.\\ \Rightarrow a=m_{hhX}=m_{Fe}+m_{Cu}=64x+56y=64.0,2+56.0,2=24\left(g\right)\)
Tính phần trăm mỗi muối sau phản ứng chắc ở phản ứng với Clo dư.
\(\%m_{FeCl_3}=\dfrac{0,2.162,5}{0,2.162,5+0,2.135}.100\approx54,622\%\\ \Rightarrow\%m_{CuCl_2}\approx45,378\%\)
b)
\(n_{HCl}=2x=2.0,2=0,4\left(mol\right)\\ \Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\\ \Rightarrow m_{ddHCl}=\dfrac{14,6.100}{36,5}=40\left(g\right)\\ \Rightarrow V_{ddHCl}=\dfrac{m_{ddHCl}}{D_{ddHCl}}=\dfrac{40}{1,25}=32\left(ml\right)=0,032\left(l\right)\)
Đúng 0
Bình luận (0)
Cho 3,2g natri tác dụng hoàn toàn với khí clo thu được 5,85 natri clorua . tính khối lượng khí clo đã phản ứng.
Cho 2,24 lít khí metan (đktc) phản ứng hoàn toàn với V lít khí C l 2 cùng điều kiện thu được chất A và HCl. Biết clo chiếm 83,53% khối lượng của A. Giá trị của V là
A. 2,24.
B. 4,48.
C. 3,36.
D. 6,72.
Cho dung dịch chứa 0,4 mol HCl tác dụng với M n O 2 (dư) thu được khí clo. Khí clo tạo ra phản ứng hết với nhôm. Tính khối lượng A l C l 3 thu được (Al=27, Cl=35,5).
cho 13g kém vào dung dịch HCL đến phản ứng hàn toàn thu được FeCl2 và khí H2/
a) Viết phương trình phản ứng
b)Tính khối lượng muối FeCl2 thu được
c)Dẫn Toàn bộ khí H2 tren qua bình đựng bột đồng(II) oxi đun nóng,Tính khối lượng đồng thu được sau phản yuwngs
Giúp Mình với MN ơi
Mai mình ktra rồi
CẢM ƠN MN
\(a,n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\left(1\right)\\ Theo.pt\left(1\right):n_{ZnCl_2}=n_{H_2}=0,2\left(mol\right)\\ b,m_{ZnCl_2}=0,2.136=27,2\left(g\right)\\ c,PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\left(2\right)\\ THeo.pt\left(2\right):n_{Cu}=n_{H_2}=0,2\left(mol\right)\\ m_{Cu}=0,2.64=12,8\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 1 Hoà tan hoàn toàn m gam Mg cần vừa đủ 200( gam) dung dịch HCL 7,3%, sau phản ứng thu được V lít khí H2 (Đktc) a, Tìm m, V b, Gọi tên muối và tính khối lượng muối thu được c, Tính khối lượng H2 thu được sau phản ứng
Khối lượng của axit clohidric
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{7,3.200}{100}=14,6\left(g\right)\)
Số mol của axit clohidric
nHCl= \(\dfrac{m_{HCl}}{M_{HCl}}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
Pt : Mg + 2HCl → MgCl2 + H2\(|\)
1 2 1 1
0,2 0,4 0,2 0,2
a) Số mol của magie
nMg= \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Khối lượng của magie
mMg = nMg . MMg
= 0,2 . 24
= 4,8 (g)
Số mol của khí hidro
nH2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Thể tích của khí hidro
VH2 = nH2 . 22,4
= 0,2 . 22,4
= 4,48 (l)
b) Tên của muối là : magie clorua
Số mol của muối magie clorua
nMgCl2 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của muối magie clorua
mMgCl2 = nMgCl2 . MMgCl2
= 0,2 . 95
= 19 (g)
c) Khối lượng của khí hidro
mH2 = nH2 . MH2
= 0,2 . 2
= 0,4 (g)
Chúc bạn học tốt
Đúng 4
Bình luận (1)
mHCl=14,6(g) -> nHCl=0,4(mol)
PTHH: Mg + 2 HCl -> MgCl2 + H2
a) Ta có: nH2=nMgCl2=nMg=1/2. nHCl=1/2. 0,4=0,2(mol)
m=mMg=0,2.24=4,8(g)
b) mMgCl2=0,2.95=19(g)
c) mH2=0,2.2=0,4(g)
Đúng 1
Bình luận (1)