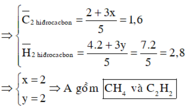Những câu hỏi liên quan
Trộn khí C2H4 với khí CxHy theo tỉ lệ 3:2 về thể tích được hỗn hợp X có tỉ khối so với khí H2 là 16,8 (các khí đo ở điều kiện tiêu chuẩn). Tính khối lượng mol của CxHy. Xác Định Công thức phân tử của CxHy biết tỉ lệ khối lượng các nguyên tố trong CxHy là mC:mH=6
Xem chi tiết
\(\dfrac{m_C}{m_H} = 6\\ \Rightarrow \dfrac{x}{y} = \dfrac{n_C}{n_H} = 6 : \dfrac{12}{1} = \dfrac{1}{2}(1)\)
Ta có :
\(M_X = \dfrac{3.28 + 2.(12x+y)}{3+2}=16,8.2\\ \Rightarrow 12x + y = 42(2)\)
Từ (1)(2) suy ra : x = 3 ; y = 6
Vậy CTPT cần tìm : C3H6
Đúng 0
Bình luận (0)
Trộn 2 lít CH4 với 1 lít CxHy được hỗn hợp khí A có tỉ khối so với heli là 7,5 ( các khí đo ở cùng đk t°,p).Xác định công thức phân tử của CxHy trong phân tử CxHy nguyên tố cacbon chiếm 82,76% về khối lượng
Xem chi tiết
\(\%C = \dfrac{12x}{12x + y}.100\% = 82,76\%\\ \Rightarrow 2,5x = y(1)\)
Ta có :
\(M_A = \dfrac{2.16 + 1.(12x + y)}{2 + 1} = 7,5.4\\ \Rightarrow 12x + y = 58(2)\)
Từ (1)(2) suy ra x = 4 ; y = 10
Vậy CTPT của hợp chất cần tìm : C4H10
Đúng 0
Bình luận (2)
đốt cháy một lượng khí A thu được 105,6 gam CO2 và 57,6 gam H2O. tìm công thức phân tử của khí A biết tỉ khối của khí A so với CH4 bằng 2,75
trộn khí A với N2 theo tỉ lệ 8:2 về khối lượng thu được hỗn hợp khí D. tính thể ở điều kiện tiêu chuẩn của 13,408 gam hỗn D
trộn V1 lít CH4 với V2 lít C2H4 thu được hỗn hợp khí X có khối lượng riêng bằng khối lượng riêng của C2H2 (các thể tích khí đo ở điều kiện tiêu chuẩn).Tỉ lệ thể tích V1:V2 bằng
a. 1:3
b. 1:4
c. 1:5
d. 1:6
Ta có
`\overline(M)=(16V_1+28V_2)/(V_1+V_2)=26`
`=>10V_1=2V_2`
`=>V_1:V_2=2:10=1:5`
`->C`
Đúng 2
Bình luận (0)
Hỗn hợp khí X gồm 1 anken và H2 có tỉ lệ số mol là 1 : 1, (đo ở 90oC và 1 atm). Nung nóng X với bột Ni một thời gian rồi đưa về điều kiện ban đầu được hỗn hợp khí Y có tỉ khối hơi so với H2 là 23,2. Xác định công thức phân tử của anken và hiệu suất phản ứng hiđro hóa: A. C6H12, H 45% B. C5H10, H 44,83%. C. C3H6, H 75% D. C4H8, H 54,45%
Đọc tiếp
Hỗn hợp khí X gồm 1 anken và H2 có tỉ lệ số mol là 1 : 1, (đo ở 90oC và 1 atm). Nung nóng X với bột Ni một thời gian rồi đưa về điều kiện ban đầu được hỗn hợp khí Y có tỉ khối hơi so với H2 là 23,2. Xác định công thức phân tử của anken và hiệu suất phản ứng hiđro hóa:
A. C6H12, H = 45%
B. C5H10, H = 44,83%.
C. C3H6, H = 75%
D. C4H8, H = 54,45%
Hỗn hợp khí A chứa hai hiđrocacbon, hỗn hợp khí B chứa O2 và O3 (tỉ khối của B so với H2 là 18,4). Trộn A và B theo tỉ lệ 1 : 2 về thể tích rồi đốt cháy thì chỉ còn CO2 và hơi H2O theo tỉ lệ 8 : 7 về thể tích. Nếu dẫn 5 lít A qua nước brom dư thì thể tích khí còn lại 2 lít. Công thức phân tử của hai hiđrocacbon là (các thể tích khí đo cùng điều kiện nhiệt độ, áp suất) A. CH4 và C3H6. B. CH4 và C4H2. C. CH4 và C2H2. D. CH4 và C3H4.
Đọc tiếp
Hỗn hợp khí A chứa hai hiđrocacbon, hỗn hợp khí B chứa O2 và O3 (tỉ khối của B so với H2 là 18,4). Trộn A và B theo tỉ lệ 1 : 2 về thể tích rồi đốt cháy thì chỉ còn CO2 và hơi H2O theo tỉ lệ 8 : 7 về thể tích. Nếu dẫn 5 lít A qua nước brom dư thì thể tích khí còn lại 2 lít. Công thức phân tử của hai hiđrocacbon là (các thể tích khí đo cùng điều kiện nhiệt độ, áp suất)
A. CH4 và C3H6.
B. CH4 và C4H2.
C. CH4 và C2H2.
D. CH4 và C3H4.
Đốt cháy hoàn toàn 2,82 gam chất hữu cơ A cần 2,856 lít khs O2 thu được khí CO2 và hơi nước theo tỉ lệ thể tích Vco2/Vh2o = 4/3 ( các khi đo ở điều kiện tiêu chuẩn ) . Hãy xác định công thức phân tử của A . Biết tỉ khối của A với không khí nhỏ hơn 7
Ta có: \(n_{O_2}=\dfrac{2,856}{22,4}=0,1275\left(mol\right)\)
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{4}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{4}{3}\)
Gọi: nCO2 = 4x (mol) ⇒ nH2O = 3x (mol)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ 2,82 + 0,1275.32 = 4x.44 + 3x.18
⇒ x = 0,03
⇒ nCO2 = 0,03.4 = 0,12 (mol) = nC
nH2O = 0,03.3 = 0,09 (mol) ⇒ nH = 0,09.2 = 0,18 (mol)
Ta có: mC + mH = 0,12.12 + 0,18.1 = 1,62 (g) < 2,82 (g)
→ A chứa C, H và O.
⇒ mO = 2,82 - 1,62 = 1,2 (g) \(\Rightarrow n_O=\dfrac{1,2}{16}=0,075\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,12:0,18:0,075 = 8:12:5
→ CTPT của A có dạng là (C8H12O5)n (n nguyên dương)
Mà: \(M_A< 29.7=203\left(g/mol\right)\)
\(\Rightarrow\left(12.8+12.1+16.5\right)n< 203\)
⇒ n < 1,08 ⇒ n = 1
Vậy: CTPT của A là C8H12O5.
Đúng 1
Bình luận (2)
Đốt cháy hoàn toàn 0,1 mol khí CxHy cần 6,72 lít khí oxi (ở đktc). Sau phản ứng thu được 8,8 gam khí cacbonic và 3,6 gam nước. Tính Khối lượng mol và xác định công thức hóa học của CxHy, biết tỉ lệ giữa x và y là 1:2.
$n_{CO_2} = \dfrac{8,8}{44} = 0,2(mol) ; n_{H_2O} = \dfrac{3,6}{18} = 0,2(mol)$
$C_xH_y + (x + \dfrac{y}{4})O_2 \xrightarrow{t^o} xCO_2 + \dfrac{y}{2}H_2O$
Theo PTHH :
$0,1.x = 0,2$ và $0,1.\dfrac{y}{2} = 0,2$
Suy ra : x = 2 ; y = 4
Vậy CTHH cần tìm là $C_2H_4$(M = 28)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 12g hỗn hợp (gồm Fe và Cu có tỉ lệ mol là 1:1) bằng axit HNO3, thu được V lít hỗn hợp khí X (gồm NO và NO2) và dung dịch Y. Tỉ khối của X với H2 là 19. Tính V (biết các khí đo ở điều kiện tiêu chuẩn)
Gọi: nFe = nCu = x (mol)
⇒ 56x + 64x = 12 ⇒ x = 0,1 (mol)
Gọi: \(\left\{{}\begin{matrix}n_{NO}=a\left(mol\right)\\n_{NO_2}=b\left(mol\right)\end{matrix}\right.\)
BT e, có: 3nFe + 2nCu = 3nNO + nNO2
⇒ 3a + 2b = 0,5 (1)
Mà: Tỉ khối của X với H2 là 19.
\(\Rightarrow\dfrac{30a+46b}{a+b}=19.2\left(2\right)\)
Từ (1) và (2) ⇒ a = b = 0,1 (mol)
\(\Rightarrow V_{hh}=\left(0,1+0,1\right).22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)