cho 10,6g Na2CO3 tác dụng vừa đủ với CaCl2,phản ứng xảy ra hoàn toàn thu được NaCl và CaCO3.tính khối lượng các chất tạo thành sau phản ứng

Những câu hỏi liên quan
Cho 22,2g CaCl2 , tác dụng vừa đủ với AgNO3 , phản ứng xảy ra hoang toàn thu được AgCl và Ca(NO3)2.Tính khối lượng AgCl tạo thành
Xem chi tiết
\(n_{CaCl_2}=\dfrac{22.2}{111}=0.2\left(mol\right)\)
\(CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl\)
\(0.2....................................................0.4\)
\(m_{AgCl}=0.4\cdot143.5=57.4\left(g\right)\)
Đúng 5
Bình luận (0)
nCaCl2=22,2/111=0,2(mol)
CaCl2 + 2AgNO3 -----> 2AgCl + Ca(NO3)2
TPT:nAgCl=2.nCaCl2=2.0,2=0,4(mol)
mAgCl=0,4.143,5=57,4(g)
Đúng 0
Bình luận (0)
Bài 8: Cho 10,6 g Na2CO3 tác dụng vừa đủ với CaCl2. Tính khối lượng các chất tạo thành sau phản ứng
-nNa2CO3= m/M = 10,6/106 = 0,1 (mol)
-PT:Na2CO3+CaCl2->CaCO3+2NaCl
____0,1____________0,1______0,2
-mCaCO3= n.M = 0,1.100 = 10 (g)
-mNaCl= n.M = 0,2.58,5 = 11,7 (g)
Đúng 4
Bình luận (0)
\(n_{Na_2CO_3}=\dfrac{10.6}{106}=0.1\left(mol\right)\\ PTHH:CaCl_2+Na_2CO_3\rightarrow CaCO_3+2NaCl\\ n_{CaCO_3}=n_{Na_2CO_3}=0,1\left(mol\right)\\ \Rightarrow m_{CaCO_3}=0,1.100=10g\)
$n_{NaCl}=n_{Na_2CO_3}=0,1.2=0,2(mol)$
`=>` $m_{NaCl}=0.2.58,5=11,7g$
Đúng 0
Bình luận (2)
Thực hiện phản ứng nhiệt nhôm hỗn hợp bột X (gồm Al và một oxit sắt) sau phản ứng thu được 92,35 gam chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư, phản ứng xong vẫn còn phần không tan Z và thu được 8,4 lít khí E (đktc). Cho 1/4 lượng chất Z tan hoàn toàn trong dung dịch H2SO4 đặc nóng cần vừa đủ 60 gam H2SO4 98%. Biết các phản ứng xảy ra hoàn toàn . Khối lượng Al2O3 tạo thành có chứa trong chất rắn Y là: 98%. Biết các phản ứng xảy ra hoàn toàn. Khối lượng Al2O3 tạo thành có chứa trong chất r...
Đọc tiếp
Thực hiện phản ứng nhiệt nhôm hỗn hợp bột X (gồm Al và một oxit sắt) sau phản ứng thu được 92,35 gam chất rắn Y. Cho Y tác dụng với dung dịch NaOH dư, phản ứng xong vẫn còn phần không tan Z và thu được 8,4 lít khí E (đktc). Cho 1/4 lượng chất Z tan hoàn toàn trong dung dịch H2SO4 đặc nóng cần vừa đủ 60 gam H2SO4 98%. Biết các phản ứng xảy ra hoàn toàn . Khối lượng Al2O3 tạo thành có chứa trong chất rắn Y là: 98%. Biết các phản ứng xảy ra hoàn toàn. Khối lượng Al2O3 tạo thành có chứa trong chất rắn Y là
A. 38,08 gam
B. 40,8 gam
C. 24,48 gam
D. 48,96 gam
Do khi phản ứng với NaOH tạo khí nên Al dư, oxit sắt hết .
Z là Fe.
2Fe+ 6H2SO4 → Fe2(SO4)3 + 3SO2 + 6H2O
=> n Fe = 0,2 mol => n Fe (Z)= 0,8 mol
Lại có n H2 = 0,375 mol
=> nAl (Z) =0,25 mol
=> m Al2O3(Z)= 92,35 – 56.0,8 – 0,25.27 =40,8 g =>B
Đúng 0
Bình luận (0)
Bài 1: Cho 32g Oxi tác dụng vừa đủ với Magie.
a. Tìm khối lượng của Mg trong phản ứng .
b. Tìm khối lượng của Magie oxit tạo thành.
Bài 2: Cho 10g CaCo3 vào một bình kín rồi đun nóng tới khi phản ứng xảy ra hoàn toàn thì thu được CaO và CO2
a. Tìm thể tích khí CO2 ở đktc
b. Tính khối lượng CaO tạo thành sau phản ứng
Bài 2 :
\(n_{CaCO3}=\dfrac{10}{100}=0,1\left(mol\right)\)
Pt : \(CaCO_3\underrightarrow{t^o}CaO+CO_2|\)
1 1 1
0,1 0,1 0,1
a) \(n_{CO2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(V_{CO2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
b) \(n_{CaO}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{CaO}=0,1.56=5,6\left(g\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
Bài 1 :
\(n_{O2}=\dfrac{32}{32}=1\left(mol\right)\)
Pt : \(O_2+2Mg\underrightarrow{t^o}2MgO|\)
1 2 2
1 2 1
a) \(n_{Mg}=\dfrac{1.2}{1}=2\left(mol\right)\)
⇒ \(m_{Mg}=2.24=48\left(g\right)\)
c) \(n_{MgO}=\dfrac{2.1}{2}=1\left(mol\right)\)
⇒ \(m_{MgO}=1.40=40\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Cho 22,2g CaCl2, tác dụng vừa đủ vs AgNO3
a.Tính khối lượng AgNO3
b.Tính khối lượng các chất còn lại trong phản ứng
Cho 10,6g Na2CO3 tác dụng vừa đủ vs CaCl2 . Tính Khối lượng các chất tạo thành sau phản ứng
\(PTHH:CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl\downarrow\)
\(n_{CaCl_2}=\frac{22,2}{111}=0,2\left(mol\right)\)
Theo PT: \(n_{AgNO_3}=2n_{CaCl_2}=0,4\left(mol\right)\)
\(\Rightarrow m_{AgNO_3}=0,4.170=68\left(g\right)\)
b) Các chất còn lại trong phản ứng là Ca(NO3)2, AgCl
\(TheoPT:n_{Ca\left(NO_3\right)_2}=n_{CaCl_2}=0,2\left(mol\right)\)
\(n_{AgCl}=2n_{CaCl_2}=0,4\left(mol\right)\)
\(\Rightarrow m_{Ca\left(NO_3\right)_2}=0,2.164=32,8\left(g\right)\)
\(m_{AgCl}=0,4.143,5=57,4\left(g\right)\)
Đúng 0
Bình luận (1)
CaCl2 + 2AgNO3 → Ca(NO3)2 + 2AgCl
\(n_{CaCl_2}=\frac{22,2}{111}=0,2\left(mol\right)\)
a) Theo PT: \(n_{AgNO_3}=2n_{CaCl_2}=2\times0,2=0,4\left(mol\right)\)
\(\Rightarrow m_{AgNO_3}=0,4\times170=68\left(g\right)\)
b) Theo PT: \(n_{Ca\left(NO_3\right)_2}=n_{CaCl_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Ca\left(NO_3\right)_2}=0,2\times164=32,8\left(g\right)\)
Theo PT: \(n_{AgCl}=n_{AgNO_3}=0,4\left(mol\right)\)
\(\Rightarrow m_{AgCl}=0,4\times143,5=57,4\left(g\right)\)
Đúng 2
Bình luận (0)
Na2CO3 + CaCl2 → 2NaCl + CaCO3
\(n_{Na_2CO_3}=\frac{10,6}{106}=0,1\left(mol\right)\)
Theo pT: \(n_{CaCO_3}=n_{Na_2CO_3}=0,1\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,1\times100=10\left(g\right)\)
Theo pT: \(n_{NaCl}=2n_{Na_2CO_3}=2\times0,1=0,2\left(mol\right)\)
\(\Rightarrow m_{NaCl}=0,2\times58,5=11,7\left(g\right)\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
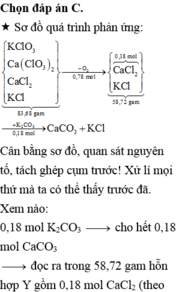
Nhiệt phân 83,68 gam hỗn hợp gồm KClO3, Ca(ClO3)2, CaCl2, KCl thu được chất rắn X và 17,472 lít khí (đktc). Chất rắn X được hỏa tan vào nước, sau đó dung dịch tạo thành cho phản ứng vừa đủ với 360 ml dung dịch K2CO3 0,5M thu được kết tủa Y và dung dịch Z. Biết các phản ứng xảy ra hoàn toàn. Khối lượng chất tan có trong dung dịch Z là A. 48,62 gam B. 43,25 gam C. 65,56 gam D. 36,65 gam
Đọc tiếp
Nhiệt phân 83,68 gam hỗn hợp gồm KClO3, Ca(ClO3)2, CaCl2, KCl thu được chất rắn X và 17,472 lít khí (đktc). Chất rắn X được hỏa tan vào nước, sau đó dung dịch tạo thành cho phản ứng vừa đủ với 360 ml dung dịch K2CO3 0,5M thu được kết tủa Y và dung dịch Z. Biết các phản ứng xảy ra hoàn toàn. Khối lượng chất tan có trong dung dịch Z là
A. 48,62 gam
B. 43,25 gam
C. 65,56 gam
D. 36,65 gam
Cho 17,3 gam hỗn hợp gồm 2 kim loại Al và Zn tác dụng với 400 gam dung dịch HCl. Sau khi phản ứng xảy ra hoàn toàn (các chất phản ứng vừa đủ) thì thu được 15,68l H2 (đktc) a. viết phương trình phản ứng xảy ra b.Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu c. Tính C% mỗi muối thu được sau phản ứng
Nung m1 gam Mg dư với lượng SiO2 thu được hỗn hợp chất rắn Y. Cho Y tác dụng vừa đủ với 300ml dung dịch HCl 2M (đktc) thu được 2,24 lít khí H2 (đktc). Tính lượng Si tạo thành. Biết các phản ứng xảy ra hoàn toàn.
A. 1,4 gam
B. 2,8 gam
C. 5,6 gam
D. 7,0 gam
Đáp án B
PTHH: 2Mg + SiO2 → 2MgO + Si (1)
Chất rắn Y chứa MgO, Si và Mg dư
MgO + 2HCl → MgCl2+ H2O (2)
Mg + 2HCl → MgCl2+ H2 (3)
Ta có: nHCl= 0,3.2= 0,6 mol; nH2= 0,1 mol
Theo PT (3): nMg= nH2= 0,1 mol;
nHCl PT 3= 2.nH2= 0,2 mol
→nHCl PT 2= 0,6- 0,2= 0,4 mol → nMgO= 0,2 mol
Theo PT (1): nSi=0,5 nMgO= 0,1 mol
→mSi= 0,1.28= 2,8 gam
Đúng 0
Bình luận (0)
Cho m gam Al tác dụng vừa đủ với 300 ml dung dịch CuSO4 1M, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X và m1 gam Cu. (a) Viết PTHH xảy ra. (b) Tính khối lượng nhôm (m) đã tham gia phản ứng. (c) Tính khối lượng Cu (m1) sinh ra
Ta có: \(n_{CuSO_4}=0,3\left(mol\right)\)
a, PT: \(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
______0,2____0,3_________________0,3 (mol)
b, \(m_{Al}=0,2.27=5,4\left(g\right)\)
c, \(m_{Cu}=0,3.64=19,2\left(g\right)\)
Bạn tham khảo nhé!
Đúng 4
Bình luận (0)