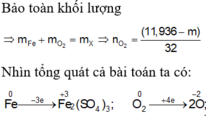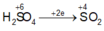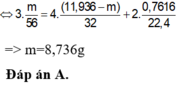Để a gam bột Fe ngoài không khí sau 1 thời gian sẽ chuyển thành hỗn hợp A có khối lượng 75,2g gồm FeO,Fe ,Fe2O3,Fe3O4.Cho hỗn hợp A phản ứng hết với H2SO4 đậm đạc nóng thu đc 6,72l khí SO2 (đktc).tính a ?

Những câu hỏi liên quan
Để m gam bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp A có khối lượng 37,6 gam gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp A phản ứng hết với H2SO4 đặc, nóng, dư thu được 3,36 lít khí SO2 (đktc). Giá trị của m là A. 56,0. B. 28,0 C. 11,2. D. 8,4.
Đọc tiếp
Để m gam bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp A có khối lượng 37,6 gam gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp A phản ứng hết với H2SO4 đặc, nóng, dư thu được 3,36 lít khí SO2 (đktc). Giá trị của m là
A. 56,0.
B. 28,0
C. 11,2.
D. 8,4.
Đáp án B
Xét giai đoạn A tác dụng với H2SO4 đặc, nóng, dư:
Số mol SO2 thu được là: n SO 2 = 0 , 15 mol
Qui đổi hỗn hợp A thành Fe : a mol; O : b mol
![]()
Sơ đồ phản ứng :
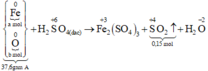
Các quá trình nhường, nhận electron:
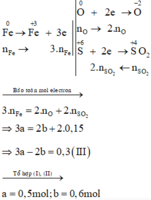
Xét giai đoạn để m gam Fe ngoài không khí:
Sơ đồ phản ứng :

Đúng 1
Bình luận (0)
Để m gam bột sắt ngoài không khí, sau một thời gian thu được 11,936 gam hỗn hợp X gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp X phản ứng hết với dung dịch H2SO4 đặc, nóng thu được 0,7616 lít khí SO2(đktc). Gía trị của m là: A. 8,736 gam B. 14,448 gam C. 5,712 gam D. 7,224 gam
Đọc tiếp
Để m gam bột sắt ngoài không khí, sau một thời gian thu được 11,936 gam hỗn hợp X gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp X phản ứng hết với dung dịch H2SO4 đặc, nóng thu được 0,7616 lít khí SO2(đktc). Gía trị của m là:
A. 8,736 gam
B. 14,448 gam
C. 5,712 gam
D. 7,224 gam
Để m gam bột sắt A ngoài không khí,sau một thời gian biến thành hỗn hợp B có khối lượng 12g gồm Fe,FeO,Fe3O4,Fe2O3.Hòa tan hoàn toàn B vào dd H2SO4 đặc,nóng dư thu đc 3,36 lít khí SO2 duy nhất(đktc).Xác định giá trị m
Coi : B gồm : Fe ( x mol) , O ( y mol)
\(m_B=56x+16y=12\left(h\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
Bảo toàn e :
\(3x=2y+0.15\cdot2\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.18,y=0.12\)
\(m_{Fe}=0.18\cdot56=10.08\left(g\right)\)
Đúng 1
Bình luận (1)
Quy đổi hỗn hợp về Fe và O.
Giả sử: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_O=y\left(mol\right)\end{matrix}\right.\)
⇒ 56x + 16y = 12 (1)
Ta có: \(n_{SO_2}=0,15\left(mol\right)\)
Theo ĐLBT mol e, có: 3x - 2y = 0,15.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,18\left(mol\right)\\y=0,12\left(mol\right)\end{matrix}\right.\)
⇒ mFe = 0,18.56 = 10,08 (g)
Bạn tham khảo nhé!
Đúng 1
Bình luận (2)
Nung nóng 12,6 gam Fe ngoài không khí sau một thời gian thu được m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 . Hỗn hợp này phản ứng hết với dung dịch H2SO4 đặc nóng (dư), thu được 4,2 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Tính m? A. 15g B. 9g C.18g D. 24g
Đọc tiếp
Nung nóng 12,6 gam Fe ngoài không khí sau một thời gian thu được m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 . Hỗn hợp này phản ứng hết với dung dịch H2SO4 đặc nóng (dư), thu được 4,2 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Tính m?
A. 15g
B. 9g
C.18g
D. 24g
Đáp án A
Ta có, nFe = 0,225 mol và nSO2 = 0,1875 mol
Quy hỗn hỗn hợp X về 2 nguyên tố Fe và O
Quá trình nhường: Fe0 → Fe+3 + 3e
Quá trình nhận e: O0 + 2e → O-2
S+6 + 2e → S+4
Áp dụng định luật bảo toàn electron ta có:
0,675 = 2x + 0,375 → x = 0,15
Mặt khác ta có: nên: m = 12,6 + 0,15.16 = 15 (gam).
Đúng 1
Bình luận (0)
Để a gam phoi bào sắt ngoài không khí một thời gian thu được b gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3. Hòa tan hết hỗn hợp X trong dung dịch H2SO4 đặc, nóng, dư thu được 5,6 lít khí SO2 (đktc) và dung dịch Y. Cho dung dịch Y phản ứng với dung dịch NaOH dư thu được kết tủa Z. Đem nung Z trong không khí đến khối lượng không đổi thu được 24 gam chất rắn. Tìm a và b. Help me, please quick!Các bạn làm ơn help me nhanh nhé
Đọc tiếp
Để a gam phoi bào sắt ngoài không khí một thời gian thu được b gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3. Hòa tan hết hỗn hợp X trong dung dịch H2SO4 đặc, nóng, dư thu được 5,6 lít khí SO2 (đktc) và dung dịch Y. Cho dung dịch Y phản ứng với dung dịch NaOH dư thu được kết tủa Z. Đem nung Z trong không khí đến khối lượng không đổi thu được 24 gam chất rắn. Tìm a và b.
Help me, please quick!
Các bạn làm ơn help me nhanh nhé
Câu 5: Cho 1,92g Cu hòa tan vừa đủ trong HNO3 thu được V lít NO (đktc). Thể tích V và khối lượng HNO3 đã phản ứng
Câu 6: Để a gam bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp A có khối lượng 75,2g gồm Fe và các oxit. Cho hỗn hợp A phản ứng hết với dd H2SO4 đậm đặc, nóng thu được 6,72 lít khí SO2. Khối lượng a là
Câu 5: Theo gt ta có: $n_{Cu}=0,03(mol)$
Bảo toàn e ta có: $n_{NO}=0,02(mol)\Rightarrow V=0,448(l)$
Dùng pt $H^+$ ta có: $n_{HNO_3}=0,08(mol)$
$\Rightarrow m_{HNO_3}=5,04(g)$
Đúng 1
Bình luận (0)
Câu 5 :
\(n_{Cu}=\dfrac{1.92}{64}=0.03\left(mol\right)\)
Bảo toàn e :
\(n_{NO}=\dfrac{2}{3}n_{Cu}=\dfrac{2}{3}\cdot0.03=0.02\left(mol\right)\)
\(V_{NO}=0.02\cdot22.4=0.448\left(l\right)\)
\(m_{HNO_3}=0.02\cdot4\cdot63=5.04\left(g\right)\)
Đúng 1
Bình luận (0)
Câu 6: Quy hỗn hợp về Fe và O với số mol lần lượt là a;b(mol)
$\Rightarrow 56a+16b=75,2$
Bảo toàn e ta có: $3a-2b=0,6$
Giải hệ ta được $a=1;b=1,2(mol)$
$\Rightarrow a=56(g)$
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Để m g bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp X gồm 4 chất rắn có khối lượng 75,2 gam. Cho hỗn hợp X phản ứng hết với dung dịch H2SO4 đặc nóng dư thấy thoát ra 6,72 lít SO2 (đktc). Tính m? A.56g B.22,4g C. 11,2g D.25,3g
Đọc tiếp
Để m g bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp X gồm 4 chất rắn có khối lượng 75,2 gam. Cho hỗn hợp X phản ứng hết với dung dịch H2SO4 đặc nóng dư thấy thoát ra 6,72 lít SO2 (đktc). Tính m?
A.56g
B.22,4g
C. 11,2g
D.25,3g
Đáp án A
Coi hỗn hợp X gồm a mol Fe và b mol O.
Quá trình nhường electron:
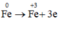
Các quá trình nhận e:
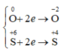
có
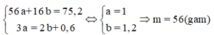
Đúng 0
Bình luận (0)
Để m g bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp X gồm 4 chất rắn có khối lượng 75,2 gam. Cho hỗn hợp X phản ứng hết với dung dịch H2SO4 đặc nóng dư thấy thoát ra 6,72 lít SO2 (đktc). Tính m? A.56g B.22,4g C. 11,2g D.25,3g
Đọc tiếp
Để m g bột sắt ngoài không khí, sau một thời gian sẽ chuyển thành hỗn hợp X gồm 4 chất rắn có khối lượng 75,2 gam. Cho hỗn hợp X phản ứng hết với dung dịch H2SO4 đặc nóng dư thấy thoát ra 6,72 lít SO2 (đktc). Tính m?
A.56g
B.22,4g
C. 11,2g
D.25,3g
Đáp án A
Coi hỗn hợp X gồm a mol Fe và b mol O.
Quá trình nhường electron:

Đúng 0
Bình luận (0)
Để 1 lượng bột sắt ngoài không khí. Sau một thời gian thu được chất rắn X gồm FeO Fe3O4 Fe2O3 và Fe có khối lượng nặng hơn lượng bột sắt ban đầu là 3,2g. Nếu cho toàn bộ X tác dụng với dung dịch H2SO4 đậm đặc, nóng, dư thu được 2,24 l khí SO2 (đktc) duy nhất thoát ra. Viết ptpư có thể xảy ra. Tính khối lượng bột sắt ban đầu
a, \(2Fe+O_2\underrightarrow{t^o}2FeO\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(4Fe+3O_2\underrightarrow{t^o}2Fe_2O_3\)
\(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(2FeO+4H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+SO_2+4H_2O\)
\(2Fe_3O_4+10H_2SO_{4\left(đ\right)}\underrightarrow{t^o}3Fe_2\left(SO_4\right)_3+SO_2+10H_2O\)
\(Fe_2O_3+3H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3H_2O\)
b, Ta có: mO2 = 3,2 (g) \(\Rightarrow n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
BT e, có: 3nFe = 4nO2 + 2nSO2
⇒ nFe = 0,2 (mol)
⇒ mFe = 0,2.56 = 11,2 (g)
Đúng 3
Bình luận (2)