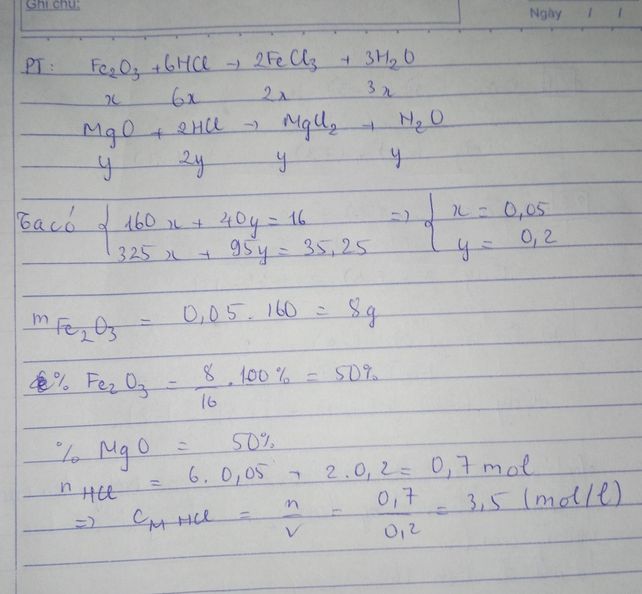Những câu hỏi liên quan
chia 78.4(g) hỗn hợp X gồm FeO và Fe2O3 thành 2 phần đều nhau:
phần 1: cho phần 1 tác dụng hết với DD axit HCL dư thu được 77.7(g) hỗn hợp muối khan
phần 2: phần 2 tác dụng vừa hết với 500ml dd Y gồm HCL và H2SO4(loãng) thu được 83.95(g) hỗn hợp muối khan
xác định khối lượng của mỗi chất trong X và tính nồng độ mol của dd Y
ai giải hộ vs
Gọi x,y tương ứng là số mol của FeO và Fe2O3
Ta có: 72x + 160y = 78,4 và 127.x/2 + 325.y/2 = 77,7. Giải hệ thu được: x = 0,2;y = 0,4 mol.
mFeO = 72.0,2 = 14,4 gam; mFe2O3 = 78,4 - 14,4 = 64 gam.
Phần 2:
Gọi a, b tương ứng là số mol của HCl và H2SO4. Hỗn hợp muối khan gồm FeCl2, FeCl3, FeSO4 và Fe2(SO4)3.
Ta có: 83,95 = mFe + mCl + mSO4 = 56(0,1 + 0,4) + 35,5a + 96b = 28 + 35,5a + 96b
Mặt khác: nCl + 2nSO4 = a + 2b = 2nFeO + 6nFe2O3 = 2.0,1 + 6.0,2 = 1,4
Giải hệ thu được: a = 0,9 và b = 0,25 mol.
Vậy: [HCl] = 0,9/0,5 = 1,8M và [H2SO4] = 0,25/0,5 = 0,5M.
Đúng 0
Bình luận (1)
Cho m gam hỗn hợp Al và Fe tác dụng vừa đủ với dd HCl 2M, thu đc dd muối A và 1,456lits H2 ở đktc. Mặt khác cho lượng hỗn hợp trên tác dụng với dd NaOH dư, thu đc 1,12 g chất rắn không tan.
a) tính khối lượng và% khối lượng mỗi chất trong hỗn hợp nói trên
b) tính khối lượng muối thu đc trong ddA
a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ 2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
Cho hỗn hợp tác dụng với NaOH, chất rắn không tan là Fe
=> mFe= 1,12 (g) \(\Rightarrow n_{Fe}=0,02\left(mol\right)\)
Ta có: \(n_{H_2\left(2\right)}=n_{Fe}=0,02\left(mol\right)\)
=> \(n_{H_2\left(1\right)}=\Sigma n_{H_2}-n_{H_2\left(2\right)}=0,065-0,02=0,045\left(mol\right)\)
\(\Rightarrow n_{Al}=\dfrac{2}{3}n_{H_2\left(1\right)}=0,03\left(mol\right)\)
\(\Rightarrow m_{Al}=0,03.27=0,81\left(g\right)\)
\(\Rightarrow\%m_{Al}=41,97\%,\%m_{Fe}=58,03\%\)
b) \(m_{FeCl_2}=0,02.127=2,54\left(g\right)\\ m_{AlCl_3}=0,03.133,5=4,005\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch HCl 10%, thu được 2,24 lít khí H 2 (ở đktc).
a/ Xác định % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b/ Tính nồng độ % các muối có trong dung dịch sau phản ứng.
Cho 6 gam hỗn hợp X gồm Al , Fe, Zn , Mg ( trong đó Fe chiếm a% về khối lượng ) tác dụng với dd HCl dư thu được 1,85925 l khí H2 (đktc) . Nếu cho 6 g hỗn hợp X tác dụng hết với Cl2 dư thì thu được 12,39 g hỗn hợp muối . Tìm a
Mọi người giúp mình với ạ:((
Coi hỗn hợp X gồm R ( có hoá trị n - a mol) và Fe (b mol)
$\Rightarrow Ra + 56b = 6$
$2R + 2nHCl \to 2RCl_n + nH_2$
$Fe + 2HCl \to FeCl_2 + H_2$
Theo PTHH : $n_{H_2} = 0,5an + b = \dfrac{1,85925}{22,4} = 0,083(mol)(1)$
$2R + nCl_2 \xrightarrow{t^o} 2RCl_n$
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$m_{Cl_2} = m_{muối} - m_X = 12,39 - 6 = 6,39(gam)$
$n_{Cl_2} = 0,5an + 1,5b = 0,09(2)$
Từ (1)(2) suy ra : an = 0,138 ; b = 0,014
$\%m_{Fe} = a\% = \dfrac{0,014.56}{6}.100\% = 13,07\%$
Đúng 2
Bình luận (1)
Cho 12,1g hỗn hợp gồm Fe và Zn tác dụng vừa đủ với 500ml HCL x(M) thu được 4,48 l khí (đktc)
a) %m mỗi khối lượng trong hợp chất ban đầu
b) tính khối lượng muối thu được
c) xác định x
a, Giả sử: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Zn}=y\left(mol\right)\end{matrix}\right.\)
⇒ 56x + 65y = 12,1 (1)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Các quá trình:
\(Fe^0\rightarrow Fe^{+2}+2e\)
x___________ 2x (mol)
\(Zn^0\rightarrow Zn^{+2}+2e\)
y____________ 2y (mol)
\(2H^++2e\rightarrow H_2^0\)
______0,4___0,2 (mol)
Theo ĐLBT mol e, có: 2x + 2y = 0,4 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1.56}{12,1}.100\%\approx46,3\%\\\%m_{Zn}\approx53,7\%\end{matrix}\right.\)
b, BTNT Fe và Zn, có: \(\left\{{}\begin{matrix}n_{FeCl_2}=n_{Fe}=0,1\left(mol\right)\\n_{ZnCl_2}=n_{Zn}=0,1\left(mol\right)\end{matrix}\right.\)
⇒ m muối = mFeCl2 + mZnCl2 = 0,1.127 + 0,1.136 = 26,3 (g)
c, BTNT H, có: \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow x=C_{M_{HCl}}=\dfrac{0,4}{0,5}=0,8\left(M\right)\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Một hỗn hợp gồm Fe2O3&MgO nặng 16g đc hòa tan hết trong dd HCl sau đó đem cô cạn dd thu đc 35,25g muối khan a. Viết PTHH xảy ra b. Tính % khối lượng mỗi muối trong hỗn hợp ban đầu c.tính Vdd HCl 20%(D=1.1g/mol)cần dùng vừa đủ để hòa tan hỗn hợp trên
Ở phần b, nếu trong hỗn hợp đầu thì phải là % khối lượng mỗi oxit chứ nhỉ? Và ở phần c phải là 1,1 g/ml chứ không phải g/mol bạn nhé!

Đúng 0
Bình luận (0)
Một hỗn hợp gồm Fe2O3&MgO nặng 16g đc hòa tan hết trong dd HCl sau đó đem cô cạn dd thu đc 35,25g muối khan a. Viết PTHH xảy ra b. Tính % khối lượng mỗi muối trong hỗn hợp ban đầu c.tính Vdd HCl 20%(D=1.1g/mol)cần dùng vừa đủ để hòa tan hỗn hợp trên
Bạn tham khảo link nhé!
một hỗn hợp gồm Fe2O3 và MgO nặng 16g được hòa tan hết trong udng dịch axit HCL sau đó đem cô cạn dung dịch thu được 35,25g muối khan a) viết các PTHH b) tính thành phần % khối lượng mỗi oxit trong hỗn hợp ban đầu >< giúp với ạ - Hoc24
Đúng 0
Bình luận (0)
Cho m gam Fe tác dụng với O2 thu được 27,2 gam hỗn hợp A gồm FeO, Fe3O4, Fe2O3, Fe dư. Cho hỗn hợp A tác dụng hết với dung dịch H2SO4 98% đun nóng thu được 6,72 lít khí SO2 (đktc) và dd B chỉ chứa muối Fe2(SO4)3 .Khối lượng m và khối lượng dung dịch H2SO4 đã dùng lần lượt là?
Cho 10g hỗn hợp gồm Na2CO3 và NaCL tác dụng với 40ml ddịch HCL tạo ra 4,48ml khí(đktc)
a.Tìm CM của dd HCL
b.Tìm khối lượng muối tạo ra sau phản ứng
c.Tìm thành phần % khối lượng từng muối trong hỗn hợp ban đầu
\(a.n_{CO_2}=\dfrac{0,00448}{22,4}=0,0002mol\\ Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\\ n_{HCl}=n_{NaCl}=0,0002.2=0,0004mol\\ C_{M_{HCl}}=\dfrac{0,0004}{0,04}=0,01M\\ b.n_{Na_2CO_3}=n_{CO_2}=0,0002mol\\ m_{NaCl}=0,0004.58,5+\left(10-0,0002.106\right)=10,022g\\ c,\%m_{Na_2CO_3}=\dfrac{0,0002.106}{10}\cdot100=0,212\%\\ \%m_{NaCl}=100-0,212=99,788\%\)
Đúng 1
Bình luận (1)