Cho phản ứng hạt nhân: C 17 37 l + X → n + A 18 37 r . Hạt nhân X là
A. H 2 4 e
B. T 1 3
C. D 1 2
D. H 1 1
Cho phản ứng hạt nhân \(Cl^{37}_{17}+X\rightarrow Ar^{^{37}_{18}}+n\) x hạt nhân nào
A. \(He^{^3_1}\)
B. \(D^{^2_1}\)
C. \(T^{^3_1}\)
D. \(H^{^1_1}\)
Bảo toàn số khối : \(37+x=1+37\Rightarrow x=1\)
Bảo toàn điện tích : \(17+y=0+18\Rightarrow y=1\)
Chọn D
Câu 24: Cho phản ứng hạt nhân \(^{37}_{17}Cl+p\rightarrow^{37}_{18}Ar+n.\) Biết khối lượng của hạt nhân \(^{37}_{17}Cl\) ; của hạt nhân \(^{37}_{18}Ar\) ; của prôtôn và của nơtron lần lượt là 36,956563 u; 36,956889 u; 1,007276 u và 1,008670 u. Lấy 1 u = 931,5 MeV/c2 . Năng lượng mà phản ứng này toả ra hoặc thu vào bằng bao nhiêu?
A. Phản ứng thu năng lượng \(\text{1,60218 MeV}\).
B. Phản ứng tỏa năng lượng \(\text{1,60218 MeV}\).
C. Phản ứng thu năng lượng \(\text{2,56349.10}^{-19}J\).
D. Phản ứng tỏa năng lượng \(\text{2,56349.10}^{-19}J.\)
Đầu tiên, chuyển đổi khối lượng từ u sang kg:
\(m_{initial}=36,956563u.\left(1,66054.10^{-27}\dfrac{kg}{u}\right)=6,1349.10^{-25}\)
\(m_{final}=36,956889u.\left(1,66054.10^{-27}\dfrac{kg}{u}\right)=6,1353.10^{-25}\)
Tiếp theo, tính năng lượng:
\(\Delta E=\left(m_{initial}-m_{final}\right).\left(3.10^8\dfrac{m}{s}\right)^2=2,56349.10^{-19}\)
Chuyển đổi năng lượng từ J sang MeV:
\(\Delta E=2,56349.10^{-19}\left(J\right).\left(6,242.10^{18}\dfrac{MeV}{J}\right)=1,60218\left(MeV\right)\)
Vậy, phản ứng này tỏa năng lượng 1,60218 MeV.
Đáp án đúng là B. Phản ứng tỏa năng lượng 1,60218 MeV.
Cho phản ứng hạt nhân sau: \(_{17}^{37}Cl +X \rightarrow _{18}^{37} Ar + n\). Biết: mCl = 36,9569 u; mn = 1,0087 u; mX = 1,0073 u; mAr = 38,6525 u. Hỏi phản ứng toả hay thu bao nhiêu năng lượng ?
A.Toả 1,58MeV.
B.Thu 1,58.103 MeV.
C.Toả 1,58 J.
D.Thu 1,58 eV.
\(m_t-m_s= m_{Cl}+ m_X -m_{Ar}-m_n = -1,697u.\)
=> \(m_t < m_s\), phản ứng là thu năng lượng.
Năng lượng thu vào là
\(E = (m_s-m_t)c^2= 1,697u.c^2 = 1,697.931 MeV= 1579,907MeV.\)
Cho phản ứng hạt nhân \(_{17}^{37}Cl +p \rightarrow _{18}^{37} Ar + n\) , khối lượng của các hạt nhân là mAr = 36,956889 u, mCl = 36,956563u, mn = 1,008670 u, mp = 1,007276 u, 1 u = 931 MeV/c2. Năng lượng mà phản ứng này toả ra hoặc thu vào là bao nhiêu ?
A.Toả ra 1,60132 MeV.
B.Thu vào 1,60132 MeV.
C.Toả ra 2,562112.10-19 J.
D.Thu vào 2,562112.10-19 J.
\(m_t = m_{Cl}+ m_p = 37,963839u.\)
\(m_s = m_{Ar}+ m_n = 37,965559u.\)
\(m_t < m_s\), phản ứng là thu năng lượng.
Năng lượng thu là
\(E = (m_s-m_t)c^2 = 1,72.10^{-3}.931 MeV/c^2.c^2= 1,60132MeV. \)
Cho phản ứng hạt nhân \(a+\overset{14}{7}N\rightarrow p+^{17}_8O\). Biết khối lượng các hạt \(m_a\) = 4,0015 u; \(m_p\) = 1,0073 u; \(m_n\) = 1,0087 u; \(m_o\) = 16,9947 u. Cho 1u = 931 MeV/c2 . Phản ứng này ( ghi cách giải)
A. 7 hạt nơtron và 3 hạt proton.
B. 4 hạt nơtron và 3 hạt proton.
C. 3 hạt nơtron và 4 hạt proton.
D. 3 hạt nơtron và 7 hạt proton.
Cho phản ứng hạt nhân: He 2 4 + 7 14 N → N + 1 1 H . Hạt nhân X có cấu tạo gồm
A. 8 prôtôn và 17 nơtron.
B. 8 nơtron và 17 prôtôn.
C. 8 prôtôn và 9 nơtron
D. 8 nơtron và 9 prôtôn.
Cho phản ứng hạt nhân: T 1 3 + X → H 2 4 e + n + 17 , 6 M e V
Hạt nhân X và năng lượng tỏa ra khi tổng hợp được 1 gam Heli theo phản ứng trên. Cho số Avôgađrô N A = 6 , 02 . 10 23 (nguyên tử/mol).
A. X = D 1 2 , E = 26 , 488 . 10 23 ( M e V )
B. X = T 1 3 , E = 2 , 65 . 10 24 ( M e V )
C. X = T 1 3 , E = 25 , 23 . 10 23 ( M e V )
D. X = D 1 2 , E = 6 , 5 . 10 24 ( M e V )
Đáp án A
Phương trình phản ứng hạt nhân:
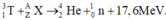
• Định luật bảo toàn số khối:
3 + A = 4 + 1 → A = 2
• Định luật bảo toàn điện tích:
1 + Z = 2 + 0 → Z = 1
• X là 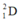
• Năng lượng tỏa ra khi tổng hợp được 1 gam Heli theo phản ứng trên là:
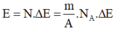
= 1/4. 6,02. 10 23 .17,6
= 26,488. 10 23 (MeV)
Cho phản ứng hạt nhân X Z A + Be 4 9 → C 6 12 + n . Trong phản ứng này X là
A. electron.
B. pôzitron.
C. proton.
D. hạt α
Cho nguyên tố A có tổng số hạt là 58 số hạt mang điện nhiều hơn số hạt không mang điện là 18
a) tính số hạt proton electron Nơtron và tên nguyên tố A
b) viết phản ứng và sơ đồ trao đổi electron của A và clo
a) Ta có
2pA+nA=58
2pA-nA=18
\(\rightarrow\)pA=eA=19 nA=20
\(\rightarrow\) A là Kali
b)
K\(\rightarrow\)K+ +1e
Cl2 +2e\(\rightarrow\)2Cl-