Một lượng khí khối lượng 15 kg chứa 5,64. 10 26 phân tử. Phân tử khí này gồm các nguyên tử hiđrô và cacbon. Hãy xác định khối lượng của nguyên cacbon và hiđrô trong khí này. Biết 1 mol khí có N A = 6,02. 10 23 phân tử.

Những câu hỏi liên quan
Một lượng khí có khối lượng là 30kg và chứa (11,(28.10^(26)) ) phân tử. Phân tử khí này gồm các nguyên tử hiđro và cacbon. Biết 1 mol khí có
N
A
6,02.10
23
phân tử. Khí này là A.
C
H
3
B.
C
2
H
2
C.
C
2
H
4
D....
Đọc tiếp
Một lượng khí có khối lượng là 30kg và chứa (11,(28.10^(26)) ) phân tử. Phân tử khí này gồm các nguyên tử hiđro và cacbon. Biết 1 mol khí có N A = 6,02.10 23 phân tử. Khí này là
A. C H 3
B. C 2 H 2
C. C 2 H 4
D. C H 4
Đáp án: D
Gọi M - khối lượng mol phân tử của chất khí
Ta có, số mol khí bằng: n = m M = N N A
Với N = 11,28.10 26 N A = 6,02.10 23 m = 30 k g = 30.10 3 g
Ta suy ra: M = m N A N = 30.10 3 .6,02.10 23 11,28.10 26 = 16 g / m o l
Mặt khác, phân tử khí này gồm các nguyên tử hiđro và cacbon
Khí CH4 có khối lượng mol phân tử là M = 12 + 4 = 16 g / m o l
=> Khí đã cho là C H 4
Đúng 0
Bình luận (0)
Một phân tử ADN có khối lượng 9.105 đvC (đơn vị Cacbon), có hiệu số % giữa nuclêôtit loại Ađênin (A) với một loại nuclêôtit không bổ sung với nó là 10%. Hãy xác định: chiều dài, số lượng từng loại nuclêôtit và số liên kết hiđrô của phân tử ADN này.
\(N=\dfrac{M}{300}=\dfrac{9.10^5}{300}=3000\left(Nu\right)\\L=\dfrac{N}{2}.3,4=\dfrac{3000}{2}.3,4=5100\left(A^o\right)\\ Ta.có:\left\{{}\begin{matrix}\%A+\%G=50\%N=1500\left(Nu\right)\\\%A-\%G=10\%N=300\left(Nu\right)\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}A=T=900\left(Nu\right)\\G=X=600\left(Nu\right)\end{matrix}\right.\\ H=2A+3G=2.900+3.600=3600\left(liên.kết\right)\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn cacbon bằng một lượng khí oxi dư, người ta thu được hỗn hợp khí gồm có khí cacbonic
C
O
2
và khí oxi
O
2
dư.Hãy xác định phần trăm theo khối lượng và thành phần phần trăm theo thể tích của khí oxi trong mỗi hỗn hợp sau: 0,3.
10
23
phân tử
C
O
2
và...
Đọc tiếp
Đốt cháy hoàn toàn cacbon bằng một lượng khí oxi dư, người ta thu được hỗn hợp khí gồm có khí cacbonic C O 2 và khí oxi O 2 dư.
Hãy xác định phần trăm theo khối lượng và thành phần phần trăm theo thể tích của khí oxi trong mỗi hỗn hợp sau: 0,3. 10 23 phân tử C O 2 và 0,9. 10 23 phân tử O 2 .
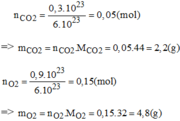
Thành phần % theo khối lượng:
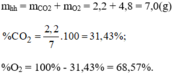
Thành phần % về thể tích:
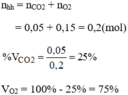
Đúng 1
Bình luận (0)
Mỗi phân tử nước gồm 1 nguyên tử ôxi và 2 nguyên tử hiđrô. Khối lượng của nguyên tử hiđrô là
1
,
67
.
10
-
27
kg , khối lượng của nguyên tử ôxi là
26
,
56
.
10
-...
Đọc tiếp
Mỗi phân tử nước gồm 1 nguyên tử ôxi và 2 nguyên tử hiđrô. Khối lượng của nguyên tử hiđrô là 1 , 67 . 10 - 27 kg , khối lượng của nguyên tử ôxi là 26 , 56 . 10 - 27 kg. Số phân tử nước trong 1 gam nước là
A. 2 , 5 . 10 24 phân tử.
B. 3 , 34 . 10 22 phân tử.
C. 1 , 8 . 10 20 phân tử.
D. 4 . 10 21 phân tử.
B
Khối lượng 1 phân tử nước m 0 = 2 . 1 , 67 . 10 - 27 + 26 , 56 . 10 - 27 = 29 , 9 . 10 - 27 kg
Số phân tử nước trong 1 gam nước
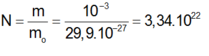
Đúng 0
Bình luận (0)
Khí A có tỉ khối đối với H2 là 22.
a) Tính khối lượng mol khí A.
b) Một phân tử khí A gồm 1 nguyên tử nguyên tố X liên kết với 2 nguyên tử oxygen. Xác định công thức hoá học của phân tử khí A.
a) Khí A có tỉ khối đối với H2 là: \(d_{A/H_2}=22\) nên khối lượng mol khí A bằng MA = 22.2 = 44 g/mol
b) Ta có công thức của khí A là XO2
Do MA = 44 nên MX + 2. 16 = 44 \(\rightarrow\) MX = 12
Vậy X là Carbon(C)
Công thức hoá học của phân tử khí A là CO2
Đúng 0
Bình luận (0)
Khí A có tỉ khối đối với H2 là 22.
a) Tính khối lượng mol khí A.
b) Một phân tử khí A gồm 1 nguyên tử nguyên tố X liên kết với 2 nguyên tử oxygen. Xác định công thức hoá học của phân tử khí A.
\(a)Có:d_{A/H_2}=\dfrac{M_A}{2}=22\\ \Rightarrow M_A=44g/mol\\ b)CTPT\left(A\right):XO_2\\ M_A=M_X+16.2=44\\ \Rightarrow M_X=12g/mol\\ \Rightarrow X.là.carbon\\ \Rightarrow CTPT\left(A\right):CO_2\)
Đúng 2
Bình luận (0)
a, \(M_A=22.2=44\left(g/mol\right)\)
b, A có CTHH dạng XO2
⇒ MX + 16.2 = 44 ⇒ MX = 12 (g/mol)
→ X là C.
Vậy: CTHH của A là CO2
Đúng 0
Bình luận (0)
a) Khí A có tỉ khối đối với \(H_2\) là: \(d_{A/H_2}=22\) nên khối lượng mol khí \(A\) bằng:
\(M_A=22.2=44\left(g/mol\right)\)
b) Ta có công thức của khí \(A\) là \(XO_2\)
Do \(M_A=44\) nên \(M_X+2.16=44\rightarrow M_X=12\)
Công thức hoá học của phân tử khí A là \(CO_2\)
Đúng 0
Bình luận (0)
Trộn 2 lít CH4 với 1 lít CxHy được hỗn hợp khí A có tỉ khối so với heli là 7,5 ( các khí đo ở cùng đk t°,p).Xác định công thức phân tử của CxHy trong phân tử CxHy nguyên tố cacbon chiếm 82,76% về khối lượng
Xem chi tiết
\(\%C = \dfrac{12x}{12x + y}.100\% = 82,76\%\\ \Rightarrow 2,5x = y(1)\)
Ta có :
\(M_A = \dfrac{2.16 + 1.(12x + y)}{2 + 1} = 7,5.4\\ \Rightarrow 12x + y = 58(2)\)
Từ (1)(2) suy ra x = 4 ; y = 10
Vậy CTPT của hợp chất cần tìm : C4H10
Đúng 0
Bình luận (2)
Xác định công thức phân tử của các chất x, y, z biết thành phần % khối lượng như sau:
a) Chất x chứa 85, 71 % cacbon và 14, 29% Hiđro. Phân tử khối của x bằng phân tử khối của Nitơ
b) Chất y chứa 80 % cacbon và 20 % Hiđro, cho phân tử khối của y = 30
c) Chất z chứa 40 % cacbon, 6,67 % Hiđro và 53,33 % Oxi. Biết phân tử z chỉ có 2 nguyên tử Oxi
a) Gọi CTHH của chất x là CxHy
Ta có : 85,71% cacbon và 14,29 % hiđro.
Ta có : x : y = \(\frac{\%C}{M_C}:\frac{\%H}{M_H}=\frac{85,71}{12}:\frac{14,29}{1}=\frac{1}{2}\)
Vậy CTHH của CxHy là CH2
Đúng 0
Bình luận (0)
b) Gọi CTHH của chất y là CxHy
Ta có : 80% cacbon và 20% hiđro.
Ta có : \(\frac{12x}{80}=\frac{y}{20}=\frac{30}{80+20}=\frac{30}{100}=0,3\)
\(\Rightarrow\frac{12x}{80}=0,3\Rightarrow x=2\)
\(\Rightarrow\frac{y}{20}=0,3\Rightarrow y=6\)
Vậy CTHH của CxHy là C2H6
Đúng 0
Bình luận (0)
Gọi CTHH của chất x là CxHy
Ta có : 85,71% cacbon; 14,29% hiđro và phân tử khối của x bằng phân tử khối của nitơ
Ta có : \(x:y=\frac{\%C}{M_C}:\frac{\%H}{M_H}=\frac{85,71}{12}:\frac{14,29}{1}=\frac{2}{4}\)
Vậy CTHH của CxHy là C2H4
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Một hỗn hợp X gồm ankan A và anken B có cùng số nguyên tử C và đều ở thể khí ở đktc. Cho hỗn hợp X đi qua nước brom dư thì thể tích khí Y còn lại bằng nửa thể tích X, còn khối lượng Y bằng 15/29 khối lượng của X. Xác định công thức phân tử của A,B và thành phần phần trăm theo thể tích của A và B trong hỗn hợp.

























