Nguyên tử nguyên tố X (Z=12) có điện hoá trị trong hợp chất với nguyên tử các nguyên tố nhóm VIIA là
A. 2+
B. 2 -
C. 7+
D. 7 -
Điện hoá trị của các nguyên tố nhóm VIA, VIIA trong các hợp chất với các nguyên tố nhóm IA lần lượt bằng
A. 2,3. B. 2, 1
C.1,2. D. 1,3.
Xác định điện hóa trị của các nguyên tố nhóm VIA, VIIA trong các hợp chất với các nguyên tố nhóm IA.
Điện hóa trị của các nguyên tố nhóm VIA, VIIA, trong các hợp chất vời nguyên tố nhóm IA là:
Các nguyên tố kim loại thuộc nhóm IA có số electron ở lớp ngoài cùng là 1, có thể nhường 1 electron này nên có điện hóa trị 1+.
Các nguyên tố phi kim thuộc nhóm VIA, VIIA có 6,7 electron ở lớp ngoài cùng, có thể nhận thêm 2 hay 1 electron vào lớp ngoài cùng nên có điện hóa trị 2- hay 1-.
Một hợp chất có phân tử gồm 1 nguyên tử của nguyên tố X liên kết với 1 nguyên tử oxi và có phân tử khối là 40 đvC. X là nguyên tố nào? Lập công thức hoá học của hợp chất tạo bởi X và nhóm (NO3)biết nhóm (NO3)có hoá trị 1, X chỉ có 1 loại hoá trị
Ta có :
$M_{hợp\ chất} = X + 16 = 40 \Rightarrow X = 24$
Vậy X là nguyên tố Magie
CTHH với nhóm $NO_3$ là : $Mg(NO_3)_2
Các nguyên tố thuộc nhóm VIIA gồm những nguyên tố nào ?
Nguyên tử của các nguyên tố thuộc nhóm này có bao nhiêu electron hoá trị ?
Khi hai nguyên tử của cùng một nguyên tố thuộc nhóm này liên kết với nhau tạo thành phân tử thì mỗi nguyên tử phải góp bao nhiêu electron, tạo thành mấy liên kết, tại sao ? Cho thí dụ.
Các nguyên tố thuộc nhóm VIIA gồm các nguyên tố : flo (F), clo (Cl), brom (Br), iot (I), atatin (At). Nguyên tử của chúng có 7 electron hoá trị.
Khi hai nguyên tử của cùng một nguyên tố thuộc nhóm này liên kết với nhau tạo thành phân tử thì mỗi nguyên tử góp 1 electron, tạo thành một cặp electron chung tức là một liên kết, vì mỗi nguyên tử chỉ thiếu electron để đạt được cấu hình 8 electron vững bền (giống như của khí hiếm đứng sau nó).
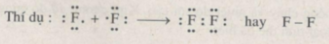
Xác định điện hóa trị của các nguyên tố nhóm VIA, VIIA trong hợp chất với các nguyên tố nhóm IA.
Các nguyên tố kim loại thuộc nhóm IA có 1 electron lớp ngoài cùng, nên nhường 1 electronnên có điện hóa trị 1+
Các nguyên tố phi kim thuộc nhóm VIA, VIIA có 6 hoặc 7 electron ở lớp ngoài cùng, có thể nhận 2 hay 1 electron nên có điện hóa trị 2- hay 1-.
Điện hóa trị của các nguyên tố F, I (thuộc nhóm VIIA) trong các hợp chất với các nguyên tố nhóm IA bằng
Điện hóa trị của các nguyên tố nhóm VIA, VIIA trong các hợp chất với các nguyên tố nhóm IA là:
Các nguyên tố kim loại thuộc nhóm IA có số electron ở lớp ngoài cùng là 1, có thể nhường 1 electron này nên điện hóa trị là +1
Các nguyên tố phi kim thuộc nhóm VIA, VIIA có 6, 7 electron ở lớp ngoài cùng, có thể nhận thêm 2 hay 1 electron vào lớp ngoài cùng nên có điện hóa trị 2- hoặc 1-
Xác định điện hóa trị của các nguyên tố nhóm VIA,VIIA trong hợp chất với các nguyên tố nhóm IA.
Điện hóa trị của các nguyên tố nhóm VIA, VIIA trong các hợp chất với các nguyên tố nhóm IA là:
Các nguyên tố kim loại thuộc nhóm IA có số electron ở lớp ngoài cùng là 1, có thể nhường 1 electron này nên điện hóa trị là +1
Các nguyên tố phi kim thuộc nhóm VIA, VIIA có 6, 7 electron ở lớp ngoài cùng, có thể nhận thêm 2 hay 1 electron vào lớp ngoài cùng nên có điện hóa trị 2- hoặc 1-
Xác định hoá trị các nguyên tố và nhóm nguyên tử trong các hợp chất sau :
a) Hoá trị của Fe trong Fe2O3 ; FeO ; Fe3O4.
b) Hoá trị của S trong H2S ; SO2 ; SO3.
c) Hoá trị của nhóm nguyên tử (SO3) trong H2SO3.
a. Fe2O3 (III); FeO (I); Fe3O4 (II, III)
b. H2S (II); SO2 (IV); SO3 (VI)
c. SO3 (II)
d. PO4 (III)
a.
Lần lượt là: Fe(III), Fe(II), Fe(II, III)
b.
Lần lượt là: S(II), S(IV), S(VI)
c.
Lần lượt là: SO3(II)
Câu 11: Nguyên tố A có số hiệu nguyên tử là 8, chu kì 2, nhóm VI trong bảng tuần hoàn các nguyên tố hoá học. Hãy cho biết:
- Cấu tạo nguyên tử của A
- Tính chất hoá học đặc trưng của A
- So sánh tính chất hoá học của A với các nguyên tố lân cận ?
a) A có 8 electron, 8 proton
b) Câu hình e: 1s22s22p4
=> A có 6e lớp ngoài cùng
=> A có tính chất của phi kim
c)
- A là O (oxi)
- Trong chu kì 2, 2 nguyên tố lân cận với O là N, F
Trong 1 chu kì, theo chiều tăng điện tích hạt nhân, tính phi kim tăng dần
=> N < O < F (Xét theo tính phi kim)
- Trong nhóm VIA, nguyên tố lân cận với O là S
Trong 1 nhóm A, theo chiều tăng điện tích hạt nhân, tính phi kim giảm dần
=> O > S (Xét theo tính phi kim)
a: Do A có Z=8 nên A là oxi
Cấu tạo nguyên tử là \(O=O\)
b: Tính chất hóa học đặc trưng là tính phi kim, có tính oxi hóa mạnh
Số hiệu là 8
Cấu tạo nguyên tử: O
Tính chất hóa học đặc trưng là kim loại hoạt động mạnh
Tính chất hóa học của A mạnh hơn C,N nhưng yếu hơn F