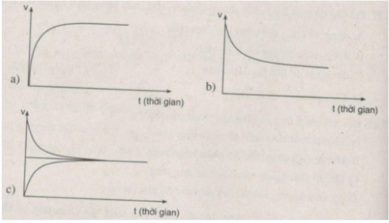
Đồ thị nào sau đây biểu diễn sự biến đổi tốc độ phản ứng thuận theo thời gian ? Sự biến đổi tốc độ phản ứng nghịch theo thời gian ? Trạng thái cân bằng hoá học ?
Cho các phát biểu sau:
1, Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau.
2, Chất xúc tác làm tăng tốc độ phản ứng thuận và nghịch.
3, Tại thời điểm cân bằng trong hệ vẫn luôn có mặt các chất phản ứng và các sản phẩm.
4, Khi phản ứng đạt trạng thái cân bằng hoá học, nồng độ các chất vẫn có sự thay đổi.
5, Khi phản ứng đạt trạng thái cân thuận nghịch bằng hoá học, phản ứng dừng lại.
Các phát biểu sai là
A. 2, 3.
B. 4, 5.
C. 3, 4.
D. 3, 5.
Đáp án B
(1) Đúng
(2) Đúng, xúc tác làm tăng tốc độ cả phản ứng thuận và nghịch
(3) Đúng do phản ứng thuận nghịch phản ứng xảy ra k hoàn toàn, tại thời điểm cân bằng luôn có mặt chất pu và chất sp
(4) Sai do nồng độ các chất k đổi thì phản ứng tiến tới trạng thái cân bằng
(5) Sai do cân bằng là cân bằng động nên phản ứng vẫn xảy ra, tốc độ phản ứng thuân và nghịch là bằng nhau
Chọn B
Cho các phát biểu sau:
1, Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau trong cùng điều kiện.
2, Chất xúc tác làm tăng tốc độ phản ứng thuận và nghịch.
3, Tại thời điểm cân bằng trong hệ vẫn luôn có mặt các chất phản ứng và các sản phẩm.
4, Khi phản ứng đạt trạng thái cân bằng hoá học, nồng độ các chất vẫn có sự thay đổi.
5, Khi phản ứng đạt trạng thái cân thuận nghịch bằng hoá học, phản ứng dừng lại.
Số phát biểu sai là
A. 2
B. 3
C. 1
D. 4
Đáp án A
1, đúng
2, đúng
3, đúng
4, sai, nồng độ các chất sẽ không thay đổi ở trạng thái cân bằng (ở đây giả thiết các điều kiện khác không đổi)
5, sai, ở trạng thái cân bằng, phản ứng thuận và nghịch vẫn tiếp tục, nhưng nồng độ các chất đều không đổi.
=> Đáp án A
Cho hai đồ thị (a) và (b) dưới đây. Mỗi đồ thị biểu diễn sự thay đổi tốc độ phản ứng thuận và tốc độ phản ứng nghịch theo thời gian.
Hãy cho biết đồ thị nào thể hiện đúng Ví dụ 2. Đường màu xanh trong đồ thị đó biểu diễn tốc độ phản ứng thuận hay tốc độ phản ứng nghịch?
Sau một khoảng thời gian, màu tím của hỗn hợp khí không thay đổi, chứng tỏ nồng độ I2 không thay đổi. Nghĩa là sau một thời gian, lượng I2 sinh ra từ phản ứng nghịch và lượng I2 mất đi từ phản ứng thuận bằng nhau. Hay tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. Do đó đồ thị (a) thể hiện đúng Ví dụ 2.
Đường màu xanh biểu diễn tốc độ phản ứng nghịch. Ban đầu phản ứng, chưa sinh ra HI nên tốc độ phản ứng nghịch bằng 0. Sau một thời gian, lượng HI sinh ra càng nhiều, tốc độ phản ứng nghịch tăng. Sau đó, lượng HI sinh ra từ phản ứng thuận bằng lượng HI mất đi từ phản ứng nghịch, tức tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch nên đường đồ thị màu xanh trùng với đường đồ thị màu đỏ.
Cho các phát biểu sau:
1) Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau.
2) Chất xúc tác làm tăng tốc độ phản ứng thuận và nghịch.
3) Tại thời điểm cân bằng trong hệ vẫn luôn có mặt các chất phản ứng và các sản phẩm.
4) Khi phản ứng đạt trạng thái cân bằng hóa học, nồng độ các chất vẫn có sự thay đổi.
5) Khi phản ứng đạt trạng thái cân bằng hóa học thuận nghịch, phản ứng dừng lại.
Các phát biểu sai là
A. 2, 3
B. 4, 5
C. 3, 4
D. 3, 5
(1) Đúng
(2) Đúng, xúc tác làm tăng tốc độ cả phản ứng thuận và nghịch
(3) Đúng do phản ứng thuận nghịch phản ứng xảy ra không hoàn toàn, tại thời điểm cân bằng luôn có mặt chất phản ứng và chất sản phẩm
(4) Sai do nồng độ các chất không đổi thì phản ứng tiến tới trạng thái cân bằng
(5) Sai do cân bằng là cân bằng động nên phản ứng vẫn xảy ra, tốc độ phản ứng thuận và nghịch là bằng nhau
Chọn B
Cho phát biểu sau:
1) Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau trong cùng điều kiện.
2) Chất xúc tác làm tăng tốc độ phản ứng thuận và nghịch.
3) Tại thời điểm cân bằng trong hệ vẫn luôn có mặt các chất phản ứng và các sản phẩm.
4) Khi phản ứng đạt trạng thái cân bằng hóa học, nồng độ các chất vẫn có sự thay đổi.
5) Khi phản ứng đạt trạng thái cân thuận nghịch bằng hòa học, phản ứng dừng lại
Số phát biểu sai là
A. 2
B. 3
C. 1
D. 4
1) đúng
2) đúng
3) đúng
4) sai, nồng độ các chất sẽ không thay đổi ở trạng thái cân bằng (ở đây giả thiết các điều kiện khác không đổi)
5) sai, ở trạng thái cân bằng, phản ứng thuận và nghịch tiếp tục, nhưng nồng độ các chất đều không đổi
Đáp án A
Câu hỏi: Xét phản ứng thuận nghịch: H2(g) + I2(g) ⇌ 2HI(g).
Số liệu về sự thay đổi số mol các chất trong bình phản ứng ở thí nghiệm 1 được trình bày trong Bảng 1.1 dưới đây:
a) Vẽ đồ thị biểu diễn sự thay đổi số mol các chất theo thời gian.
b) Từ đồ thị, nhận xét về sự thay đổi số mol của các chất theo thời gian.
c) Viết biểu thức định luật tác dụng khối lượng đối với phản ứng thuận và phản ứng nghịch, từ đó dự đoán sự thay đổi tốc độ của mỗi phản ứng theo thời gian (biết các phản ứng này đều là phản ứng đơn giản).
d) Bắt đầu từ thời điểm nào thì số mol các chất trong hệ phản ứng không thay đổi nữa?
b) Từ đồ thị ta thấy: Lúc đầu số mol sản phẩm bằng 0, theo thời gian, số mol chất tham gia (hydrogen, iodine) giảm dần, số mol chất sản phẩm (hydrogen iodide) tăng dần, đến khi số mol của các chất hydrogen, iodine, hydrogen iodide không thay đổi nữa.
c) Biểu thức định luật tác dụng khối lượng:
- Đối với phản ứng thuận:
vthuận = \({\rm{k}}{\rm{.}}{{\rm{C}}_{{{\rm{H}}_{\rm{2}}}}}{\rm{.}}{{\rm{C}}_{{{\rm{I}}_{\rm{2}}}}}\)
- Đối với phản ứng nghịch:
vnghịch = \({\rm{k'}}{\rm{.C}}_{{\rm{HI}}}^2\)
Dự đoán:
- Ban đầu tốc độ phản ứng thuận giảm dần, sau một thời gian tốc độ phản ứng thuận không thay đổi theo thời gian.
- Ban đầu tốc độ phản ứng nghịch tăng dần, sau một thời gian tốc độ phản ứng nghịch không thay đổi theo thời gian.
d) Tại thời điểm phản ứng thuận nghịch đạt tới trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch thì số mol các chất trong hệ phản ứng không thay đổi nữa.
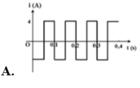
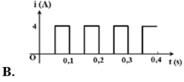
Từ thông Ф qua một khung dây biến đổi theo thời gian được diễn tả như trên đồ thị. Biết khung dây có điện trở 0,5 Ω, đồ thị nào sau đây biểu diễn đúng sự biến đổi của dòng điện cảm ứng trong khung theo thời gian ?
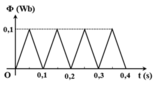
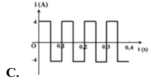
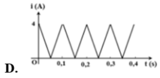
Suất điện động cảm ứng trong một mạch điện biến đổi theo thời gian được diễn tả bằng đồ thị trên hình vẽ. Chọn chiều dương của dòng điện thuận hiều với pháp tuyến mạch điện. Biết từ thông cực tiểu bằng 0
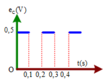
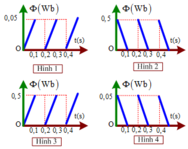
Đồ thị biểu diễn sự biến đổi của dòng điện cảm ứng trong khung theo thời gian là hình:
A. (1)
B. (2)
C. (3)
D. (4)
Từ thông Φ qua một khung dây biến đổi theo thời gian được diễn tả bằng đồ thị trên hình vẽ. Chọn chiều dương của dòng điện thuận chiều với pháp tuyến khung dây có điện trở 0,5Ω
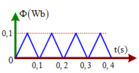
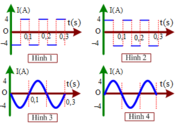
Đồ thị biểu diễn sự biến đổi của dòng điện cảm ứng trong khung theo thời gian là hình
A. (1)
B. (2)
C. (3)
D. (4)