Nhiệt độ sôi của H2O cao hơn so với H2S là do :
A. Liên kết hidro của H2O bền hơn
B. Độ dài liên kết trong H2O ngắn hơn trong H2S.
C. Sự phân cực liên kết trong H2O lớn hơn.
D. A và C
Dãy gồm các chất trong phân tử chỉ có liên kết cộng hoá trị phân cực là
A. O 2 , H 2 O , NH 3 B. H 2 O , HF , H 2 S
C. HCl , O 2 , H 2 S D. HF , Cl 2 , H 2 O
So sánh độ phân cực của các liên kết trong các phân tử sau: NH3, H2S, H2O, H2Te, CsCl, CaS, BaF2
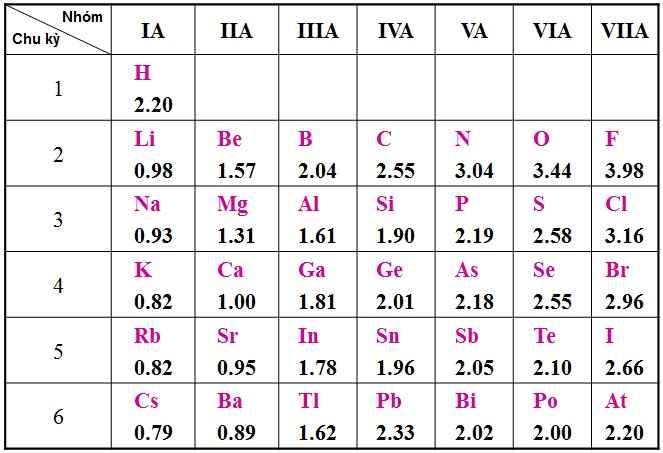
Hiệu độ âm cực càng lớn thì độ phân cực càng mạnh.
---
Áp dụng bài tập:
Hiệu độ âm điện của NH3: 3,04 - 2,2= 0,84
Hiệu độ âm điện của H2S: 2,58 - 2,2= 0,38
Hiệu độ âm điện của H2O: 3,44 - 2,2= 1,24
Hiệu độ âm điện của H2Te: 2,2 - 2,1= 0,1
Hiệu độ âm điện của CsCl: 3,16 - 0,79= 2,37
Hiệu độ âm điện của CaS: 2,58 - 1= 1,58
Hiệu độ âm điện của BaF2: 2,58 - 0,89= 1,69
Ta thấy: 2,37 > 1,69 > 1,58 > 1,24 > 0,84 > 0,38 > 0,1
=> Thứ tự độ phân cực: CsCl > BaF2 > CaS > H2O > NH3 > H2S > H2Te
Cho độ âm điện Cs: 0,79; Ba: 0,89; H: 2,2; Cl: 3,16; S: 2,58; N: 3,04; O: 3,44 để xét sự phân cực của liên kết trong ptử các chất sau: NH3, H2S, H2O, CsCl. Chất nào trong các chất trên có liên kết ion?
A. NH3
B. H2O.
C. CsCl.
D. H2S
Chọn đáp án và giải thích cách làm giúp em ạ !!! Em cảm ơn
Cho 12,8g dd rượu A( dung môi H2O) có nồng độ 71,875% tác dụng với H2O dư thu dc 5,6 lít khí( đktc). Tìm công thức cấu tạo của A biết tỉ khối hơi của A so với NO2 bằng 2 và rượu bền khi nhóm OH liên kết với cacbon no và mỗi nguyên tử C chỉ liên kết với 1 nhóm OH
m rượu = 12,8.71,875% = 9,2(gam)
m H2O = 12,8 - 9,2 = 3,6(gam) => n H2O = 3,6/18 = 0,2(mol)
n H2 = 5,6/22,4 = 0,25(mol)
M A = 46.2 = 92 => n A = 9,2/92 = 0,1(mol)
$2OH + 2Na \to ONa + H_2$
$2Na + 2H_2O \to 2NaOH + H_2$
Theo PTHH :
n OH + n H2O = 2n H2 = 0,5
=> n OH = 0,5 - 0,2 = 0,3(mol)
Suy ra
Số nhóm OH trong rượu là n OH / n A = 0,3/0,1 = 3
CTHH của A : R(OH)3
M A = R + 17.3 = 92 => R = 41(-C3H5)
Vật CTCT của A là : HO-CH2-CH(OH)-CH2OH
Cặp electron liên kết bị lệch nhiều hơn trong phân tử NH3 hay trong phân tử H2O? Vì sao?
- Trong phân tử NH3: độ âm điện của H và N lần lượt là 2,2 và 3,0
⟹ Nguyên tử N hút electron liên kết mạnh hơn H gấp 3,0 : 2,2 = 1,36 lần.
- Trong phân tử H2O: độ âm điện của H và O lần lượt là 2,2 và 3,4
⟹ Nguyên tử O hút electron liên kết mạnh hơn H gấp 3,4 : 2,2 = 1,54 lần.
Vậy cặp electron liên kết trong phân tử H2O bị lệch nhiều hơn trong phân tử H2O.
Cho các phát biểu sau:
(1) Tinh thể I2 là tinh thể phân tử.
(2) Tinh thể H2O là tinh thể phân tử.
(3) Liên kết giữa các nguyên tử trong tinh thể nguyên tử là liên kết yếu.
(4) Liên kết giữa các phân tử trong tinh thể phân tử là liên kết mạnh.
(5) Tinh thể ion có nhiệt độ nóng chảy cao, khó bay hơi, khá rắn vì liên kết cộng hóa trị trong các hợp chất ion rất bền vững.
(6) Kim cương là một dạng thù hình của cacbon.
Số phát biểu đúng là:
A. 5
B. 3
C. 4
D. 6
Chọn đáp án B
(1) Tinh thể I2 là tinh thể phân tử. Đúng theo SGK lớp 10.
(2) Tinh thể H2O là tinh thể phân tử. Đúng theo SGK lớp 10.
(3) Sai. Là liên kết mạnh
(4) Sai. Là liên kết yếu
(6) Kim cương là một dạng thù hình của cacbon. Đúng theo SGK lớp 10.
Cho các phát biểu sau:
(1) Tinh thể I2 là tinh thể phân tử.
(2) Tinh thể H2O là tinh thể phân tử.
(3) Liên kết giữa các nguyên tử trong tinh thể nguyên tử là liên kết yếu.
(4) Liên kết giữa các phân tử trong tinh thể phân tử là liên kết mạnh.
(5) Tinh thể ion có nhiệt độ nóng chảy cao, khó bay hơi, khá rắn vì liên kết cộng hóa trị trong các hợp chất ion rất bền vững.
(6) Kim cương là một dạng thù hình của cacbon.
Số phát biểu đúng là:
A. 5
B. 3
C. 4
D. 6
Chọn đáp án B
(1) Tinh thể I2 là tinh thể phân tử. Đúng theo SGK lớp 10.
(2) Tinh thể H2O là tinh thể phân tử. Đúng theo SGK lớp 10.
(3) Sai. Là liên kết mạnh
(4) Sai. Là liên kết yếu
(6) Kim cương là một dạng thù hình của cacbon. Đúng theo SGK lớp 10.
Liên kết của chất nào sau đây không phải là liên kết cộng hóa trị. Giải thích?
Cl2 ; H2S ; H2O ; NaCl ; O2 ; MgO ; HCl ; CO2 ; NH3 ; Al2O3
Các bạn làm nhanh giúp mình nhé, 1/11 là mình thi rồi, cảm ơn mọi người nhiều!!!
Câu 59: Cho các chất sau: Cl2, HCl, O2, H2O, NaCl, CaO, Na2O, NH4Cl. Số chất mà trong phân tử chứa liên kết ion, liên kết cộng hóa trị phân cực, liên kết cộng hóa trị không phân cực lần lượt là
A. 4, 2, 2. B. 3, 3, 2. C. 4, 1, 2. D. 4, 3, 2.
Câu 60: X là nguyên tố mà nguyên tử có 20 proton, còn Y là nguyên tố mà nguyên tử có 9 proton. Công thức phân tử và liên kết trong hợp chất tạo thành giữa X và Y là
A. X2Y, liên kết cộng hóa trị B. XY2 liên kết cộng hóa trị
C. XY2, liên kết ion D. X2Y3 liên kết ion
Câu 61: A và B là 2 nguyên tố ở cùng 1 nhóm và thuộc 2 chu kỳ liên tiếp trong bảng tuần hoàn. Biết tổng số hạt proton trong nguyên tử của nguyên tố A và B là 32. Số hiệu nguyên tử của A và B là
A. 12 và 20 B. 15 và 17 C. 7 và 25 D. 11 và 21
Câu 62: Hai nguyên tố X, Y nằm ở 2 ô liên tiếp trong 1 chu kỳ, có tổng số proton là 29 (ZX > ZY). Nhận xét nào sau đây đúng?
A. X, Y đều là kim loại. B. X có 8 electron p.
C. Y nằm ở chu kỳ 2. D. X có công thức oxit cao nhất là X2O5.
Câu 63: Nguyên tố R thuộc có thể tạo ra oxit RO3 tương ứng với với hóa trị cao nhất. Hợp chất của nó với hiđro có thành phần khối lượng là 5,88 % hiđro, còn lại là R. Nguyên tố R là
A. S. B. C. C. N. D. Al.
Câu 64: Công thức phân tử của hợp chất khí tạo bởi nguyên tố R và hiđro là RH3. Trong oxit mà R có hoá trị cao nhất thì oxi chiếm 74,07% về khối lượng. Nguyên tố R là
A. S. B. As. C. N. D. P.