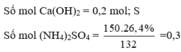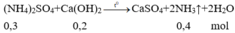Cho 14,8 gam C a O H 2 vào 150 gam dung dịch N H 4 2 S O 4 26,4% rồi đun nóng nhẹ thu được V lít (đktc) khí X (giả sử toàn bộ khí sinh ra thoát ra khí dung dịch). Để đốt cháy hết V lít khí X trên cần vừa đủ lượng O 2 sinh ra khi nung m gam K C l O 3 (có xúc tác). Giá trị của m là
A. 24,5.
B. 49.
C. 36,75.
D. 12,25.