Cho hỗn hợp Fe, Mg vào dung dịch AgNO 3 và Cu ( NO 3 ) 2 thì thu được dung dịch A và một kim loại. Kim loại thu được sau phản ứng là
A. Cu.
B. Ag.
C. Fe.
D. Mg.
Hòa tan hoàn toàn 12,4g hỗn hợp hai kim loại Fe và Cu vào dung dịch HNO3 loãng thu được dung dịch chứa hai muối Fe(NO3)3 và Cu(NO3) đồng thời có 3,36 lít khí NO bay ra. Khối lượng hỗn hợp muối có trong dung dịch là?
nNO=3,36/22,4=0,15
Theo định luật bảo toàn mol e
\(Fe^0\rightarrow Fe^{+3}+3e
\)
\(Cu^0\rightarrow Cu^{+2}+2e\)
\(N^{+5}+3e\rightarrow N^{+2}\)
=> 3a+2b=3.0,15=0,45
Ta có hpt:\(\begin{cases}3a+2b=0,45\\56a+64b=12,4\end{cases}\Leftrightarrow\begin{cases}a=0,05\left(mol\right)\\b=0,15\left(mol\right)\end{cases}}\)
\(n_{Fe\left(NO3\right)3}=n_{Fe}=0,05,n_{Cu\left(NO3\right)2}=n_{Cu_{ }_{ }}=0,15\)Từ đó tính m nha bạn
Cho hỗn hợp X gồm Mg và Fe vào 200 ml dung dịch chứa Cu(NO3)2 1M và AgNO3 0,5M đến khi kết thúc các phản ứng được 24,16 gam hỗn hợp kim loại và dung dịch Y. Cho Y tác dụng với HCl dư được 0,224 lít NO (sản phẩm khử duy nhất, đktc). Phần trăm khối lượng của Fe trong hỗn hợp X có giá trị gần nhất với:
A. 28
B. 31
C. 30
D. 29
Đáp án C
Ta có: nCu(NO3)2 = 0 , 2 m o l ; n A g N O 3 = 0 , 1 m o l
Ta có: 0,2.64 + 0,1.108 = 23,6 < 24,16 chứng tỏ Cu(NO3)2 và AgNO3 hết, còn kim loại dư.
Dung dịch Y tác dụng với HCl dư thu được 0,01 mol NO chứng tỏ Y chứa 0,03 mol Fe(NO3)2.
Bảo toàn điện tích: n Mg (NO 3 ) 2 = 0 , 2 . 2 + 0 , 1 - 0 , 03 . 2 2 = 0 , 22 m o l
Mặt khác do Y chứa Fe(NO3)2 nên kim loại chỉ có Fe dư và khối lượng Fe dư là 0,56 gam.
→ m x = 0 , 56 + 0 , 03 . 56 + 0 , 22 . 24 = 7 , 52 → %Fe = 29,79%
Cho hỗn hợp X gồm Mg và Fe vào 200 ml dung dịch chứa Cu(NO3)2 1M và AgNO3 0,5M đến khi kết thúc các phản ứng được 24,16 gam hỗn hợp kim loại và dung dịch Y. Cho Y tác dụng với HCl dư được 0,224 lít NO (sản phẩm khử duy nhất, đktc). Phần trăm khối lượng của Fe trong hỗn hợp X có giá trị gần nhất với:
A. 28
B. 31
C. 30
D. 29
Đáp án C
Ta có: n C u ( N O 3 ) 2 = 0 , 2 m o l , n A g N O 3 = 0 , 1 m o l
Ta có: 0,2.64 + 0,1.108 = 23,6 < 24,16 chứng tỏ Cu(NO3)2 và AgNO3 hết, còn kim loại dư.
Dung dịch Y tác dụng với HCl dư thu được 0,01 mol NO chứng tỏ Y chứa 0,03 mol Fe(NO3)2.
Bảo toàn điện tích:
![]()
Mặt khác do Y chứa Fe(NO3)2 nên kim loại chỉ có Fe dư và khối lượng Fe dư là 0,56 gam.
→ m X = 0,56 + 0,03.56 + 0,22.24 = 7,52 => %Fe = 29,97%
Hòa tan hoàn toàn hỗn hợp X gồm Cu, Fe, Mg vào dung dịch HNO3 dư, sau phản ứng thu được dung dịch Y chỉ chứa muối của kim loại và hỗn hợp khí gồm 0,01 mol N2, 0,02 mol NO. Số mol HNO3 đã phản ứng là
A. 0,10
B. 0,12
C. 0,16
D. 0,20
Ở ví dụ 4, ta đã giải quyết câu hỏi này bằng bảo toàn nguyên tố, giờ với phương trình liên hệ mol H+ và sản phẩm khử, ta có ngay: nH+ = 12nN2 + 4nNO = 12.0,01 + 4.0,02 =0,2 mol
Chọn đáp án D
Hòa tan hoàn toàn hỗn hợp X gồm Cu, Fe, Mg vào dung dịch HNO3 dư, sau phản ứng thu được dung dịch Y chỉ chứa muối của kim loại và hỗn hợp khí gồm 0,01 1mol N2, 0,02 mol NO. Số mol HNO3 đã phản ứng là
A. 0,10
B. 0,12
C. 0,16
D. 0,20
Cho 0,3 mol Mg vào 100 ml dung dịch hỗn hợp chứa Fe(NO3)2 2M và Cu(NO3)2 1M , sau khi phản ứng xảy ra hoàn toàn , khối lượng kim loại thu được là :
Cho 2,22 gam hỗn hợp Al, Fe vào bình chứa dung dịch hỗn hợp Fe(NO3)3 và Cu(NO3)2. Sau một thời gian cho tiếp dung dịch HNO3 dư vào bình, thấy thoát ra 1,12 lít khí NO (đktc) (sản phẩm khử duy nhất). Phần trăm khối lượng của Al trong hỗn hợp là
A. 24,32%
B. 12,20%
C. 36,50%
D. 48,65%
Chọn đáp án A
Vì HNO3 dư nên cuối cùng Al, Fe hay các ion kim loại trong dung dịch đều đạt hóa trị tối đa
Þ Xem như không có phản ứng giữa Al, Fe và Fe(NO3)3 và Cu(NO3)2 ban đầu mà phản ứng thẳng với HNO3
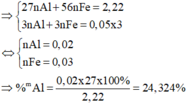
Hòa tan hoàn toàn 15,2 gam hỗn hợp gồm Fe và Cu trong dung dịch HNO3, thu được dung dịch X và 4,48 lút khí NO. Cho 3,96 gam kim loại Mg vào X đến khi phản ứng xảy ra hoàn toàn, thu được 224ml khí NO và m gam chất rắn không tan. biết NO là sản phẩm khử duy nhất của N+5. Gía trị cảu m là
A. 6,4 B.12,8 C.9,6 D.4,8
Hòa tan hoàn toàn 15,2 gam hỗn hợp gồm Fe và Cu trong dung dịch HNO3, thu được dung dịch X và 4,48 lút khí NO. Cho 3,96 gam kim loại Mg vào X đến khi phản ứng xảy ra hoàn toàn, thu được 224ml khí NO và m gam chất rắn không tan. biết NO là sản phẩm khử duy nhất của N+5. Gía trị cảu m là
A. 6,4 B.12,8 C.9,6 D.4,8
Hòa tan hoàn toàn m gam hỗn hợp X chứa Cu, Mg, Fe3O4 và Fe(NO3)2 trong dung dịch chứa 0,61 mol HCl thu được dung dịch Y chứa (m + 16,195) gam hỗn hợp muối và 1,904 lít hỗn hợp khí Z (đktc) gồm H2 và NO với tổng khối lượng là 1,57 gam. Cho NaOH dư vào Y thấy xuất hiện 24,44 gam kết tủa. Phần trăm khối lượng của Cu có trong X là
A. 15,92%
B. 22,18%
C. 26,32%
D. 25,75%
Hòa tan hoàn toàn m gam hỗn hợp X chứa Cu, Mg, Fe3O4 và Fe(NO3)2 trong dung dịch chứa 0,61 mol HCl thu được dung dịch Y chứa (m + 16,195) gam hỗn hợp muối và 1,904 lít hỗn hợp khí Z (đktc) gồm H2 và NO với tổng khối lượng là 1,57 gam. Cho NaOH dư vào Y thấy xuất hiện 24,44 gam kết tủa. Phần trăm khối lượng của Cu có trong X là:
A. 15,92%
B. 22,18%
C. 26,32%
D. 25,75%
Đáp án D
có : 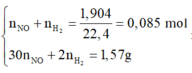
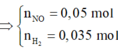
![]()
![]()
![]()
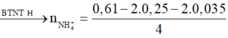
= 0,01 mol
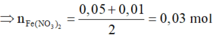
Có khí H2 thoát ra => Chứng tỏ muối sắt tạo thành là Fe2+.
Đặt số mol của Cu, Mg, Fe3O4 lần lượt là a, b, c.
![]()
![]()
![]() Kết tủa
Kết tủa
![]()
![]() (2)
(2)
![]()
![]()
![]()
=> c = 0,03 , thay vào (1), (2) suy ra
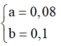
=> % m C u =
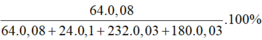
= 25,75 %