Trộn 200ml dung dịch HCl 0,1M và H2SO4 0,05M với 300ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và 500ml dung dịch có pH =13. Vậy a và m có giá trị lần lượt là:
A. 0,15M ; 2,33g
B. 0,15M ; 10,485g
C. 0,3M ; 4,66g
D. 0,2M ; 6,99g
Trộn 200ml dung dịch Ba(OH)2 aM với 300ml dung dịch H2SO4 có pH=1 thu được m gam kết tủa và 500ml dung dịch có pH=2. Giá trị của a và m lần lượt là:
A. 0,125M và 5,825 gam
B. 0,1 M và 4,66 gam
C. 0,0625M và 2,9125 gam
D. 0,125M và 3,495 gam
Đáp án C
nBa(OH)2 = 0,2.a mol; nOH-= 0,4a mol
dung dịch H2SO4 có pH = 1 nên [H+] = 10-1 M
→nH+ = [H+].Vdd = 0,3.10-1 = 0,03 mol, nSO4(2-) = 0,015 mol
H2SO4→ 2H++ SO42-
0,03 →0,015 mol
Ba(OH)2→ Ba2++ 2OH-
0,2a→ 0,2a 0,4a
H+ + OH- → H2O
0,4a 0,4a
Dung dịch sau phản ứng có pH = 2 nên axit dư
nH+ dư = 0,03-0,4a
[H+] dư = nH+ dư/ Vdd = (0,03-0,4a)/0,5 = 10-2 suy ra a = 0,0625 M
Ba2++ SO42- → BaSO4
0,0125 0,015 0,0125 mol
mBaSO4 = 2,9125 gam
Trộn 200 ml dung dịch chứa hỗn hợp HCl 0,1M và H2SO4 0,05M với 300 ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và dung dịch có pH = 13. Giá trị của a và m là
A. 0,3 và 104,85.
B. 0,3 và 23,3.
C. 0,15 và 104,85.
D. 0,15 và 23,3.
Trộn 200 ml dung dịch chứa hỗn hợp HCl 0,1M và H2SO4 0,05M với 300 ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và dung dịch có pH = 13. Giá trị của a và m là
A. 0,3 và 10,485
B. 0,3 và 2,33
C. 0,15 và 10,485
D. 0,15 và 2,33
Trộn 200ml dung dịch hỗn hợp HCl 0,1M và H2SO4 0,05M với 300ml dung dịch Ba(OH)2 a M thu được m (g) kết tủa và 500ml dung dịch ph=13. Tìm a , m .
a=0,12
m=2,33g
Trộn 200 ml dung dịch gồm HCl 0,1M và H 2 SO 4 0,15M với 300 ml dung dịch Ba OH 2 nồng độ aM, thu được m gam kết tủa và 500 ml dung dịch có pH = 1. Giá trị của a và m lần lượt là
A. 0,15 và 2,330
B. 0,10 và 6,990.
C.0,10 và 4,660
D. 0.05 và 3,495
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH = x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
![]()
![]()
![]()
![]()
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH = x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
A. 2 , 5 . 10 - 3 M ; 13
B. 2 , 5 . 10 - 3 M ; 12
C. 0 , 05 M ; 13
D. 0 , 05 M ; 12
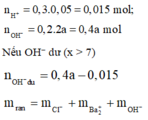
→ 0,015.35,5 + 0,2a.137 + 17(0,4a - 0,015) = 1,9875
→ a = 0,05 M

Đáp án D
Trộn 200 ml dung dịch gồm HCl 0,1M và H2SO4 0,15M với 300 ml dung dịch Ba(OH)2 nồng độ 0,05M, thu được m gam kết tủa và dung dịch (X).
a/ Tính m và nồng độ các ion có trong dung dịch (X)
b/ pH của dung dịch (X)
a, \(n_{HCl}=0,2.0,1=0,02\left(mol\right)=n_{H^+}=n_{Cl^-}\)
\(n_{H_2SO_4}=0,2.0,15=0,03\left(mol\right)=n_{SO_4^{2-}}\) \(\Rightarrow n_{H^+}=2n_{H_2SO_4}=0,06\left(mol\right)\)
\(\Rightarrow\Sigma n_{H^+}=0,02+0,06=0,08\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,3.0,05=0,015\left(mol\right)=n_{Ba^{2+}}\)
\(\Rightarrow n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,03\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,03___0,03 (mol) ⇒ nH+ dư = 0,05 (mol)
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
0,015___0,015______0,015 (mol) ⇒ nSO42- dư = 0,015 (mol)
⇒ m = mBaSO4 = 0,015.233 = 3,495 (g)
\(\left[Cl^-\right]=\dfrac{0,02}{0,2+0,3}=0,04\left(M\right)\)
\(\left[H^+\right]=\dfrac{0,05}{0,2+0,3}=0,1\left(M\right)\)
\(\left[SO_4^{2-}\right]=\dfrac{0,015}{0,2+0,3}=0,03\left(M\right)\)
b, pH = -log[H+] = 1
Trộn 200 ml dung dịch gồm HCl 0,1M và H2SO4 0,05 M với 300 ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và 500 ml dung dịch có pH=13. Các giá trị a, m tương ứng là
A. 0,25 và 4,66
B. 0,15 và 2,33
C. 0,15 và 3,495
D. 0,2 và 2,33