100ml dung dịch X chứa K 2 C O 3 0,1M và K 2 S O 4 0,1M tác dụng hết với dung dịch B a C l 2 dư. Khối lượng kết tủa thu được là
A. 4,3 gam.
B. 2,93 gam.
C. 3,4 gam.
D. 2,39 gam.
100ml dung dịch X chứa N a 2 S O 4 0,1M và N a 2 C O 3 0,1M tác dụng hết với dung dịch B a N O 3 2 dư. Khối lượng kết tủa thu được là
A. 4,3 gam.
B. 2,93 gam.
C. 3,4 gam.
D. 2,39 gam.
Cho 100ml dung dịch X chứa KOH 0,13M và Ba ( OH ) 2 0,1M tác dụng với 200ml dung dịch H 2 SO 4 x mol/lít. Sau khi phản ứng kết thúc thu được dung dịch có pH = 2. Giá trị của x là
A. 0,03
B. 0,09
C. 0,06
D. 0,045
Chọn B
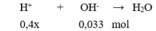
Dung dịch sau phản ứng có pH = 2 < 7 nên dung dịch sau phản ứng có H + dư
→ 0,4x – 0,033 = 10 - 2 .0,3 → x = 0,09
Trộn 100ml dung dịch chứa H2SO4 0,1M và HNO3 0,3M với 100ml dung dịch chứa Ba(OH)2 0,3M và KOH 0,1M thu được dung dịch X và kết tủa Y. Cho quỳ tím vào dung dịch Y, hiện tượng gì xảy ra ?
A. tím chuyển sang đỏ
B. quỳ tím chuyển sang xanh
C. quỳ tím không chuyển màu
D. quỳ tím mất màu
Đáp án B
nH+ = 0,05 mol; nOH- = 0,07 mol
H+ + OH- → H2O
Ta thấy H+ hết, OH- dư nên nhúng quỳ tím vào Y thì quỳ tím chuyển thành màu xanh.
Cho 100ml dung dịch Ba(O H ) 2 0,1M vào 100ml dung dịch HCl 0,1M. Dung dịch thu được sau phản ứng
A. Làm quỳ tím hoá xanh
B. Làm quỳ tím hoá đỏ
C. Phản ứng được với magie giải phóng khí hiđro
D. Không làm đổi màu quỳ tím
Chọn A
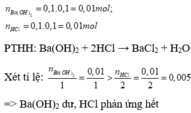
=> Dung dịch sau phản ứng thu được gồm BaC l 2 và Ba(O H ) 2 dư
Vì BaC l 2 là muối, không làm đổi màu quỳ, còn Ba(O H ) 2 là bazơ làm quỳ hóa xanh
=> dung dịch thu được sau phản ứng làm quỳ hóa xanh
Thêm m gam K vào 200ml dung dịch chứa Ba(OH)2 0,1M và NaOH 0,1M thu được dung dịch X. Cho từ từ dung dịch X vào 200ml dung dịch Al2 (SO4)3 0,1M thu được kết tủa Y. Để thu được kết tủa Y lớn nhất thì giá trị của m là:
A. 1,17 gam
B. 2,34 gam
C. 3,12 gam
D. 1,59 gam
Bài tập về kim loại kiềm và nhôm tác dụng với H2O
Đem hòa tan x gam Na vào 200ml dung dịch Ba(OH)2 0,1M thu được dung dịch A. Cho từ từ dung dịch A vào 100ml dung dịch Al2(SO4)3 0,1M thu được y gam kết tủa. Tìm trih số của x để y có trị số lớn nhất.
Na + H2O → NaOH + 1/2 H2
x/23..........................x/23........x/46 (mol)
nBa(OH)2 = 0,02 (mol)
Dung dịch A có x/23 (mol) NaOH và 0,02 (mol) Ba(OH)2
nAl2(SO4)3 = \(\frac{100\cdot0,1}{1000}\) = 0,01 (mol)
y max => baso pư vừa đủ
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4
(mol) x/23..............x/ 138.................x/69........................3x/23
3 Ba(OH)2 + Al2(SO4)3 → 3BaSO4↓ + 2Al(OH)3↓
(mol) 0,02....................0,02/3
Theo đề ta có : \(\frac{x}{138}\) + \(\frac{0,02}{3}\) = 0,01
<=> x = 0,52 (gam)
Vậy để y có trị số lớn nhất thì x = 0,52 gam
Đặt :
nNa= a mol
Na + H2O --> NaOH + 1/2H2
a_____________a
dd A: a mol NaOH , 0.02 mol Ba(OH)2
nAl2(SO4)3 = 0.1*0.1 = 0.01 mol
Cho A vào dd Al2(SO4)3 :
6NaOH + Al2(SO4)3 --> 3Na2SO4 + 2Al(OH)3
a__________a/6
3Ba(OH)2 + Al2(SO4)3 --> 3BaSO4 + 2Al(OH)3
0.02_________1/150
Để lượng kết tủa lớn nhất thì : OH- và Al2(SO4)3 đủ
<=> nAl2(SO4)3 = 0.01
<=> a/6 + 1/150 = 0.01
<=> a = 0.02
mNa = 0.02 * 23 = 0.46 g
Cù Văn Thái
Trộn 3 dung dịch axit thành dung dịch X gồm có H2SO4 0,1M, HCl 0,2M và HNO3 0,3M. Cho 300 ml dung dịch X tác dụng với V lít dung dịch Y chứa NaOH 0,2 M và Ba(OH)2 0,1M được dung dịch Z có pH=1. Giá trị của V là
A. 0,24 lít.
B. 0,36 lít.
C. 0,16 lít.
D. 0,32 lít.
Đáp án : B
Trong X :
n H + = 2 n H 2 S O 4 + n H C l + n H N O 3 = 0,21 mol
Trong Y : nOH = nNaOH + 2 n B a O H 2 = 0,4V mol
Vì dung dịch sau trộn có pH = 1 < 7 => axit dư
=> n H + Z = (V + 0,3).10-pH= 0,21 – 0,4V
=> V = 0,36 lit
Dung dịch X thu được khi trộn một thể tích dung dịch H2SO4 0,1M với một thể tích dung dịch HCl 0,2M . Dung dịch Y chứa NaOH 0,2M và Ba(OH)2 0,1M . Đổ 100ml dung dịch X vào 100ml dung dịch Y , khuấy đều để phản ứng xảy ra hoàn toàn , thu được 200ml dung dịch X có pH=a và m gam kết tủa Y . Giá trị của a và m là ?
Ta có: \(\Sigma n_{H^+}=0,1.0,1.2+0,1.0,2=0,04\left(mol\right)\)
\(\Sigma n_{OH^-}=0,1.0,2+0,1.0,1.2=0,04\left(mol\right)\)
PT ion: \(H^++OH^-\rightarrow H_2O\)
_____0,04____0,04_________ (mol)
⇒ H+ pư vừa đủ với OH-
⇒ a = pH = 7
Ta có: \(n_{SO_4^{2-}}=0,1.0,1=0,01\left(mol\right)\)
\(n_{Ba^{2+}}=0,1.0,1=0,01\left(mol\right)\)
PT ion: \(SO_4^{2-}+Ba^{2+}\rightarrow BaSO_{4\downarrow}\)
_______0,01___0,01______0,01___ (mol)
\(\Rightarrow m=m_{BaSO_4}=0,01.233=2,33\left(g\right)\)
Bạn tham khảo nhé!
cho ai chưa biết thì nH+ tùy theo lượng H trong acid. Ví dụ như ở bài này là nH+(H2SO4)= 2nH2SO4 và NH+(HCl)= nHCl
Vậy nên bài bạn Lê Ng Hải Anh làm rất đúng, không sai chỗ nào để tôi có thể sửa =))
Trộn 100ml dung dịch X chứa Ba(OH)2 0,2M và NaOOH 0,1M với 100ml dung dịch Y chứa H2SO4 và HCl 0,1M thu được dung dịch Z và 2,33 g kết tủa . Tìm pH của dung dịch Z ?