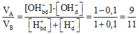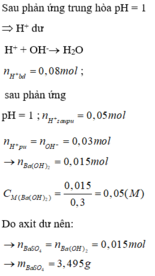Trộn ba dung dịch HCl 0,15M ; HNO3 0,3M và H2SO4 0, 3M với thể tích bằng nhau thu được dung dịch X. Cho 100 ml dung dịch X vào dung dịch chứa 0,005 mol KOH và 0,005 mol Ba(AlO2)2 . Khối lượng kết tủa thu được là :
A. 2,33g
B. 3,11g
C. 0,78g
D. 1,425g