Cho cấu hình electro LNC các ion sau, hãy viết cấu hình electro của các nguyên tử tương ứng
X-: 3p6, X3+: 2p6
Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng.
a) Viết cấu hình electron của Na+ và Cl-.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
a) Na (Z = 11) 1s22s22p63s1 ⇒ Na+: 1s22s22p6.
Cl (Z = 17) 1s22s22p63s23p5 ⇒ Cl-: 1s22s22p63s23p6.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp p của Cl. AO đó là AO chứa 1 electron.
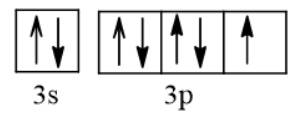
Câu 6: Ở trạng thái cơ bản, nguyên tử X có 7 electron thuộc các phân lớp s. Hãy cho biết cấu hình đúng của X là:
A. 1s2 2s2 2p6 3s2 3p6 4s1 B. 1s2 2s2 2p6 3s2 3p6 3d5 4s1
C. 1s2 2s2 2p6 3s2 3p6 3d10 4s1 D. Cả 3 trường hợp đều thỏa mãn.
7 Cấu hình eletron lớp ngoài cùng của ion âm là 3s2 3p6 thì cấu hình electron của nguyên tư tạo ra ion đó có thể là
(I) 1s2 2s2 2p6 3s2 (IV) 1s2 2s2 2p6 3s2 3p4
(II) 1s2 2s2 2p6 3s2 3p5 (V) 1s2 2s2 2p5
(III) 1s2 2s2 2p6 3s1 (VI) 1s2 2s2 2p4
7 Cấu hình eletron lớp ngoài cùng của ion âm là 3s2 3p6 thì cấu hình electron của nguyên tư tạo ra ion đó có thể là
(I) 1s2 2s2 2p6 3s2 (IV) 1s2 2s2 2p6 3s2 3p4
(II) 1s2 2s2 2p6 3s2 3p5 (V) 1s2 2s2 2p5
(III) 1s2 2s2 2p6 3s1 (VI) 1s2 2s2 2p4
Cho nguyên tố B(Z = 23)
1s2 2s2 2p6 3s2 3p6 4s2 3d3
Viết cấu hình ion có thể có của B?
Z = 23 suy ra : B là Vanadi
Cấu hình e của V+5 : 1s22s22p63s23p6
Cấu hình e của V+3 :1s22s22p63s23p64s2
Cho cấu hình electron của các hạt vi mô sau :
X : [Ne] 3s2 3p1
Y2+ : 1s2 2s2 2p6.
Z : [Ar] 3d5 4s2
M2- : 1s2 2s2 2p6 3s2 3p6
T2+ : 1s2 2s2 2p6 3s2 3p6.
Trong các nguyên tố X, Y, Z, M, T những nguyên tố nào thuộc chu kì 3?
A. X, Y, M
B. X, Y, M, T
C. X, M, T
D. X, T
Đáp án : A
Cấu hình e của nguyên tố nào có 2 ngoài cùng thuộc lớp nào thì nó sẽ thuộc chu kì đó.
X: [Ne]3s23p1 M: [Ar] 1s22s22p63s23p4
Y: 1s22s22p63s2
Cho cấu hình electron của các nguyên tố sau
X: 1s2 2s2 2p6 3s2 ; Y: 1s2 2s2 2p6 3s2 3p1 ; Z: 1s2 2s2 2p6 3s2 3p6 3d3 4s2 ; T: 1s2 2s2 2p4.
Dãy các cấu hình electron của các nguyên tố kim loại là
A
Y, Z, T.
B
X, Y, T.
C
X, Y, Z.
D
X, Z, T.
Hãy viết cấu hình electron nguyên tử của các nguyên tố sau đây : O, F, Ne. Từ các cấu hình đó hãy cho biết các nguyên tử O, F, mỗi nguyên tử nhận thêm mấy electron thì có cấu hình electron giống như của khí hiếm Ne đứng sau.
Hãy cho biết tại sao các nguyên tử phi kim lại có khuynh hướng nhận thêm electron để trở thành các ion âm ?
O: 1 s 2 2 s 2 2 p 4
F: 1 s 2 2 s 2 2 p 5
Ne: 1 s 2 2 s 2 2 p 6
Từ các cấu hình trên ta dễ dàng thấy rằng nếu nguyên tử F nhận thêm 1e để trở thành ion F - , nguyên tử O nhận thêm 2e để trở thành ion O 2 - thì các ion được hình thành có cấu hình electron giống cấu hình electron của khí hiếm Ne với 8 electron ở lớp ngoài cùng.
Như ta đã biết, cấu hình electron của các khí hiếm với 8 electron (đối với He là 2 electron) ở lớp ngoài cùng là một cấu hình electron vững bền (năng lượng thấp). Vì vậy, các nguyên tử phi kim có khuynh hướng nhận electron để có cấu hình electron vững bền của khí hiếm đứng sau.
Viết cấu hình electron nguyên tử của các nguyên tố sau đây : Al, Mg, Na, Ne. Từ các cấu hình đó hãy cho biết các nguyên tử Al, Mg, Na, mỗi nguyên tử nhường mấy electron thì có cấu hình electron giống như của khí hiếm Ne.
Hãy cho biết tại sao các nguyên tử kim loại lại có khuynh hướng nhường electron để trở thành các ion dương ?
Cấu hình electron của Al, Mg, Na, Ne :
Al 1 s 2 2 s 2 2 p 6 3 s 2 3 p 1 |
Mg 1 s 2 2 s 2 2 p 6 3 s 2 |
Na 1 s 2 2 s 2 2 p 6 3 s 1 |
Ne 1 s 2 2 s 2 2 p 6 |
Từ các cấu hình trên ta dễ dàng thấy rằng nếu :
nguyên tử Na nhường le để trở thành ion Na + ;
nguyên tử Mg nhường 2e để trở thành ion Mg 2 + ;
nguyên tử Al nhường 3e để trở thành ion Al 3 + ,
thì các ion được hình thành có cấu hình electron giống cấu hình electron của khí hiếm Ne với 8 electron ở lớp ngoài cùng.
Ta đã biết cấu hình electron của các khí hiếm với 8 electron (đối với He là electron) ở lớp ngoài cùng là một cấu hình electron vững bền. Vì vậy, các nguyên tử kim loại có khuynh hướng dễ nhường electron để có cấu hình electron vững bền của khí hiếm đứng trước.
Nguyên tử flo có số hiệu nguyên tử là 9. Cấu hình electron của anion F- là ?
A.1s2 2s2 2p5 .
B.1s2 2s2 2p6 3s2 3p5 .
C.1s2 2s2 2p6 3s2 3p6 .
D.1s2 2s2 2p6
Cho nguyên tử các nguyên tố sau: K (Z = 19), Ca (Z = 20), Al (Z = 13), F (Z =9), Br (Z = 35). Viết cấu hình e và quá trình hình thành ion tương ứng của các nguyên tử trên.