Trong một cái cốc đựng muối cacbonat của kim loại hóa trị I. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hóa trị I là:
A. Li
B. Na
C. K
D. Ag
Trong một cái cốc đựng một muối cacbonat của kim I loại hoá trị. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hoá trị I là
A. Li.
B. Na.
C. K.
D. Ag.
Đáp án B
Giả sử

khối lượng dung dịch sau phản ứng:
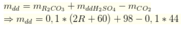
![]()
![]()
Một cốc đựng dung dịch muối cacbonat của một kim loại hóa trị II .Rót từ từ dung dịch H2SO4 có nồng độ 20% vào cốc cho đến khi khí thoát ra vừa hết thì thu được dung dịch muối có nồng độ 24,91%.Hãy xác định muối cacbonat của kim loại gì ?
gọi dd muối CO3 là ACO3
ACO3 +H2SO4 -->ASO4 +CO2+H2O
giả sử có 1 mol ACO3
=>mACO3= MA +60(g)
theo PTHH : nH2SO4=nACO3=1(mol)
=>mdd H2SO4=1.98.100/20=490(g)
nASO4=nACO3=1(mol)
=>mASO4=MA +96(g)
nCO2=nACO3=1(mol)
=>mCO2=44(g)
=>\(\dfrac{MA+96}{MA+60+490-44}\).100=24,91
giải ra ta được MA=40(g/mol0
=>ACO3:CaCO3
ta có pthh: ACO3 +H2SO4--ASO4+H2O+CO2
(A+60)g......98g.......(A+96)g..........44g
mdd H2SO4=(98.100):20=490g
mdd muối sau phản ứng=(A+60)+490-44= (A+506)g
theo đê bài ta có:C% ASO4=(A+96).100:A+506
suy ra A=40 CÓ: CTHH :CACO3
mdd muối sau phản ứng=(A+60)+490-44: (A+506)g=24,91%
hòa tan một lượng muối cacbonat của một loại hóa trị III bằng dung dịch H2SO4 16%. Sau khi khí không thoát ra nữa, được dung dịch chứa 20% mưới sunfat tan. Xác định tên kim loại hóa trị III.
Gọi CT của muối cacbonat là MCO3.
Giả sử có 100g H2SO4,nH2SO4=0,15mol
MCO3+H2SO4=MSO4+CO2+H2O
0,15 0,15 0,15 0,15
(H2SO4 hết vì sau pư còn chất rắn ko tan là MCO3)
mddsaupư=mddH2SO4bđ+mMCO3-mCO2=100+0,1... (gam)
C%MSO4=mMSO4x100/mdd
suy ra:0,15(M+96)/(102,4+0,15M)=0,17 suy ra M=24 nên M là Mg
Bài 15 trong cốc đựng A2CO3. Thêm từ từu H2SO4 10% vào cốc cho tới khi khí vừa thoát ra hết thu đc dd muối nồng độ 13,63%. XĐ tên kim loại A
Bài 15
Đặt \(n_{A_2CO_3}=1\left(mol\right)\Rightarrow m_{A_2CO_3}=2A+60\left(g\right)\)
\(A_2CO_3\left(1mol\right)+H_2SO_4\left(1mol\right)\rightarrow A_2SO_4\left(1mol\right)+CO_2\left(1mol\right)+H_2O\)
Theo PTHH: \(n_{H_2SO_4}=1\left(mol\right)\Rightarrow m_{H_2SO_4}=98\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{98.100}{10}=980\left(g\right)\)
\(n_{CO_2}=1\left(mol\right)\Rightarrow m_{CO_2}=44\left(g\right)\)
\(n_{A_2SO_4}=1\left(mol\right)\Rightarrow m_{A_2SO_4}=\left(2A+96\right)\left(g\right)\)
\(m_{ddA_2SO_4}=m_{A_2CO_3}+m_{ddH_2SO_4}-m_{CO_2}\)
\(=2A+60+980-44=2A+996\left(g\right)\)
Theo đề, dd muối thu được có nồng độ 13,63%
\(\Leftrightarrow13,63=\dfrac{\left(2A+96\right).100}{2A+996}\)
\(\Rightarrow A=23\left(Na\right)\)
hoà tan một muối cacbonat của kim loại R ( chưa biết hoá trị ) trong một lượng vừa đủ dung dịch H2SO4 12,25% thu được dung dịch muối sunfat của kim loại R có nồng độ 17,431%. Xác định kim loại R
tham khảo
Coi mdd H2SO4=100(gam)mdd H2SO4=100(gam)
nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)
Sau phản ứng ,
mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)
Hoà tan một lượng muối cacbonat của kim loại hoá trị III bằng dung dịch H2SO4 nồng
độ 16%. Sau khi khí không thoát ra nữa, thu được dung dịch chứa 20% muối sunfat tan. Xác
định kim loại đó.
GIÚP MÌNH VỚI Ạ!!!!!!!!!!!!!!!!!!!!!!!!!!
\(Đặt.muối:A_2\left(CO_3\right)_3\\ n_{A_2\left(CO_3\right)_3}=a\left(mol\right)\Rightarrow n_{H_2SO_4}=3a\left(mol\right)\\ m_{ddH_2SO_4}=\dfrac{3a.98.100}{16}=1837,5a\left(g\right)\\ A_2\left(CO_3\right)_3+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3CO_2+3H_2O\\ m_{ddsau}=\left(M_A.2+180\right).a+1837,5a-44a.3=1885,5a+2M_A.a\left(g\right)\\ Vì:C\%_{dd.muối.sunfat}=16\%\\ \Leftrightarrow\dfrac{\left(2M_A+288\right).a}{\left(1885,5+2M_A\right).a}.100\%=16\%\\ \Leftrightarrow M_A=8,14\left(loại\right)\)
Không có kim loại thỏa
Cho 9.85g muối cacbonat của kim loại hóa trị II TÁC DỤNG HẾT VS DUNG DỊCH H2SO4 LOÃNG, DƯ THU ĐƯỢC 11,65G MUỐI SUNFAT. HÃY TÌM CTPT của muối cacbonat hóa trị II.
Giúp mk : Trong 1 chiếc cốc đựng muối cacbonat trung hòa kloại hóa trị I, thêm từ từ dd H2SO4 10% vào cốc cho tới khi khí thoát hết thu đk muối sunfat có nộng độ 13,63%. Xác định muối cacbonat.
giả sử muối cacbonat là A2CO3
A2CO3 +H2SO4 --> A2SO4 +CO2+H2O(1)
giả sử nA2CO3=1(mol)
=>mA2CO3=(2MA+60) (g)
theo (1) : nCO2=nA2SO4=nH2SO4=nA2CO3=1(Mol)
=>mddH2SO4=980(g)
mCO2=44(g)
mA2SO4=(2MA+96) (g)
=>\(\dfrac{2MA+96}{2MA+60+980-44}.100=13,63\left(\%\right)\)
=>MA=23(g/mol)
=>A:Na,A2CO3:Na2CO3
Hòa tan một lượng muối cácbonat của một kim loại hóa trị 2 bằng dung dịch H2SO4 16% Sau khi khí ngừng thoát ra nữa thì thu được dung dịch chứa 22,2% muối sunfat xác định công thức phân tử của muối CO3
Gọi công thức muối cacbonat cần tìm là MCO3
giả sử có 1 mol H2SO4 phản ứng
MCO3 + H2SO4 ---> MSO4 + CO2 + H2O
1 <--- 1 --> 1 1
m H2SO4 = 1.98 = 98g---> m dung dịch H2SO4 = (98 . 100)/ 16 = 612,5 g
m MCO3 = M + 60
m CO2 = 1. 44=44 g
m dds pứ = mMCO3 + mH2SO4 - m CO2
= M + 60 + 612,5 - 44
= M + 628,5 g
C% = ( m MSO4 / m dds pứ ) .100= 22,2%
hay ( M+96 / 628,5) .100 = 22,2%
--> M = 56 (1)
và M là hóa trị 2 (2)
---> M là sắt ( Fe = 56 , hóa trị 2)
---> công thức phân thức của muối là FeCO3
Gọi M là kim loại cần tìm
vì chất khí không thoát ra, vẫn còn chất rắn không tan, muối sunphat tan => H2SO4 hết, muối cacbonet còn dư
Giả sử có 1 mol axit phản ứng
MCO3 + H2SO4 --> MSO4 + H2O + CO2
1 <------ 1 --------> 1 --------------> 1
khối lượng muối sunphat = (M+96).1
khối lượng dd sau phản ứng = khối lượng dd axit + khối lượng muối cacbonat đã phản ứng - khối lượng CO2 thoát ra = 1.98.100/14,7 + (M+60).1 - 1.44 = M + 682,67
C% muối sunphat = %
=> M = 24 => M là Mg