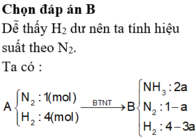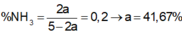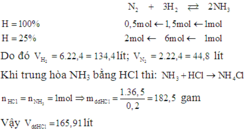Từ 2m3 (đktc) hỗn hợp N2 và H2 (có tỉ lệ thể tích là 1:3) thu được một lượng NH3 đủ để pha chế 3,914 lit dung dịch NH3 20% (d=0,923g/ml). Tính hiệu suất quá trình tổng hợp NH3

Những câu hỏi liên quan
Lượng NH3 tổng hợp được từ 105,4 m3 (đktc) hỗn hợp A được đem chế hóa tiếp thành HNO3 và thu được 252 kg dung dịch HNO3 50%. Tính hiệu suất của quá trình.
Lượng NH3 tổng hợp được từ 105,4 m3 (đktc) hỗn hợp A được đem chế hóa tiếp thành HNO3 và thu được 252 kg dung dịch HNO3 50%. Tính hiệu suất của quá trình.
A gồm N2 và H2 có tỉ lệ mol lần lượt là 1:4. Nung A với xúc tác một thời gian được hỗn hợp B, trong B có 20% NH3 theo thể tích . Tìm hiệu suất phản ứng tổng hợp NH3: A. 62,25% B. 83,34% C. 41,67% D. 50,00%
Đọc tiếp
A gồm N2 và H2 có tỉ lệ mol lần lượt là 1:4. Nung A với xúc tác một thời gian được hỗn hợp B, trong B có 20% NH3 theo thể tích . Tìm hiệu suất phản ứng tổng hợp NH3:
A. 62,25%
B. 83,34%
C. 41,67%
D. 50,00%
Giả sử nN2 = 1mol ⇒ nH2 = 4 mol
N2 + 3H2 → 2NH3
a 3a 2a
Thể tích khí sau phản ứng là: 5 – 4a + 2a = 5 – 2a
B có 20% NH3 theo thể tích ⇒ 2a : (5 – 2a) = 0,2
⇒ a = 0,4167 ⇒ H = 41,67%
Đáp án C.
Đúng 1
Bình luận (0)
Một hỗn hợp A gồm hai khí N2 và H2 theo tỉ lệ 1:3. Tạo phản ứng giữa H2 với N2 cho ra NH3. Sau phản ứng thu được hỗn hợp khí B có tỉ khối: dA/B 0,6. Tính hiệu suất phản ứng tổng hợp NH3. A. 80% B. 50% C. 20% D. 75%
Đọc tiếp
Một hỗn hợp A gồm hai khí N2 và H2 theo tỉ lệ 1:3. Tạo phản ứng giữa H2 với N2 cho ra NH3. Sau phản ứng thu được hỗn hợp khí B có tỉ khối: dA/B = 0,6. Tính hiệu suất phản ứng tổng hợp NH3.
A. 80%
B. 50%
C. 20%
D. 75%
Hỗn hợp A gồm N2 và H2 có tỷ lệ số mol tương ứng là 1:4. Nung A với xúc tác thích hợp thu được hỗn hợp khí B, trong đó NH3 chiếm 20% về thể tích. Hiệu suất của phản ứng tổng hợp NH3 là: A. 10,41%. B. 41,67%. C. 20,83%. D. 43,76%.
Đọc tiếp
Hỗn hợp A gồm N2 và H2 có tỷ lệ số mol tương ứng là 1:4. Nung A với xúc tác thích hợp thu được hỗn hợp khí B, trong đó NH3 chiếm 20% về thể tích. Hiệu suất của phản ứng tổng hợp NH3 là:
A. 10,41%.
B. 41,67%.
C. 20,83%.
D. 43,76%.
Từ 20m3 hỗn hợp khí N2 và H2 lấy theo tỉ lệ 1:3 về thể tích có thể sản xuất được một thể tích NH3 là (Biết hiệu suất phản ứng tổng hợp thực tế là 85%)
A. 5m3
B. 8,5m3
C. 7,5m3
D. 4,75m3
Từ 10 m3 hỗn hợp N2 và H2 ( tỉ lệ 1 : 3 về thể tích ) với hiệu suất phản ứng tổng hợp thực tế là 95% có thể sản xuất được bao nhiêu m3 NH3
PT: \(N_2+3H_2\underrightarrow{t^o}2NH_3\)
VN2 : VH2 = 1:3
VN2 + VH2 = 10
⇒ VN2 = 2,5 m3, VH2 = 7,5 m3
Ở cùng điều kiện nhiệt độ áp suất, tỉ lệ số mol cũng là tỉ lệ thể tích.
Theo PT: \(V_{NH_3\left(LT\right)}=2V_{H_2}=5\left(m^3\right)\)
Mà: H = 95% ⇒ VNH3 (TT) = 5.95% = 4,75 (m3)
Đúng 4
Bình luận (0)
Phải dùng bao nhiêu lít N2 và H2 (đktc) để điều chế 17 gam NH3. Biết hiệu suất chuyển hoán thành NH3 là 25%. Nếu dùng dung dịch HCl 20% (d 1,1g/ml) để trung hòa lượng NH3 trên thì cần bao nhiêu ml? A. 165,91 lít B. 163 lít C. 175,91 lít D. 153 lít
Đọc tiếp
Phải dùng bao nhiêu lít N2 và H2 (đktc) để điều chế 17 gam NH3. Biết hiệu suất chuyển hoán thành NH3 là 25%. Nếu dùng dung dịch HCl 20% (d = 1,1g/ml) để trung hòa lượng NH3 trên thì cần bao nhiêu ml?
A. 165,91 lít
B. 163 lít
C. 175,91 lít
D. 153 lít
Cho 8,96 lít (đktc) hỗn hợp khí gồm N2 và H2 có tỉ lệ thể tích 1:3.Đun nóng hỗn hợp trên với xúc tác thích hợp tạo ra NH3.Sau khi dừng phản ứng thu được &,84 lít hỗn hợp khí (đktc).Tính hiệu suất của phản ứng.
\(N_2+3H_2\leftrightarrow2NH_3\)
ban đầu: 1 mol 3 mol
phản ứng: a → 3a → 2a
dư: 1 – a 3 – 3a 2a
=> n hỗn hợp sau phản ứng = 1–a+3–3a+2a = 4 – 2a
n hỗn hợp trước phản ứng = 1 + 3 = 4 mol
Bảo toàn khối lượng:
m trước = m sau => Mt.n t = Ms.ns
\(\Rightarrow\dfrac{M_t}{M_s}=\dfrac{n_s}{n_t}\Rightarrow\dfrac{4-2a}{4}=0,6\\ \Rightarrow a=0,8\\ \Rightarrow H=\dfrac{0,8}{1}\cdot100\%=80\%\)
Đúng 1
Bình luận (0)