Đốt chày hoàn toàn 6,8g một hợp chất vô cơ A chỉ thu được 4,48l SO2(đktc) và 3,6g H2O . Tìm công thức hóa học?

Những câu hỏi liên quan
đốt cháy hoàn toàn 6,8g một hợp chất vô cơ A chỉ thu được 4,48 lít SO2 và 3,6g H2O. tìm cthh của A
\(n_{SO_2} = \dfrac{4,48}{22,4} = 0,2(mol)\\ n_{H_2O} = \dfrac{3,6}{18} = 0,2(mol) \)
BTKL :
\(m_{O_2} = m_{SO_2} + m_{H_2O} - m_A = 0,2.64 + 3,6-6,8=9,6(gam) \\ \Rightarrow n_{O_2} = 0,3\ mol\)
BTNT với O :
\(n_O = 2n_{SO_2} + n_{H_2O} - 2n_{O_2} = 0,2.2 + 0,2 - 0,3.2 = 0\).Chứng tỏ A không chứa oxi.
\(n_S = n_{SO_2} = 0,2\ mol\\ n_H = 2n_{H_2O} = 0,4\ mol\)
Ta có :
\(n_S : n_H = 0,2 : 0,4 = 1 : 2\)
Vậy CTHH của A : H2S
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn hợp chất hữu cơ A được 4,48l CO2 (đktc) và 3,6g H2O. Tìm công thức đơn giản nhất của A
Xem chi tiết
Đề bài có cho khối lượng của A không bạn?
Đúng 0
Bình luận (1)
1.Nung 9,4g M(NO3)n thu dc 4g MNO2. Tìm công thức muối nitrat
2. Đốt cháy hoàn toàn 6,8g một hợp chất vô cơ A thu dc 4,48l khí SO2(đktc) và 3,6g H2O. Tìm công thức chất A
1.
4M(NO3)\(_n\) \(\rightarrow\) 2M\(_2\)O\(_n\) + 4nNO\(_2\) + nO\(_2\)
n\(_{M\left(NO_3\right)_n}\)= \(\frac{m}{M}\)= \(\frac{9,4}{4M+248n}\) (mol)
n\(_{M_2O_n}\)= \(\frac{m}{M}\)= \(\frac{4}{\text{4M+32n}}\) (mol)
\(\frac{4}{\text{4M+32n}}\)=\(\frac{9,4}{4M+248n}\)
\(\Rightarrow\)M=32n
BL
n=1\(\Rightarrow\) M=32 ( Loại)
n=2\(\Rightarrow\) M=64 (Nhận)
n=3\(\Rightarrow\) M=128 (Loại
\(\Rightarrow\) M là Cu
\(\Rightarrow\) Cu(NO\(_3\))\(_2\)
Đúng 0
Bình luận (0)
2.
A \(\rightarrow\) H\(_2\)O + SO\(_2\) \(\uparrow\)
Mol 0,2 0,2
n\(_{SO_2}\) = \(\frac{4,48}{22,4}=0,2\) (mol)
m\(_S\)= n.M= 0,2.32=6,4(g)
m\(_H\)= 2n.M-0,2.2.1=0,4(g)
m\(_A\)=\(m_S+m_H=6,8\) (g)
Đặt công thức hóa học của tổng quát của A là H\(_x\)S
\(\frac{n_S}{n_H}=\frac{1}{x}=\frac{0,2}{0,4}=\frac{1}{2}\)
\(\Rightarrow\) H\(_2\)S
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6g hợp chất A chứa các nguyên tố C, H, O ta thu được 4,48l CO2(ĐKTC) và 3,6g H2O. Tìm CTPT của A biết MA<66.
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
\(\Rightarrow n_O=\dfrac{m_A-m_C-m_H}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,2:0,4:0,2 = 1:2:1
→ A có CT dạng (CH2O)n
Mà: MA < 66 (g/mol)
⇒ 30n < 66
⇒ n < 2,2
Với n = 1 → A là CH2O.
Với n = 2 → A là C2H4O2.
Đúng 2
Bình luận (0)
CTHH A: \(\left(C_xH_yO_z\right)_n\)
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\\ m_{CO_2}=0,2.44=8,8g\)
\(m_C=\dfrac{3}{11}\cdot8,8=2,4g\\ m_H=\dfrac{1}{9}\cdot3,6=0,4g\\ n_H=\dfrac{0,4}{1}=0,4mol\\ m_O=6-2,4-0,4=3,2g\\ n_O=\dfrac{3,2}{16}=0,2mol\)
Ta có tỉ lệ:
\(x:y:z=0,2:0,4:0,2=1:2:1\)
\(\Rightarrow\)CTHH A \(\left(CH_2O\right)_n\)
\(M_A=30n\)
mà MA < 66
\(\Rightarrow30n< 66\\ \Leftrightarrow n< 2,2\\ \Leftrightarrow n=1;2\\ \Rightarrow CTHH\left(A\right):\left[{}\begin{matrix}C_2H_4O_2\\CH_2O\end{matrix}\right.\)
Đúng 1
Bình luận (1)
đốt cháy hoàn toàn 6g hợp chất hữu cơ A thu đc 4,48l CO2(đktc) và 3,6g h2o a: tính CTPT của A biết MA= 60g/mol b: dẫn toàn bộ lượng CO2 qua dd Ca(OH)2 tính khối lượng khí thu đc
a.Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{3,6}{18}=0,4mol\)
\(n_O=\dfrac{6-\left(0,2.12+0,4.1\right)}{16}=0,2mol\)
=> A gồm C,H và O
\(CTPT:C_xH_yO_z\)
\(x:y:z=0,2:0,4:0,2=2:4:2\)
\(CTĐG:\left(C_2H_4O_2\right)n=60\)
\(\Leftrightarrow n=1\)
Vậy CTPT A: \(C_2H_4O_2\) hay \(CH_3COOH\)
b.\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 ( mol )
\(m_{CaCO_3}=0,2.100=20g\)
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn 18.4g một hợp chất hữu cơ A. Phản ứng kết thúc ta thu được 17,92l CO2(đktc) và 21,6g H2O 1.Tính khối lượng khí O2 đã tham gia phản ứng 2.Hợp chất A chứa những n.tố hóa học nào 3.xác định công thức hóa học của A. Biết tỉ khối hơi của A so với khí Oxi bằng 1,4375 lần 4. Tính số nguyên tử có trong 18,4g A Mình cảm ơn ạ☺️
\(n_{CO_2}=\dfrac{17,92}{22,4}=0,8mol\Rightarrow n_C=0,8mol\Rightarrow m_C=9,6g\)
\(n_{H_2O}=\dfrac{21,6}{18}=1,2g\Rightarrow n_H=2n_{H_2O}=2\cdot1,2=2,4mol\Rightarrow m_H=2,4g\)
\(\Rightarrow m_C+m_H=12g< m_A=18,4g\Rightarrow\)chứa O.
\(\Rightarrow m_O=18,4-12=6,4g\)
Gọi CTĐGN là \(C_xH_yO_z\)
\(x:y:z=\dfrac{m_C}{12}:\dfrac{m_H}{1}:\dfrac{m_O}{16}=\dfrac{9,6}{12}:\dfrac{2,4}{1}:\dfrac{6,4}{16}=2:6:1\)
\(\Rightarrow CTĐGN:C_2H_6O\)
a)\(C_2H_6O_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+3H_2O\)
1 0,8 1,2
\(m_{O_2}=1\cdot32=32g\)
b)Gọi CTPT là \(\left(C_2H_6O\right)_n\)
Theo bài: \(M_A=1,4375\cdot32=46\)
\(\Rightarrow46n=46\Rightarrow n=1\)
Vậy CTPT là \(C_2H_6O\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 2,2g hợp chất hữu cơ A thu được 6,6g CO2 và 3,6g H2O. Biết A có tỉ khối so với khí H2 là 22. Xác định công thức phân tử của hợp chất hữu cơ.
\(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Bảo toán C: nC(A) = 0,15 (mol)
Bảo toàn H: nH(A) = 0,2.2 = 0,4 (mol)
=> \(n_O=\dfrac{2,2-0,15.12-0,4.1}{16}=0\left(mol\right)\)
Xét nC : nH = 0,15 : 0,4 = 3:8
=> CTPT: (C3H8)n
Mà MA = 22.2 = 44(g/mol)
=> n = 1
=> CTPT: C3H8
Đúng 4
Bình luận (0)
Oxh hoàn toàn 0,1mol HCHC A cần dùng 4,48l O2 thu được 4,48l CO2 và 3,6g H2O( biết các thể tích đo ở đktc) .Xđ công thức phân tử của A
Đốt cháy hoàn toàn 2,04g hợp chất A, thu được 1,08g H2O và 1,344 lít SO2 (đktc).
Hãy xác định công thức phân tử của hợp chất A.
Xác định công thức phân tử của hợp chất A
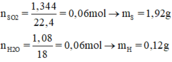
Như vậy hợp chất A chỉ có nguyên tố S và H (Do mS + mH = 1,92 + 0,12 = 2,04 =mA)
Đặt công thức phân tử hợp chất là HxSy
Ta có tỉ lệ x : y = nH : nS = 0,12 : 0,06 = 2 : 1
Vậy công thức phân tử của A và là H2S.
Đúng 0
Bình luận (0)






















