Hỗn hợp gồm Fe và Cu trộn theo tỉ lệ 7:12. Hoà tan hoàn toàn m g X vào 63g dd HNO3 24% đun nóng thu đc dd Y và khí NO2
a. Tính giá trị của m
b. Cô cạn dd y tính khối lượng muối
Hoà tan a gam Cu và Fe (Fe chiếm 30% về khối luợng) bằng 50 ml dd HNO3 63% (D= 1,38g/ml). Sau khi phản ứng xảy ra hoàn toàn thu đựơc chất rắn X cân nặng 0,75a gam, dd Y và 6,104 lít hỗn hợp khí NO và NO2 (đkc). Cô cạn Y thì số gam muối thu được là
A. 75,150g
B. 62,100g
C. 37,575g
D. 49,745g
Hòa tan hoàn toàn 1,23g hỗn hợp X gồm Cu và Al vào dd HNO3 đặc,nóng 1,344lit khí NO2(sản phẩm khử duy nhất) và dd Y.Sục từ từ khí NH3 dư vào dd Y,sau khi các p/ư xảy ra hoàn toàn thu dc m gam kết tủa.giá trị của m là?
ta có
bt kl 64nCu+27nAl=1.23
bt e 2nCu+3nAl=1.344:22.4
->nCu=0.015mol
nAl=0.01mol
h20+nh3->oh- +nh4+
cu2+ +2oh- ->cu(oh)2
0.015 0.015
al3+ +3oh- ->al(oh)3
0.01 0.01
m=0.015*98+0.01*78=2.25g
hòa tan 3,6 g muối sunfua của kim loại M (\(M_2S_n\)) trong dd \(HNO_3\) đặc nóng dư, thu được dd X và hỗn hợp khí Y gồm \(NO_2\) và \(SO_2\), tỉ khối của Y so với \(H_2\) là 24. cô cạn dd X thu được 84,6 g muối nitrat của M. tìm kim loại M
Hoà tan hoàn toàn 12 gam hỗn hợp Fe và Cu (tỉ lệ mol 1:1) bằng axit HNO3, thu được V lít (đktc) hỗn hợp khí X (gồm NO và NO2) và dung dịch Y (chỉ chứa hai muối và axit dư). Tỉ khối của X đối với H2 bằng 19. Giá trị của V là:
A. 2,24
B. 5,60
C. 3,36
D.4,48
Đáp án B
Như vậy đề bài cho axit dư nên 2 muối thu được là Fe3+ và Cu2+
Gọi x là số mol Fe và Cu ta có: 56x + 64 x = 12 ⇒ x = 0,1 mol
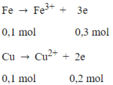
Mặt khác:
![]()
Đặt x, y là số mol của NO và NO2 thì 30x + 46 y = 38 (x+ y)
⇒ x = y
ne nhận = 3x + y = 4x, ne cho = 0,5 ⇒ 4x = 0,5 . Vậy x= 0,125 mol
V = 0,125.2. 22.4= 5,6 lít
hòa tan hết m (g) hh X gồm FeO, Fe2O3,Fe3O4 vào dd HCl đc dd Y. Cô cạn hoàn toàn Y đc 31,75(g) muối Fe(hóa trị 2) và 81,25(g) muối Fe( hóa trị 3). Tính m
hòa tan hoàn toàn 18,4g hỗn hợp gồm kl R có hóa trị 2 và kl M có hóa trị 3 thu đc 11,2l khí hidro a) nếu cô cạn dd nước thì thu đc bn gam muối khan b) tính khối lượng dd HCl 14,6%
\(n_{H_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(R+2HCl\rightarrow RCl_2+H_2\)
\(2M+6HCl\rightarrow2MCl_3+3H_2\)
Ta thấy :
\(n_{HCl}=2n_{H_2}=2\cdot0.5=1\left(mol\right)\)
\(m_{HCl}=1\cdot36.5=36.5\left(g\right)\)
Bảo toàn khối lượng :
\(m_{muối}=18.4+36.5-0.5\cdot2=53.9\left(g\right)\)
\(m_{dd_{HCl}}=\dfrac{36.5}{14.6\%}=250\left(g\right)\)
Hoà tan hoàn toàn hỗn hợp G gồm Al,Fe vào 395 ml HNO3 4M thu đc dd X ( không còn axit ) và 14,02 gam hỗn hợp khí Y gồm 4 khí sản phầm khử duy nhất.Cô cạn X thu đc m1 gam chất rắn khan Z.Cho Z vào dd NaOH vừa đủ thu đc m2 gam chất rắn A.Nung A đến khối lượng không đổi thu đc ( m2 - 8,75 ) gam chất rắn.Xác định phần trăm khối lượng của từng kim loại trong G biết m1/m2=1843/808.
Hoà tan hoàn toàn m gam Cu trong dd HNO3 thu được 1,12 lít hỗn hợp khí NO và NO2 (đktc) có tỉ khối hơi đối với H2 là 16,6. Giá trị của m là:
A. 8,32
B. 4,16
C. 3,90
D. 6,40
M (trung bình NO và NO2) = 16,6.2 = 33.2 gam. n (NO và NO2) = 0.05 (mol)
Gọi x = số mol NO, y = số mol NO2.
Ta có hệ phương trình:
x + y = 0.05
( 30x + 46y )/ (x + y) = 33.2
Giải hệ phương trình => x = 0.04, y = 0.01
Số mol HNO3 phản ứng = 0,04 . 4 + 0,01 . 2 = 0.18 mol.
3 Cu ........ + ..... 8HNO3 ------> ........
0.0675.................0.18 => m Cu = 0.0675 . 64 = 4.32 gam.
=> Đáp án B
Hòa tan hoàn toàn 100 gam hỗn hợp X gồm Fe, Cu , Ag trong dung dịch HNO 3 (dư). Kết thúc phản ứng thu được 13,44 lít hỗn hợp khí Y gồm NO 2 , NO, N 2 O theo tỉ lệ số mol tương ứng là 3 : 2 : 1 và dung dịch Z (không chứa muối NH 4 NO 3 ). Cô cạn dung dịch Z thu được m gam muối khan. Giá trị của m và số mol HNO 3 đã phản ứng lần lượt là:
A. 205,4 gam và 2,5 mol
B. 199,2 gam và 2,4 mol
C. 205,4 gam và 2,4 mol
D. 199,2 gam và 2,5 mol