cho a gam Na tác dụng với p gam nước thu được dd NaOh nồng độ x. Cho b gam Na2O tác dụng với p gam nước cùng thu được dd NaOH thu được dd NaOh nồng độ x. Lập biểu thức p theo a và b

Những câu hỏi liên quan
Cho a gam Na tác dụng với p gam nước thu được dung dịch NaOH có nồng độ x%. Cho b gam Na2O tác dụng với p gam nước cũng thu được dung dịch NaOH có nồng độ x%. Biểu thức p tính theo a, b là: A.
p
3
a
b
31
a
-
32...
Đọc tiếp
Cho a gam Na tác dụng với p gam nước thu được dung dịch NaOH có nồng độ x%. Cho b gam Na2O tác dụng với p gam nước cũng thu được dung dịch NaOH có nồng độ x%. Biểu thức p tính theo a, b là:
A. p = 3 a b 31 a - 32 b
B. p = 9 a b 31 a - 23 b
C. p = 9 a b 23 a - 31 b
D. p = 6 a b 31 a - 23 b
Đáp án : C.
Xét Na : n H 2 = 1 2 n N a = a 46 m o l
Bảo toàn khối lượng :
mdd sau = mNa + m H 2 O – m H 2 = a + p – 2. a 46 (g)
=> C%NaOH = x %
Xét Na2O
=> mdd sau = m N a 2 O + m H 2 O = b + p
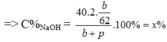
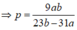
Đúng 0
Bình luận (2)
Cho a gam K tác dụng với m gam nước thu được KOH có nồng độ x%. Cho b gam K2O tác dụng với m gam nước cùng thu được KOH x%. Lập biểu thức m tính theo a và b
Cho m1 gam Na tác dụng với p gam nước thu được dung dịch NaOH nồng đọ a%. Cho m2 gam Na2O tác dụng với p gam nước cũng thu đưuọc dung dịch NaOH nồng độ a%. Lập biểu thức liên hệ giữa m1,m2 và p.
cho a gam na vào p gam h2o thu được dd naoh x%. cho b gam na2o vào p gam h2o cũng thu được dd naoh x%. lập biểu thức tính p theo a và b
Theo đề bài ta có :
nNa=\(\dfrac{a}{23}mol\)
Ta có PTHH : 1
\(2Na+2H2O\rightarrow2NaOH+H2\)
a/23.........a/23.........a/46
X=\(\dfrac{mct\left(mNaOH\right)}{m\text{dd}NaOH}.100\%=\dfrac{\left(\dfrac{a}{23}\right).40}{a+p-\left(\dfrac{a}{46}\right)}=\dfrac{40a}{23a+23p}\)(1)
Ta có : nNa2O=\(\dfrac{b}{62}mol\)
PTHH 2 :
\(Na2O+H2O\rightarrow2NaOH\: \)
b/62mol................2.(b/62)mol
=> X=\(\dfrac{mct}{m\text{dd}}.100\%=\dfrac{\left(2.\left(\dfrac{b}{62}\right)\right).40}{b+p}=\dfrac{40b}{124b+124p}\left(2\right)\)
Ta cho (1)=(2)
ta có biểu thức :
\(\dfrac{40a}{23a+23p}=\dfrac{40b}{124b+124p}\)
Bạn tự rút gọn biểu thức nhé!
Đúng 0
Bình luận (1)
CHO MÌNH CHỮA LẠI 1 CHÚT nãy ghi nhầm =.=
Theo đề bài ta có :
nNa=\(\dfrac{a}{23}mol\)
PTHH 1 :
\(2Na+2H2O\rightarrow2NaOH+H2\uparrow\)
a/23mol..................2(a/23)mol....1/2(a/23)mol
=> X=\(\dfrac{mct}{m\text{dd}}.100\%=\dfrac{40.2.\left(\dfrac{a}{23}\right)}{a+p-2.\dfrac{1}{2}\left(\dfrac{a}{23}\right)}\)=\(\dfrac{80a}{23a+23p}\)(1)
Theo đề bài ta có :
nNa2O=\(\dfrac{b}{62}mol\)
PTHH 2 :
\(Na2O+H2O\rightarrow2NaOH\)
b/62mol.................2(b/62)mol
=> X= \(\dfrac{mct}{m\text{đ}}.100\%=\dfrac{40.2\left(\dfrac{b}{62}\right)}{b+p}=\dfrac{80b}{62b+62p}\left(2\right)\)
Cho (1)=(2)
Ta có biểu thức : \(\dfrac{80a}{23a+23p}\)= \(\dfrac{80b}{62b+62p}\)
Đúng 0
Bình luận (4)
LÀM TẮT NHA
Dùng điện thoại khó ghi lắm .
Na +2H2O --> 2NaOH + H2 (1)
a/23 mol.................................a/23mol
Na2O + H2O --> 2NaOH(2)
b/62mol...............................b/32mol
mdd(1) = a+p-a/23.x%=40a/22a+23p
mdd(2) = b+ p.x%=40b /31b+31p
=>p=ab/b - 31p
Vậy....
đánh mất 30 phút v:
Đúng 0
Bình luận (1)
Cho 200 gam dd NaOH tác dụng hoàn toàn với 200 gam dd Axit Clohidric 7,3% sau phản ứng thu được dd muối Natri Clorua và nước.
a/ Tính nồng độ phần trăm dung dịch NaOH cần dùng.
b/ Tính nồng độ phần trăm dd muối tạo thành sau PƯ.
(Na= 23; Cl= 35,5; H= 1)
a)mH2SO4=\(\dfrac{200.7,3\text{%}}{100\%}\)=14,6g
nHCl=\(\dfrac{14,6}{36,5}\)=0,4(mol)
PTHH:
NaOH+ HCl→ NaCl+ H2O
1 1 1 1
0,4 0,4 0,4 (mol)
⇒mNaOH=0,4.40=16(g)
Nồng độ % của dd NaOH cần dùng là:
C%NaOH=\(\dfrac{16}{200}\) .100%=8%
b)Ta có:mdd spứ=mdd trc pứ=400g
mNaCl=0,4.58,5=23,4g
Nồng độ % dd muối tạo thành sau pứ là:
C%dd NaCl=\(\dfrac{23,4}{400}\) .100%=5,85%
Đúng 1
Bình luận (0)
Câu 2:Có một hỗn hợp m gam gồm kim loại Al và Fe, hai dd NaOH và HCl chưa rõ nồng độ biết rằng: - 100ml dd HCl tác dụng vừa đủ với 3,71 gam Na2CO3 và 20 gam dd NaOH thu được 5,85g muối khan. - Cho m gam hỗn hợp Al, Fe tác dụng vừa đủ với 66,67 g dd NaOH hoặc 700ml dd HCl. a. Tính CM dd HCl và nồng độ % dd NaOH. b. Tính khối lượng mỗi kim loại trong hỗn hợp.
Cho 4.6 gam Na tác dụng hết với nước thu được 200 gam dd X và thấy có V lít khí H2 thoát ra ở đktc a) Viết PTHH xảy ra b) Tính V? c) dd X là gì/ Tính nồng độ phần trăm của dd X tạo thành
\(n_{Na}=\dfrac{4.6}{23}=0.2\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(0.2......................0.2.......0.1\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
Dung dịch X : NaOH
\(m_{dd_X}=4.6+200-0.1\cdot2=204.4\left(g\right)\)
\(C\%_{NaOH}=\dfrac{0.2\cdot40}{204.4}\cdot100\%=3.9\%\%\)
Đúng 1
Bình luận (1)
a) $2Na + 2H_2O \to 2NaOH + H_2$
n Na = 4,6/23 = 0,2(mol)
n H2 = 1/2 n Na = 0,1(mol)
V H2 = 0,1.22,4 = 2,24(lít)
c) Dung dịch X là dd NaOH
n NaOH = n Na = 0,2(mol)
C% NaOH = 0,2.40/200 .100% = 4%
Đúng 0
Bình luận (0)
Cho 200 ml dung dịch Al 2 SO 4 3 0,5M tác dụng với 200 gam dd NaOH thu được 11,7 gam kết tủa trắng. Nồng độ dung dịch NaOH lớn nhất là
A. 10%
B. 9%
C. 12%
D. 13%
Cho 15,5 gam Na2O tác dụng với nước thu được 500 ml dd A. Tính:
a/ Nồng độ mol dd A? b/ Để trung hòa dd A cần dùng bn lit dd H2SO4 20% (d = 1,14 g/ml)?
Số mol của natri oxit
nNa2O = \(\dfrac{m_{Na2O}}{M_{Na2O}}=\dfrac{15,5}{62}=0,25\left(mol\right)\)
Pt : Na2O + H2O→ 2NaOH\(|\)
1 1 2
0,25 0,5
a) Số mol của dung dịch natri hidroxit
nNaOH = \(\dfrac{0,25.2}{1}=0,5\left(mol\right)\)
500ml = 0,5l
Nồng độ mol của dung dịch natri hidroxit
CMNaOH = \(\dfrac{n}{V}=\dfrac{0,5}{0,5}=1\left(M\right)\)
b) H2SO4 + 2NaOH → Na2SO4 + 2H2O\(|\)
1 2 1 2
0,25 0,5
b) Số mol của axit sunfuric
nH2SO4 = \(\dfrac{0,5.1}{2}=0,25\left(mol\right)\)
Khối lượng của axit sunfuric
mH2SO4 = nH2SO4 . MH2SO4
= 0,25 . 98
= 24,5 (g) Khối lượng của dung dịch axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{24,5.100}{20}=122,5\) (g)
Thể tích của dung dịch axit sunfuric cần dùng
D = \(\dfrac{m}{V}\Rightarrow V=\dfrac{m}{D}=\dfrac{122,5}{1,14}=107,45\left(ml\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (1)



















