muốn pha 100ml dung dịch h2so4 3m thì khối lượng h2so4 cần lấy là

Những câu hỏi liên quan
Có 100ml dung dịch H2SO4 98%, khối lượng riêng là 1,84 g/ml. Người ta muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20%.
Tính thể tích nước cần dung để pha loãng.
Thể tích nước cần dùng để pha loãng.
Khối lượng của 100ml dung dịch axit 98%
100ml × 1,84 g/ml = 184g
Khối lượng H2SO4 nguyên chất trong 100ml dung dịch trên: 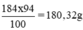
Khối lượng dung dịch axit 20% có chứa 180,32g H2SO4 nguyên chất: 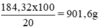
Khối lượng nước cần bổ sung vào 100ml dung dịch H2SO4 98% để có được dung dịch 20%: 901,6g – 184g = 717,6g
Vì D của nước là 1 g/ml nên thể tích nước cần bổ sung là 717,6 ml.
Đúng 1
Bình luận (0)
Có 100ml dung dịch H2SO4 98%, khối lượng riêng là 1,84 g/ml. Người ta muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20%.
Khi pha loãng phải tiến hành như thế nào?
Cách tiến hành khi pha loãng
Khi pha loãng lấy 717,6 ml H2O vào ống đong hình trụ có thể tích khoảng 2 lít. Sau đó cho từ từ 100ml H2SO4 98% vào lượng nước trên, đổ axit chảy theo một đũa thủy tinh, sau khi đổ vài giọt nên dùng đũa thủy tinh khuấy nhẹ đều. Không được đổ nước vào axit 98%, axit sẽ bắn vào da, mắt..và gây bỏng rất nặng
Đúng 0
Bình luận (0)
Có 100 ml H2SO4 98% , khối lượng riêng là 1,84 g/ml. Nếu muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20% thì cần thêm vào bao nhiêu ml nước? Bồ ơi giúp với❤
\(C\%_{sau}=0,2=\dfrac{100.1,84.0,98}{100.1,84+V_{H_2O}}\\ V_{H_2O}=717,6mL\)
Đúng 1
Bình luận (0)
Từ dung dịch H2SO4 98% có d = 1.84 g/ml. Cần bao nhiêu lít dung dịch trên để pha thành 1L dung dịch H2SO4 5M. Lấy 100ml dung dịch H2SO4 5M trên sau đó cho vào 750ml nước. Xác định nồng độ dung dịch H2SO4 vừa pha.
Trung hòa 100ml dung dịch H2SO4 3M bằng dung dịch KOH 2M
a) Viết PTHH.
b) Tính khối lượng muối thu được.
c) Tính thể tích của dung dịch KOH cần dùng?
d) Tính nồng độ mol/l của dung dịch thu được sau phản ứng?
100ml = 0,1l
\(n_{H2SO4}=3.0,1=0,3\left(mol\right)\)
a) Pt : \(H_2SO_4+2KOH\rightarrow K_2SO_4+2H_2O|\)
1 2 1 2
0,3 0,6 0,3
b) \(n_{K2SO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
⇒ \(m_{K2SO4}=0,3.174=52,2\left(g\right)\)
c) \(n_{KOH}=\dfrac{0,3.2}{1}=0,6\left(mol\right)\)
\(V_{ddKOH}=\dfrac{0,6}{2}=0,3\left(l\right)\)
d) \(V_{ddspu}=0,1+0,3=0,4\left(l\right)\)
\(C_{M_{K2SO4}}=\dfrac{0,3}{0,4}=0,75\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
1)Tính thể tích dung dịch H2SO4 1M thu được khi pha loãng 30ml dug dịch H2SO4 98%(D=1,84g/ml)
2)Tính khối lượng SO3 cần dùng để khi pha vào 200g dung dịch H2SO4 9,8% thu được dung dịch H2SO4 49%
3)Tính tỉ lệ khối lượng oleum 71% SO3 cần để khi trộn với dung dịch H2SO4 nguyên chất tạo oleum 62%SO3
1. \(n_{H_2SO_4\left(98\%\right)}=\dfrac{30.1,84.98\%}{98}=0,552\left(mol\right)\)
=>\(V_{H_2SO_4\left(1M\right)}=\dfrac{0,552}{1}=0,552\left(l\right)\)
Đúng 1
Bình luận (0)
Hòa tan 12,1 gam hỗn hợp gồm CuO và ZnO thì cần 100ml dung dịch HCl 3M
a, Viết PTHH xảy ra
b, Tính thành phần % theo khối lượng của mỗi oxit trong hỗn hợp
c, Tính khối lượng dung dịch H2SO4 nồng độ 20% để hòa tan hoàn toàn lượng hỗn hợp oxit trên
CuO +2HCl= CuCl2 +H2O
ZnO+2HCl= ZnCl2 +H2O
gọi x,y là mol của CuO, ZnO
80x + 81y = 12.1
2x+2y = 0.3
=> x=0.05 , y=0.1 => mCuO= 4 %CuO=4/12.1 m ZnO=8.1 =>%ZnO=8.1/12.1
nH2SO4=1/2nHCl=0.3/2 =0.15
mH2SO4=0.15x98=14.7g => mddH2SO4=14.7/20%=73.5g
Đúng 0
Bình luận (0)
Một loại oleum có công thức H2SO4.nSO3. Lấy 33,8 g oleum nói trên pha thành 100ml dung dịch A. Để trung hoà 25 ml dung dịch A cần dùng vừa đủ 100ml dung dịch NaOH 2M. Giá trị của n là
A. 1
B. 2
C. 3
D. 4
Đáp án C
Giải:
nH2SO4=1/2 nNaOH = 0,1 => nH2SO4 tạo thành = 0,4 H2SO4.nSO3+nH2O -> (n+1)H2SO4
=> noleum = 0,4/(n+1) => 98+80n = 33,8(n+1)/0,4 => n=3
Đúng 0
Bình luận (0)
Xác định lượng SO3 và lượng dung dịch H2SO4 49% cần lấy để pha thành 450g dung dịch H2SO4 73,5%
Gọi x là KL SO3 cần lấy và y là KL dd H2SO4 49% cần lấy (g)
mH2SO4(dd 73,5%)= 73,5%. 450=330,75(g) (Axit đặc vậy tạt đánh ghen là chết)
SO3 + H2O -> H2SO4
Ta có hpt:
\(\left\{{}\begin{matrix}x+y=450\\\dfrac{98}{80}x+0,49y=330,75\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=150\\y=300\end{matrix}\right.\)
Vậy cần dùng 150 gam SO3 và 300 gam dung dịch H2SO4 49% để pha chế thành 450 gam dung dịch H2SO4 73,5% (đặc qué rồi)
Đúng 3
Bình luận (2)



















