Có m g hỗn hợp gồm Mg và CuO hòa tan trong dung dịch H2SO4 loãng dư đến khi lượng hỗn hợp tan hoàn toàn thấy vừa hết 58,8g H2SO4 lúc đó dung dịch sau phản ứng tăng thêm m - 0,58 so với ban đầu. Tính m
Cho 6,4g hỗn hợp A gồm Fe và Mg phản ứng với 100g dung dịch H2SO4 loãng vừa đủ được 3,584 lít (đkc) và dung dịch B a, tính % theo khối lượng mỗi chất có trong A b, tính C% của từng muối trong dung dịch B c, đốt cháy 6,4g hỗn hợp A ở trên với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không có khí dư). Hòa tan Y bằng 1 lượng vừa đủ 120ml dung dịch HCl 2M thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z thu được 56,69g kết tủa. Tính % theo thể tính của Cl2 trong hỗn hợp X
Hòa tan hết m gam hỗn hợp X gồm: Na, Na2O, K, K2O , Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng vào nước thu được 400ml dung dịch Y và 1,568 lít H2( đktc). Trộn 200ml dung dịch Y với 200ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400ml dung dịch có pH = 13. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 12.
B. 14.
C. 15.
D. 13.
Đáp án D
► Xử lý dữ kiện 200 ml dung dịch Y: nH+ = 0,2 × (0,2 + 0,15 × 2) = 0,1 mol.
pH = 13 ⇒ OH– dư ⇒ [OH–] = 1013 – 14 = 0,1M ⇒ nOH– dư = 0,4 × 0,1 = 0,04 mol.
||⇒ nOH–/Y = 0,04 + 0,1 = 0,14 mol ⇒ 400 ml dung dịch Y chứa 0,28 mol OH–.
► Dễ thấy nOH– = 2nH2 + 2nO/oxit ⇒ nO/oxit = (0,28 – 2 × 0,07) ÷ 2 = 0,07 mol.
||⇒ m = 0,07 × 16 ÷ 0,0875 = 12,8(g)
Hỗn hợp A có khối lượng 6,1g gồm CuO, Al2O3 và FeO. Hòa tan hoàn toàn A cần 130ml dung dịch H2SO4 loãng 1M, thu được dung dịch B.Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc lấy kết tủa đen nung trong không khí đến khối lượng không đổi, được 3,2g chất rắn.
Tính khối lượng từng oxit trong A.
giúp em với ạ.
giup
Gọi x,y,z là số mol của \(CuO, Al_2O_3, FeO\)
=> \(80x+102y+72z=6,1\)(1)
A + \(H_2SO_4\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
\(FeO+H_2SO_4\rightarrow FeSO_4+H_2O\)
=>x+3y+z=0,13 (2)
B+NaOH dư, lấy kết tủa nung trong không khí
=>Chất rắn là CuO và Fe2O3 do kết tủa của nhôm tan hết trong NaOH dư
\(BTNT(Cu):\)\(n_{CuO}=x\left(mol\right)\)
\(BTNT\left(Fe\right):n_{Fe_2O_3}=\dfrac{1}{2}n_{FeO}=\dfrac{z}{2}\)
=> 80x+\(160.\dfrac{z}{2}\)=3,2 (3)
Từ (1), (2), (3)=>x=0,02 ; y=0,03; z=0,02
\(\Rightarrow m_{CuO}=1,6\left(g\right);m_{Al_2O_3}=3,06\left(g\right);m_{FeO}=1,44\left(g\right)\)
Hòa tan 12,8 gam hỗn hợp A gồm (Fe và Fe2O3) vào dung dịch H2SO4 loãng 0,46M dư. Sau khi phản ứng kết thúc thu được 4,48 lít khi H2 (đktc).
a/ Viết các phương trình hóa học.
b/ Tính % theo khối lượng của mỗi chất có trong hỗn hợp A.
c/ Tính thể tích H2SO4 loãng tham gia phản ứng.
\(a,Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ b,n_{Fe}=n_{H_2}=0,2\left(mol\right)\\ \%m_{Fe}=\dfrac{0,2.56}{12,8}.100\%=87,5\%\\ \%m_{Fe_2O_3}=100\%-87,5\%=12,5\%\\ c,n_{Fe_2O_3}=\dfrac{12,8-11,2}{160}=0,01\left(mol\right)\\ n_{H_2SO_4}=n_{Fe}+3n_{Fe_2O_3}=0,2+3.0,01=0,23\left(mol\right)\\ V_{ddH_2SO_4}=\dfrac{0,23}{0,46}=0,5\left(M\right)\)
Hỗn hợp X gồm Fe3O4 và CuO. Cho 29,2 gam X phản ứng với CO nung nóng, sau một thời gian thu được hỗn hợp rắn Y và hỗn hợp khí Z. Cho Z tác dụng với dung dịch Ba(OH)2 dư thu được 9,85 gam kết tủa. Hòa tan hết Y trong 150 gam dung dịch HNO3 63% đun nóng thu được dung dịch T và 4,48 lít NO2 (đktc) (sản phẩm khử duy nhất). Cho V (lít) dung dịch NaOH 1M vào dung dịch T, phản ứng hoàn toàn tạo ra kết tủa với khối lượng lớn nhất. Phần trăm khối lượng Fe3O4 và giá trị V là
A. 79,45% và 0,525 lít
B. 20,54% và 1,300 lít
C. 79,45% và 1,300 lít
D. 20,54% và 0,525 lít.
Hòa tan 14,8 gam hỗn hợp gồm Fe và Cu vào lượng dư dung dịch hỗn hợp HNO3 và H2SO4 đặc nóng. Sau phản ứng thu được 10,08 lít NO2 (đktc) và 2,24 lít SO2 (đktc). Khối lượng Fe trong hỗn hợp ban đầu là:
A. 5,6
B. 8,4
C. 18
D. 18,2
Đáp án B
Gọi a, b lần lượt là số mol của Fe, Cu
56a + 64b = 14,8 (1)
Quá trình nhường electron:
Fe - 3e → Fe
a 3a
Cu - 2e → Cu
b 2b
→ ∑ne nhường = (3a + 2b) mol
Quá trình nhận electron:
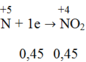
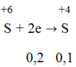
→ ∑ne nhận = 0,45 + 0,2 = 0,65 mol
Áp dụng định luật bảo toàn electron:
3a + 2b = 0,65 → a = 0,15 và b = 0,1 → mFe = 8,4 g
Cho hỗn hợp X gồm CuO và NaOH có tỉ lệ số mol 1:1 tác dụng vừa đủ với dung dịch hỗn hợp HCl 1M và H2SO4 0,5M thu được dung dịch Y chỉ chứa m gam hỗn hợp muối trung hòa. Điện phân dung dịch Y với điện cực trơ màng ngăn xốp cường độ I = 2,68A đến khi khối lượng dung dịch giảm 20,225 gam mất t giây thì dừng lại, thu được dung dịch Z. Cho m gam Fe vào Z, sau khi phản ứng kết thúc thu được 0,9675m gam hỗn hợp hai kim loại. Giá trị của t là
A. 11523
B. 10684
C. 12124
D. 14024
Cho m gam hỗn hợp X gồm hai amino axit A và B (MA < MB) có tổng số mol là 0,05; chỉ chứa tối đa 2 nhóm -COOH (cho mỗi chất). Cho m gam hỗn hợp X trên tác dụng với 56 ml dung dịch H2SO4 0,5M. Sau phản ứng phải dùng 6 ml dung dịch NaOH 1M để trung hòa hết với H2SO4 dư. Nếu lấy 1/2 hỗn hợp X tác dụng vừa đủ với 25 ml dung dịch Ba(OH)2 0,6M; cô cạn dung dịch sau phản ứng thu được 4,26 gam muối. Thành phần phần trăm (khối lượng) của amino axit B trong m gam hỗn hợp X là
A. 52,34
B. 32,89.
C. 78,91.
D. 24,08.
Hòa tan hoàn toàn 7.5 gam hỗn hợp gồm Mg và Al bằng lượng vừa đủ V lít dung dịch HNO3 1M. Sau khi các phản ứng kết thúc, thu được 0,672 lít N2 (đktc) duy nhất và dung dịch chứa 54,9 gam muối. Giá trị của V là?
nN2 = 0,03
m muối - mkim loại = mNO3
=> mNO3 = 54,9-7,5 = 47,4(g)
=> nN(trong muối) = nNO3 = \(\frac{47,4}{62}=0,764mol\)
BT nguyên tố N => nHNO3 = nN(trong muối) +nN2 = 0,764 + 0,03.2 = 0,824 mol
=> V = 0,824 (l)