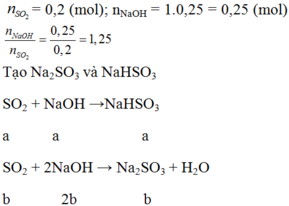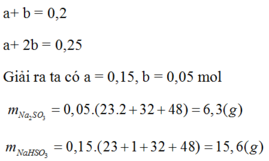Câu 2.Hấp thụ hoàn toàn 12,8 gam SO2 vào 250 ml dung dịch NaOH 1M.
a) Viết các phương trình hóa học của phản ứng xảy ra. b) Tính khối lượng muối tạo thành sau phản ứng.
Những câu hỏi liên quan
hấp thụ hoàn toàn 12,8 gam SO vào 250 ml dung dịc NaOH 1M : a) viết phương trình hóa học của các phản ứng có thể xảy ra ; b) tính khối lượng muối tạo thành sau phản ứng .
a)NaOH+SO2 \(\rightarrow\) NaHSO3 (1)
NaOH+SO2 \(\rightarrow\) Na2SO3+H2O (2)
b)Ta có co số mol SO2 là : n = 12,8 / 64 = 0,2
số mol NAOH là : n =0,25 x 1 = 0,25
Ta có tỷ lệ :
n [NaOH]/ n [SO2] = 0,25/0,2 = 1,25
Nên sẽ xảy ra đồng thời 2 phản ứng 1 và 2
NaOH + SO2 = NaHSO3 (1)
x mol x mol x mol
2NaOH + SO2 = Na2So3 + H2O (2)
y mol y/2 mol y/2 mol
Từ (1)(2): Ta có hệ phương trình :
x+y = 0,25
x+y/2 = 0,2
Giải hệ trên ta có x = 0,15 mol
y= 0,1 mol
Khối lượng muối sau phản ứng sẽ bao gồm 2 muối là NaHSO3 và NA2SO3
Số mol Nahso3 = x = 0,15 mol
==> Khối lương NAHSO3 = 0,15 x 104 = 15,6 g
Số mol NA2SO3 = y/2 = 0,1 /2 = 0,05 mol
==> Khối lượng NA2SO3 = 0,05 x 126 = 6,3 g
Vậy khối lượng muối thu dc sau phản ứng là : 15,6 + 6,3 = 21,9 g
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 12,8g SO2 vào 250ml dung dịch NaOH 1M.
Viết các phương trình hóa học của phản ứng có thể xảy ra.
Tính khối lượng muối tạo thành sau phản ứng

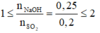 ⇒ phản ứng tạo 2 muối
⇒ phản ứng tạo 2 muối
Phương trình hóa học của phản ứng
SO2 + NaOH → NaHSO3
SO2 + 2NaOH → Na2SO3 + H2O
Gọi nNa2SO3 = x mol; nNaHSO3 = y mol
nNaOH = 2x + y = 0,25.
nSO2 = x + y = 0,2.
Giải ra ta có: x = 0,05, y = 0,15.
mNaHSO3 = 0,15 x 104 = 15,6g.
mNa2SO3 = 0,05 x 126 = 6,3g.
Đúng 0
Bình luận (0)
Cho một lượng sắt phản ứng vừa đủ với dung dịch đồng 2 sunfat. Thêm 200 ml dung dịch NaOH 1M vào dung dịch sau phản ứng để kết tủa hết muối sắt tạo ra a) viết các phương trình hóa học của các phản ứng xảy ra b) tính khối lượng sắt tham gia phản ứng
\(a)Fe+CuSO_4\rightarrow FeSO_4+Cu\\ FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_2+Na_2SO_4\\ b)n_{NaOH}=0,2.1=0,2mol\\ n_{Fe}=n_{Fe\left(OH\right)_2}=0,2:2=0,1mol\\ m_{Fe}=0,1.56=5,6g\)
Đúng 2
Bình luận (0)
15. Hấp thụ hoàn toàn 12,8 g SO2 vào 250 ml dd NaOH 1M
a) Viết các phương trình phản ứng có thể xảy ra.
b) Tính khối lượng muối tạo thành sau phản ứng.
a) PTPỨ: \(SO_2+NaOH\rightarrow NaHSO_3\)
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
b) \(n_{SO_2}=0,2\left(mol\right);n_{NaOH}=1.0,25=0,25\left(mol\right)\)
\(\Rightarrow\frac{n_{NaOH}}{n_{SO_2}}=\frac{0,25}{0,2}=1,25\)
\(SO_2+NaOH\rightarrow NaHSO_3\)
a a a
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
b 2b b
\(\Rightarrow\left\{{}\begin{matrix}a+b=0,2\\a+2b=0,25\end{matrix}\right.\)
Giải ra ta được: \(a=0,15mol;b=0,05mol\)
\(\rightarrow m_{Na_2SO_3}=0,05\left(23,2+32+48\right)=6,3\left(g\right)\)
\(\rightarrow m_{NaHSO_3}=0,15\left(23+1+32+48\right)=15,6\left(g\right)\)
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 12,8g SO2 vào 250ml dung dịch NaOH 1M. Khối lượng muối tạo thành sau phản ứng là: A. 15,6g và 5,3g B. 18g và 6,3g C. 15,6g và 6,3g D. Kết quả khác
Đọc tiếp
Hấp thụ hoàn toàn 12,8g SO2 vào 250ml dung dịch NaOH 1M. Khối lượng muối tạo thành sau phản ứng là:
A. 15,6g và 5,3g
B. 18g và 6,3g
C. 15,6g và 6,3g
D. Kết quả khác
Hấp thụ hoàn toàn 12,8g SO2 vào 250 ml dung dịch NaOH 1M.
a) Viết các phương trình hóa học của các phản ứng có thể xảy ra.
b) Tính khối lượng muối tạo thành sau phản ứng.
nSO2 = 12,8 / 64 = 0,2 mol.
nNaOH = 1 x250 / 1000 = 0,25 mol.
a) Phương trình hóa học của phản ứng
SO2 + NaOH → NaHSO3
SO2 + 2NaOH → Na2SO3 + H2O
Gọi nNa2SO3 = x; nNaHSO3 = y.
nNaOH = 2y + x = 0,25.
nSO2 = x + y = 0,2.
Giải ra ta có: x = 0,15, y = 0,05.
mNaHSO3 = 0,15 x 104 = 15,6g.
mNa2SO3 = 0,5 x 126 = 63g.
Đúng 0
Bình luận (0)
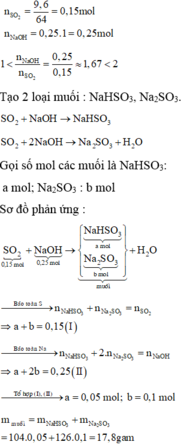
Hấp thụ hoàn toàn 9,6 gam SO2 vào 250ml dung dịch NaOH 1M. Khối lượng của muối thu được sau phản ứng là
A. 15,6 gam.
B. 18,9 gam.
C. 6,3 gam.
D. 17,8 gam.
đốt cháy hoàn toàn 6,2 gam photpho trong oxi dư . cho sản phẩm tạo thành tác dụng vừa đủ với dung dịch NaOH 32% tạo ra muối Na2HPO4 .
a) viết phương trình hóa học của các phản ứng xảy ra .
b) tính khối lượng dung dịch NaOH đã dùng .
c) tính nồng độ phần trăm của muối trong dung dịch thu được sau phản ứng .
a, (1) 4P+5.O2->2.P2O5
(2) P2O5+4.NaOH->2.Na2HPO4+H2O
b, photpho có n=6,2:31=0,2 mol.dựa theo pt (1) thấy nP2O5=0,1mol.theo pt (2) thấy nNaOH=0,4mol vậy mNaOH=0,4.40=16 g vậy m(dd NaOH)=16:32%=50 g
c, theo pt (2) nNa2HPO4 =0,2 mol vậy mNa2HPO4=0,2.142=28,4 g
m(dd sau pư)=mP+m(dd NaOH)=6,2+50=56,2 g
=> C%(dd Na2HPO4)=28,4:56,2=50,53%
Đúng 0
Bình luận (2)
đốt cháy hoàn toàn 6,2 gam photpho trong oxi dư . cho sản phẩm tạo thành tác dụng vừa đủ với dung dịch NaOH 32% tạo ra muối Na2HPO4 .
a) viết phương trình hóa học của các phản ứng xảy ra .
b) tính khối lượng dung dịch NaOH đã dùng .
c) tính nồng độ phần trăm của muối trong dung dịch thu được sau phản ứng .