Cho 1,1 g một kim loại kiềm tác dụng với nước thu được 1,792 lit H2 (đktc)
a) Viết PTHH dạng tổng quát
b) Xác định tên kim loại kiềm
Bài 1: Cho 5.52g một kim loại kiềm tác dụng với nước tạo ra 2.688 lít khí H2 (đktc). Xác định tên kim loại đó.
Bài 2: Cho 1.84g một kim loại kiềm tác dụng với nước tạo ra 896ml khí H2 (đktc). Xác định tên kim loại đó.
Bài 1:
Gọi kim loại kiềm là R
\(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
Giả sử R hóa trị I:
\(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\\ \Rightarrow n_R=0,12.2=0,24\left(mol\right)\\ \Rightarrow M_R=\dfrac{5,52}{0,24}=23\left(đvC\right)\)
Giả sử đúng, tên kim loại đó là sodium (Na)
Bài 2: Tự làm tương tự bài 1 nhé=0
Cho 8,0 gam một kim loại kiềm thổ ( hóa trị II) tác dụng với nước dư thu được 4,48 lít khí H2 (đktc). Xác định tên kim loại kiềm thổ trên?
Giúp em với
\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(M+2H_2O\rightarrow M\left(OH\right)_2+H_2\)
\(0.2........................................0.2\)
\(M_M=\dfrac{8}{0.2}=40\left(\dfrac{g}{mol}\right)\)
\(M:Ca\left(Canxi\right)\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: A + 2H2O --> A(OH)2 + H2
_____0,2<--------------------------0,2
=> \(M_A=\dfrac{8}{0,2}=40\left(g/mol\right)=>Ca\)
Hòa tan 3,68 g một kim loại kiềm M hòa tan vào nước dư, thu được 1,792 lit khí H, (đktc) và 200 ml dung dịch X. a-Xác định tên kim loại kiểm. b-Tính nồng độ moll của dung dịch X.
Gọi M là khối lượng mol trung bình của 2 nguyên tố
nH2=6.72/22.4=0.3 mol
M + H2O --> MOH + 1/2 H2
0.6mol---------------------0.3mol
-> M=20.2/0.3=67.3333
-->M1<67.33<M2
mà 2 kim loại này thuộc hai chu kì liên tiếp nhau
--> Kim loại đó là KI và Rb
Cho 3,9 gam một kim loại kiềm tác dụng với H2O dư thu được 1,12 lit H2 (đktc).Xác định tên kim loại đó.
Hãy xác định ô nguyên tố, chu kì, nhóm; Công thức hợp chất khí với hiđro (nếu có), Công thức oxit, hiđroxit cao nhất, hiđroxit cao nhất có tính chất gì?
Cho 3,1 g hỗn hợp gồm hai kim loại kiềm ở hai chu kì kế tiếp nhau trong bảng tuần hoàn tác dụng hết với nước thu được 1,12 lít H2 ở đktc và dung dịch kiềm. Xác định tên 2 KL đó và tính thành phần phần trăm khối lượng mỗi kim loại
Gọi công thức chung cho hai kim loại kiềm là M
Số mol H2: nH2 = 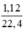 = 0,05(mol)
= 0,05(mol)
PTHH: 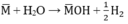
Theo pt: nM = 2. nH2 = 2. 0,05 = 0,1(mol)
⇒ M = 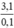 = 31 → Na, K
= 31 → Na, K
Gọi x, y lần lượt là số mol của Na và K trong hỗn hợp
Theo bài ra ta có hệ phương trình:
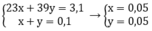
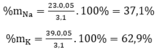
Cho a gam kim loại kiềm tác dụng với dung dịch HCL dư thu được 11,7gam muối và 2,24 lít khí H2 đktc .Xác định tên kim loại và tính giá trị a
\(\text{Đ}\text{ặt}:A\\ A+HCl\rightarrow ACl+H_2\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_A=n_{ACl_2}=2.n_{H_2}=0,1.2=0,2\left(mol\right)\\ M_{ACl}=\dfrac{11,7}{0,2}=58,5\left(\dfrac{g}{mol}\right)\\ M\text{à}:M_{ACl}=M_A+35,5\\ \Rightarrow M_A=23\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Natri\left(Na\right)\\ a=23.0,2=4,6\left(g\right)\)
nH2=2,24/22,4=0,1(mol)
2M+2HCl→2MCl+H2
0,2 ← 0,2 ← 0,1
Có 0,2 .(M+35,5)=11,7(gam)
⇒ M=23 ⇒M là Na
mNa=23. 0,2= 4,6 (gam)
Cho 1,17 gam một kim loại kiềm X tác dụng với nước (dư) thu được 0,336 lit khí H2 (đktc). X là
A. Rb
B. Li
C. Na
D. K
Chọn D
X + H2O -> XOH + ½ H2
=> nX = 2nH2 = 0,03 mol => MX = 39g (K)
Cho 11,5 gam một kim loại kiềm tác dụng hết với nước thu được 5,6 lít khí hidro (đktc). Xác định tên của kim loại (Li=7, Na=23, K=39, Ba=137).
Cho 7,02 gam kim loại kiềm tác dụng hết với nước thu được 0,18 gam khí ( đktc). Xác định tên kim loại là ( Na=23, K=39, Ba=137, Ca=40)
Gọi CTHH của kim loại kiềm là A
A + H2O ----> AOH + 1/2H2
nH2 = 0,18/2 = 0,09 (mol)
Theo pthh : nA = 2nH2 = 0,18 (mol)
=> MA = mA/nA = 7,02/0,18 = 39 (g/mol)
=> Kim loại cần tìm là Kali