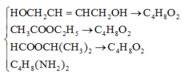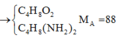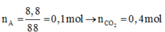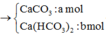Một hỗn hợp khí X gồm hidrocacbon X1 và anken X2. Đốt cháy hoàn toàn 100 cm3 hỗn hợp trên thu được 300 cm3 khí CO2 và 300 cm3 Hơi nước. xác định CTPT

Những câu hỏi liên quan
Một hỗn hợp khí X gồm hidrocacbon X1, anekn X2. Đốt cháy hoàn toàn 100 cm3 hỗn hợp trên thu được 400 cm3 khí CO2; 450 cm3 hơi nước. Xác định CTPT
Vì khi nung hỗn hợp H2, anken, ankan chỉ thu được 1 hidrocacbon duy nhất => Ankan và anken có cùng số nguyên tử cacbon trong phân tử và H2 anken phản ứng hết
Gọi công thức ankan và anken là : CnH2n+2 và CnH2n (n≥2)
Gọi x, y, z là thể tích của H2, CnH2n và CnH2n+2 trong 100cm3 hỗn hợp
CnH2n + H2 →→ CnH2n+2
x x x
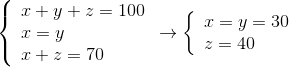 => Vankan+anken =70cm3
=> Vankan+anken =70cm3
n=VCO2Vankan+anken=21070=3
Đốt cháy hoàn toàn 15 cm3 một hidrocacbon A phải dùng hết 82,5 cm3 O2. Các khí thu đc ở đktc. Xác định CTPT A. Biết A có 2 liên kết đôi và tham gia pư trùng hợp
Hỗn hợp khí A gồm metan và hidrocacbon. Đốt cháy hoàn toàn 1,0 lít A cần dùng vừa đủ 2,6 lít khí O2 thu được CO2 và hơi nước. Dẫn toàn bộ sản phẩm cháy lội từ từ vào dung dịch H2SO4 đặc dư thấy có 1,6 lít khí KHÔNG bị hấp thụ. Xác định CTPT của hiddrocacbon và tính phần trăm thể tích của CH4 trong hỗn hợp A. Biết rằng các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất.
Đọc tiếp
Hỗn hợp khí A gồm metan và hidrocacbon. Đốt cháy hoàn toàn 1,0 lít A cần dùng vừa đủ 2,6 lít khí O2 thu được CO2 và hơi nước. Dẫn toàn bộ sản phẩm cháy lội từ từ vào dung dịch H2SO4 đặc dư thấy có 1,6 lít khí KHÔNG bị hấp thụ. Xác định CTPT của hiddrocacbon và tính phần trăm thể tích của CH4 trong hỗn hợp A. Biết rằng các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất.
Đốt cháy 100 cm3 hỗn hợp gồm amin đơn chức A với không khí có dư thì thu được 105 cm3 khí. Cho hơi nước ngưng tụ còn 91 cm3. Cho hỗn hợp qua tiếp dung dịch KOH dư thì còn 83 cm3 Tìm công thức cấu tạo của A Tính % về thể tích của A trong hỗn hợp đầu. Biết các thể tích đo cùng điều kiện, và không khí chứa 80% thể tích N2
Khi đốt cháy hoàn toàn 8,8 gam hỗn hợp A gồm HOCH2CHCHCH2OH,CH3COOC2H5,HCOOCH(CH3)2,C4H8(NH2)2, thu được hỗn hợp sản phẩm cháy X gồm các khí và hơi. Dẫn toàn bộ hỗn hợp X qua 300 ml dung dịch nước vôi trong 1M thu thấy khối lượng dung dịch tăng 5,7 gam. Xác định % thể tích N2 trong hỗn hợp X. A. 8,11% B. 1,43% C. 2,86% D. 4,05%
Đọc tiếp
Khi đốt cháy hoàn toàn 8,8 gam hỗn hợp A gồm
HOCH2CH=CHCH2OH,CH3COOC2H5,HCOOCH(CH3)2,C4H8(NH2)2, thu được hỗn hợp sản phẩm cháy X gồm các khí và hơi. Dẫn toàn bộ hỗn hợp X qua 300 ml dung dịch nước vôi trong 1M thu thấy khối lượng dung dịch tăng 5,7 gam. Xác định % thể tích N2 trong hỗn hợp X.
A. 8,11%
B. 1,43%
C. 2,86%
D. 4,05%
đốt cháy hoàn toàn hỗn hợp A gồm 1 hidrocacbon ở thể khí và oxi dư thu dduocj hỗn hợp B có thành phần thể tích là 30%co2 20%h2o 50%o2 xác định ctpt của h-c
\(Coi\ n_B = 1(mol) \\ n_{CO_2} = 1.30\% =0,3(mol) ; n_{H_2O} = 1.20\% = 0,2(mol)\\ A: C_nH_{2n+2-2k}\\\ n_C = n_{CO_2} = 0,3(mol)\\ n_H = 2n_{H_2O} = 0,4(mol)\\ Ta có : \dfrac{n}{2n+2-2k} = \dfrac{0,3}{0,4}\\ \Leftrightarrow 0,4n = 0,6n + 0,6 - 0.6k\\ \Leftrightarrow 0,6k -0,2n = 0,6\\ \Leftrightarrow 6k - 2n = 6\)
Với k = 1 thì n = 0(loại)
Với k = 2 thì n = 3(chọn)
Với k = 3 thì n = 6(chọn)
.....
Vậy hidrocacbon có thể là : \(C_3H_4 ; C_6H_8,...\)
Đúng 2
Bình luận (0)
\(Coi\ n_B = 1(mol)\\ \Rightarrow n_{CO_2} = 1.30\% = 0,3(mol) ; n_{H_2O} = 20\% = 0,2(mol) ; n_{O_2} = 50% = 0,5(mol)\)
Vì \(n_{CO_2} > n_{H_2O} \Rightarrow A: C_nH_{2n-2}\)
\(n_A = n_{CO_2} - n_{H_2O} = 0,3 - 0,2 = 0,1(mol)\\ \Rightarrow n = \dfrac{n_{CO_2}}{n_A} = \dfrac{0,2}{0,1} = 2\\ CTPT\ A: C_2H_2\)
Đúng 1
Bình luận (2)
Một hỗn hợp X (gồm hai anken liên tiếp nhau trong dãy đồng đẳng và một lượng hidro dư) có tỉ khối hơi so với hiđro là 6,875. Nung hỗn hợp trên với Ni đến phản ứng hoàn toàn (H 100%) thu được hỗn hợp khí Y có tỉ khối hơi so với hiđro là 55/6. Xác định CTPT hai anken A. C2H4 và C3H6 B. C5H12 và C5H10 C. C4H8 và C3H6 D. C4H8 và C5H10
Đọc tiếp
Một hỗn hợp X (gồm hai anken liên tiếp nhau trong dãy đồng đẳng và một lượng hidro dư) có tỉ khối hơi so với hiđro là 6,875. Nung hỗn hợp trên với Ni đến phản ứng hoàn toàn (H = 100%) thu được hỗn hợp khí Y có tỉ khối hơi so với hiđro là 55/6. Xác định CTPT hai anken
A. C2H4 và C3H6
B. C5H12 và C5H10
C. C4H8 và C3H6
D. C4H8 và C5H10
Đáp án C
hhX gồm hai anken kế tiếp và H2 dư có dX/H2 = 6,875.
Nung X với Ni → hhY có dY/H2 = 55/6.
• Giả hhX gồm hai anken có CT là CnH2n x mol và H2 dư y mol.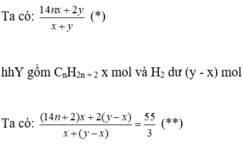
Từ (*), (**) → x = 3y → n = 3,5
→ Hai anken là C3H6 và C4H8
Đúng 0
Bình luận (0)
Đốt 100cm3 hỗn hợp khí gồm hiđro, 1 ankan, 1 ankin thu được 210 cm3 CO2. Nếu đun 100cm3 hỗn hợp với bột Ni thì chỉ còn 70 cm3 1 hiđrocacbon duy nhất. Các thể tích khí đo ở cùng điều kiện.
Tìm CTPT của 2 hiđrocacbon trên và thành phần % thể tích của hỗn hợp đầu
khi đun hh với Ni tạo ra 1 hidrocacbon duy nhất => ankan và ankin có cúng số nguyên tử C
các khí đo ở cùng điều kiện nên tỉ lệ mol= tỉ lệ V
CTTQ ankan : CnH2n+2
ankin : CnH2n-2
CnH2n+2 + \(\dfrac{3n+1}{2}\)O2 -to-> nCO2 +(n+1)H2O (1)
CnH2n-2 + \(\dfrac{3n-1}{2}\)O2 -to-> nCO2 +(n-1)H2O (2)
2H2 +O2 -to-> 2H2O (3)
CnH2n-2 + 2H2 -Ni-> CnH2n+2 (4)
VH2=100-70=30(cm3)
=> Vankan,ankin=70(cm3)
giả sử nankan=x(mol)
nankin=y(mol)
=> x+y=70 (I)
lại có n(x+y)=210(II)
thay (I) vào (II)
=>n=3
=> ankan : C3H8
ankin : C3H4
theo (4) : nC3H4=1/2nH2=15 (cm3) => VC3H4 =15(cm3)
=> VC3H8=55(cm3)
=> %VH2=30(%)
%VC3H4=15(%)
%VC3H8=55(%)
Đúng 0
Bình luận (0)
đốt cháy hoàn toàn hỗn hợp A gồm 1 hidrocacbon ở thể khí và oxi dư thu dduocj hỗn hợp B có thành phần thể tích là 30%co2 20%h2o 50%o2 xác định ctpt của h-c