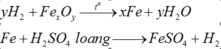Tính thể tích khí Hidro (đktc) cẩn thiết để khử 4,8g \(Fe_2O_3\). Nếu khử \(Fe_2O_3\)bằng khí CO thì thể tích khí là bao nhiêu? Trong thực tế nên khử các oxit kim loại bằng khí CO hay khí\(H_2\)? Tại sao?

Những câu hỏi liên quan
Khử 16 gam hỗn hợp các oxit kim loại: FeO, Fe2O3, Fe3O4, CuO và PbO bằng khí CO ở nhiệt độ cao, khối lượng chất rắn thu được là 11,2 gam. Tính thể tích khí CO đã tham gia phản ứng (đktc).
A. 22,4l
B. 4,48 l
C. 5,6 l
D. 6,72 l
Đáp án D
Áp dụng ĐLBTKL:
Ta có:

⇒ 28x - 44x = 11,2 - 16
⇒ x = 0,3
Vậy VCO = 0,3.22,4 = 6,72 lít
Đúng 0
Bình luận (0)
Cho 10,8g Al tác dụng hết với đ HCl. Hãy cho biết: a) Thể tích khí H2 sinh ra ở đktc b) Tính khối lượng muối tạo thành c) Nếu dùng thể tích H2 trên để khử CuO tính khốu lượng Cu sinh ra
a) \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,4------------>0,4---->0,6
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b)
\(m_{AlCl_3}=0,4.133,5=53,4\left(g\right)\)
c)
PTHH: CuO + H2 --to--> Cu + H2O
0,6------>0,6
=> mCu = 0,6.64 = 38,4 (g)
Đúng 5
Bình luận (1)
`n_[Al]=[10,8]/27=0,4(mol)`
`2Al + 6HCl -> 2AlCl_2 + 3H_2 \uparrow`
`0,4` `0,4` `0,6` `(mol)`
`a)V_[H_2]=0,6.22,4=13,44(l)`
`b)m_[AlCl_2]=0,4.98=39,2(g)`
`c)`
`H_2 + CuO` $\xrightarrow{t^o}$ `Cu + H_2 O`
`0,4` `0,4` `(mol)`
`=>m_[Cu]=0,4.64=25,6(g)`
Kim loại M có thể được điều chế bằng cách khử ion của nó trong oxit bởi khí hiđro ở nhiệt độ cao. Mặt khác, kim loại M có thể tác dụng với dung dịch H2SO4 loãng giải phóng H2. Vậy kim loại M là A. Fe. B. Al. C. Ag. D. Cu.
Đọc tiếp
Kim loại M có thể được điều chế bằng cách khử ion của nó trong oxit bởi khí hiđro ở nhiệt độ cao. Mặt khác, kim loại M có thể tác dụng với dung dịch H2SO4 loãng giải phóng H2. Vậy kim loại M là
A. Fe.
B. Al.
C. Ag.
D. Cu.
Kim loại M có thể được điều chế bằng cách khử ion của nó trong oxit bởi khí hiđro ở nhiệt độ cao. Mặt khác, kim loại M có thể tác dụng với dung dịch
H
2
SO
4
loãng giải phóng
H
2
. Vậy kim loại M là: A. Fe. B. Al. C. Cu. D. Ag
Đọc tiếp
Kim loại M có thể được điều chế bằng cách khử ion của nó trong oxit bởi khí hiđro ở nhiệt độ cao. Mặt khác, kim loại M có thể tác dụng với dung dịch H 2 SO 4 loãng giải phóng H 2 . Vậy kim loại M là:
A. Fe.
B. Al.
C. Cu.
D. Ag
Kim loại M có thể được điều chế bằng cách khử ion của nó trong oxit bởi khí hiđro ở nhiệt độ cao. Mặt khác, kim loại M có thể tác dụng với dung dịch H2SO4 loãng giải phóng H2. Vậy kim loại M là A. Fe B. Al C. Cu D. Ag
Đọc tiếp
Kim loại M có thể được điều chế bằng cách khử ion của nó trong oxit bởi khí hiđro ở nhiệt độ cao. Mặt khác, kim loại M có thể tác dụng với dung dịch H2SO4 loãng giải phóng H2. Vậy kim loại M là
A. Fe
B. Al
C. Cu
D. Ag
Khử hoàn toàn m gam oxit MxOy cần vừa đủ 17,92 lít khí CO (đktc), thu được a gam kim loại M. Hòa tan hết a gam M bằng dung dịch H2SO4 đặc nóng (dư), thu được 20,16 (lít) khí SO2 (sản phẩm khử duy nhất, ở đktc). Oxit MxOy là: A. Cr2O3 B. FeO C. Fe3O4 D. CrO
Đọc tiếp
Khử hoàn toàn m gam oxit MxOy cần vừa đủ 17,92 lít khí CO (đktc), thu được a gam kim loại M. Hòa tan hết a gam M bằng dung dịch H2SO4 đặc nóng (dư), thu được 20,16 (lít) khí SO2 (sản phẩm khử duy nhất, ở đktc). Oxit MxOy là:
A. Cr2O3
B. FeO
C. Fe3O4
D. CrO
Đáp án C
Ta có: nCO = 0,8 mol; = 0,9 mol
Gọi n là hóa trị của kim loại M (1 ≤ n ≤ 3)
Trong phản ứng giữa M với H2SO4 đặc nóng, M là chất khử nhường electron.
H2SO4 đặc là chất oxi hóa nhận electron:

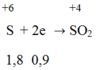
Trong phản ứng khử oxit kim loại bởi CO ta luôn có:
nO (trong oxit) = nCO = 0,8 mol
⇒Tỉ lệ:
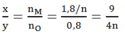
Dựa vào các đáp án ta thấy n = 2 hoặc n = 3

Đúng 0
Bình luận (0)
1/ cho 8,96 l khí CO đi qua ống sứ tròn, dài, nung nóng chứa m g bột đồng(II) oxit.khi pư kết thúc thu được hỗn hợp khí X có tỉ khối so voi khi H2 là 18. tính m? biết các khí đo ở đktc
2/ khử hoàn toàn m gam Fe2O3 bằng khí CO ở nhiệt độ cao, lượng kim loại thu được sau pư cho vao dd HCl dư đến khi pư kết thúc đem toàn bộ khí thu được khử một oxit của kim loại R bị khử cũng là m g. Tìm CTPT kim loại R?
Đọc tiếp
1/ cho 8,96 l khí CO đi qua ống sứ tròn, dài, nung nóng chứa m g bột đồng(II) oxit.khi pư kết thúc thu được hỗn hợp khí X có tỉ khối so voi khi H2 là 18. tính m? biết các khí đo ở đktc
2/ khử hoàn toàn m gam Fe2O3 bằng khí CO ở nhiệt độ cao, lượng kim loại thu được sau pư cho vao dd HCl dư đến khi pư kết thúc đem toàn bộ khí thu được khử một oxit của kim loại R bị khử cũng là m g. Tìm CTPT kim loại R?
1/
\(PTHH:\) \(CO+CuO-t^o->Cu+CO_2\)
Theo đề, hỗn hợp khí thu được sau phản ứng có tỉ khối so với H2 là 18. Mà tỉ khối của CO2 so với H2 là 22
Chứng tỏ khí X thu được sau phản ứng gồm \(\left\{{}\begin{matrix}CO_2:a\left(mol\right)\\CO\left(dư\right):b\left(mol\right)\end{matrix}\right.\)
\(\overline{M_X}=18.2=36\left(\dfrac{g}{mol}\right)\)
\(< =>36=\dfrac{44a+28b}{a+b}\)
\(< =>8a-8b=0\)
\(<=>a-b=0\) \((I)\)
Theo PTHH: \(nCO(pứ)=a(mol)\)
\(nCO(đktc)=\dfrac{8,96}{22,4}=0,4(mol)\)
\(< =>a+b=0,4\) \((II)\)
Từ (I) và (II) ta có: \(\left\{{}\begin{matrix}a-b=0\\a+b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,2\end{matrix}\right.\)
Theo PTHH: \(nCuO=nCO_2=b=0,2(mol)\)
\(=> m=mCuO=0,2.80=16(g)\)
Đúng 0
Bình luận (0)
Khử 24g Fe2O3 ở nhiệt độ cao bằng các chất khác nhau là : H2, bột Al, CO
a) Viết các phương trình phản ứng xảy ra
b) Tính thể tích ( đktc) của các chất khử ở thể khí và khối lượng của chất khử ở thể rắn
c) Tính khối lượng Fe thu được trong mỗi trường hợp trên
Khử 24g Fe2O3 ở nhiệt độ cao bằng các chất khác nhau là : H2, bột Al, CO
a) Viết các phương trình phản ứng xảy ra
b) Tính thể tích ( đktc) của các chất khử ở thể khí...
Đọc tiếp
Khử 24g Fe2O3 ở nhiệt độ cao bằng các chất khác nhau là : H2, bột Al, CO
a) Viết các phương trình phản ứng xảy ra
b) Tính thể tích ( đktc) của các chất khử ở thể khí và khối lượng của chất khử ở thể rắn
c) Tính khối lượng Fe thu được trong mỗi trường hợp trên
Khử 24g Fe2O3 ở nhiệt độ cao bằng các chất khác nhau là : H2, bột Al, CO
a) Viết các phương trình phản ứng xảy ra
b) Tính thể tích ( đktc) của các chất khử ở thể khí và khối lượng của chất khử ở thể rắn
c) Tính khối lượng Fe thu được trong mỗi trường hợp trên
GIÚP MÌNH VỚI, MÌNH ĐANG CẦN GẤP Ạ ! Tks
nFe2O3=24/160=0,15(mol)
Fe2O3+3H2--t*->2Fe+3H2O(1)
0,15____0,45____0,3
Fe2O3+2Al--->Al2O3+Fe(2)
0,15___0,3___________0,15
Fe2O3+3CO--->2Fe+3CO2(3)
0,15____0,45___0,3
(1)VH2=0,45.22,4=10,08(l)
mFe=0,3.56=16,8(g)
(2)mAl=0,3.27=8,1(g)
mFe=0,15.56=8,4(g)
(3)VCO=0,45.22,4=10,08(l)
mFe=0,3.56=16,8(g)
Đúng 0
Bình luận (0)
Khử 24g Fe2O3 ở nhiệt độ cao bằng các chất khác nhau là : H2, bột Al, CO
a) Viết các phương trình phản ứng xảy ra
b) Tính thể tích ( đktc) của các chất khử ở thể khí và khối lượng của chất khử ở thể rắn
c) Tính khối lượng Fe thu được trong mỗi trường hợp trên