Hãy tìm công thức của một hợp chất X có thành phần theo khối lượng là 36,8%FE,21,0%S và 42,2%O. Biết khối lượng mol của hợp chất bằng 152g/mol. Trong 0,5 mol hợp chất X có bao nhiêu mol nguyên tử của mỗi nguyên tố

Những câu hỏi liên quan
Hãy tìm công thức hóa học của một hợp chất có thành phần theo khối lượng là 36,8% Fe; 21,0% S; 42,2% O. Biết khối lượng mol của hợp chất bằng 152 g/mol.
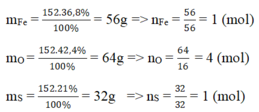
Vậy trong 1 phân tử hợp chất có 1 nguyên tử Fe, 4 nguyên tử O, 1 nguyên tử S.
⇒ CTHH là FeSO4.
Đúng 1
Bình luận (0)
Hãy tìm công thức hóa học của một hợp chất có thành phần theo khối lượng là 36,8% Fe; 21,0% S; 42,2% O. Biết khối lượng mol của hợp chất bằng 152 g/mol
Khối lượng mol của Fe là MFe = = 56 g
Khối lượng mol của S là: MS = = 32 g
Khối lượng mol của O là: MO = = 64 g
Gọi công thức hóa học của hợp chất là FeXSyOz, ta có:
56 . x = 56 => x = 1
32 . y = 32 => y = 1
16 . z = 64 => z = 4
Vậy hợp chât có công thức hóa học là FeSO4
Đúng 0
Bình luận (0)
Khối lượng mol của Fe là \(M_{Fe}\) = (152 . 36,8)/100 = 56 g
Khối lượng mol của S là: \(M_S\) = (152 . 21)/100 = 32 g
Khối lượng mol của O là: \(M_O\) = (152 . 42,2)/100 = 64 g
Gọi công thức hóa học của hợp chất là \(Fe_xS_yO_z\), ta có:
\(56.x=56\Rightarrow x=1\)
\(32.y=32\Rightarrow y=1\)
\(16.z=64\Rightarrow z=4\)
Vậy hợp chât có công thức hóa học là \(FeSO_4\)
Đúng 0
Bình luận (0)
Hãy tìm công thức hóa học của một hợp chất có thành phần theo khối lượng là 36,8% Fe; 21,0% S; 42,2% O. Biết khối lượng mol của hợp chất bằng 152 g/mol
Khối lượng mol của Fe là MFe = = 56 g
Khối lượng mol của S là: MS = = 32 g
Khối lượng mol của O là: MO = = 64 g
Gọi công thức hóa học của hợp chất là FeXSyOz, ta có:
56 . x = 56 => x = 1
32 . y = 32 => y = 1
16 . z = 64 => z = 4
Vậy hợp chât có công thức hóa học là FeSO4
Đúng 0
Bình luận (2)
Khối lượng mol của Fe là MFe = = 56 g
Khối lượng mol của S là: MS = = 32 g
Khối lượng mol của O là: MO = = 64 g
Gọi công thức hóa học của hợp chất là FeXSyOz, ta có:
56 . x = 56 => x = 1
32 . y = 32 => y = 1
16 . z = 64 => z = 4
Vậy hợp chât có công thức hóa học là FeSO4
Đúng 0
Bình luận (1)
Trong hợp chất 1 mol có khối lượng của từng nguyên tố là :
\(m_{Fe}=\dfrac{152.36,8}{100}=56\) \(g\)
\(m_S=\dfrac{152.21}{100}=32\) \(g\)
\(m_O=\dfrac{152.42,2}{100}=64\) \(g\)
Gọi CTHH của hợp chất là \(Fe_xS_yO_z\) , ta có :
\(56.x=56\Rightarrow x=1\)
\(32.y=32\Rightarrow y=1\)
\(16.2=64\Rightarrow z=4\)
Vậy hợp chất có CTHH là \(FeSO_4\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
bài 1: hợp chất A có tỉ khối so với H2 là 22. Hãy cho biết 5,6 lít khí A ở(đktc) có khối lượng là bao nhiêu gam?bài 2: tìm công thữ hóa học của những hợp chất có thành phần nguyên tố như sau:a) hợp chất A tạo bởi 2 nguyên tố: C và O có khối lượng mol là 44(g?mol),trong đó cacbon chiếm 27,3% về khối lượng,còn lại là % Ob) hợp chất B tạo bởi 3 nguyên tố: Na,C,O có khối lượng mol là 44(g/mol), thành phần các nguyên tố lần lượt là: 43,4% Na,11,3% C,45,3%c) một hợp chất khí A có thành phần % theo khố...
Đọc tiếp
bài 1: hợp chất A có tỉ khối so với H2 là 22. Hãy cho biết 5,6 lít khí A ở(đktc) có khối lượng là bao nhiêu gam?
bài 2: tìm công thữ hóa học của những hợp chất có thành phần nguyên tố như sau:
a) hợp chất A tạo bởi 2 nguyên tố: C và O có khối lượng mol là 44(g?mol),trong đó cacbon chiếm 27,3% về khối lượng,còn lại là % O
b) hợp chất B tạo bởi 3 nguyên tố: Na,C,O có khối lượng mol là 44(g/mol), thành phần các nguyên tố lần lượt là: 43,4% Na,11,3% C,45,3%
c) một hợp chất khí A có thành phần % theo khối lượng: 82,35% N,17,65% H. Hợp chất A có tỉ khối với H2 là 8,5. Hãy cho biết:
- CTHH của hợp chất A
- số mol nguyên tử của các nguyên tố có trong 0,5 mol hợp chất A.
bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
Đúng 0
Bình luận (0)
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g
Đúng 0
Bình luận (0)
a)
MC=27,3×44÷100\(\approx\)12g/mol
% mO=100-27,3=72,7%
MO=72,7×44÷100\(\approx\)32g/mol
Công thức hóa học chung: CaxOy
Theo công thức hóa học có:
x×\(III\)=y×\(IV\)
Lập tỉ lệ: \(\dfrac{x}{y}=\dfrac{II}{IV}=\dfrac{2}{4}=\dfrac{1}{2}\)
=>x=1 và y=2
Công thức hóa học của hợp chất: CO\(_2\)
Đúng 0
Bình luận (0)
Hãy tìm công thức hoá học của những hợp chất có thành phần các nguyên tố như sau : a, Hợp chất A có khối lượng mol phần tử là 58,5g/mol , thành phần các nguyên tố theo khối lượng : 60,68% CI và còn lại là Na. b, Hợp chất B có khối lượng mol phần tử là 106g/mol , thành phần các nguyên tố theo khối lượng : 43,4% Na ; 11,3% C và 45,3%O
b. Ta có: \(\%_{Na}=100\%-60,68\%=39,32\%\)
Gọi CTĐG của A là: NaxCly
Ta lại có: \(\dfrac{x}{y}=\dfrac{\dfrac{39,32\%}{23}}{\dfrac{60,68\%}{35,5}}\approx\dfrac{1,7}{1,7}=\dfrac{1}{1}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
Gọi CTHH của A là: \(\left(NaCl\right)_n\)
Theo đề, ta có: \(M_{\left(NaCl\right)_n}=\left(23+35,5\right).n=58,5\)(g/mol)
\(\Leftrightarrow n=1\)
Vậy CTHH của A là NaCl
b. Gọi CTĐG của B là: \(Na_aC_bO_c\)
Ta có: \(x:y:z=\dfrac{43,4\%}{23}:\dfrac{11,3\%}{12}:\dfrac{45,3\%}{16}\approx1,9:0,9:2,8\approx2:1:3\)
Gọi CTHH của B là: \(\left(Na_2CO_3\right)_t\)
Theo đề, ta có: \(M_{\left(Na_2CO_3\right)_t}=\left(23.2+12+16.3\right).t=106\)(g/mol)
\(\Leftrightarrow t=1\)
Vậy CTHH của B là Na2CO3
Đúng 2
Bình luận (1)
Tìm công thức hoá học của hợp chất B biết thành phần % theo khối lượng của các nguyên tố của hợp chất B là : 80% Cu và 20% O . Biết hợp chất B có khối lượng mol phân tử là 80g/mol
\(m_{Cu}=\dfrac{80.80}{100}=64g\\ m_O=80-64=16g\\ n_{Cu}=\dfrac{64}{64}=1mol\\ n_O=\dfrac{16}{16}=1mol\\ CTHH:CuO\)
Đúng 2
Bình luận (1)
Gọi CTHH của B là: \(Cu_xO_y\)
Ta có: \(x:y=\dfrac{80\%}{64}:\dfrac{20\%}{16}=1,25:1,25=1:1\)
Vậy CTHH của B là: CuO
Vì Cu và O không có chỉ số tỉ lệ với nhau nên không cần khối lượng mol nhé
Đúng 0
Bình luận (1)
\(m_{Cu}=\%Cu.M_B=80\%.80=64\left(g\right)\\ m_O=m_B-m_{Cu}=80-64=16\left(g\right)\\ n_{Cu}=\dfrac{m}{M}=\dfrac{64}{64}=1\left(mol\right)\\ n_O=\dfrac{m}{M}=\dfrac{16}{16}=1\left(mol\right)\\ CTHH:CuO\)
Đúng 0
Bình luận (1)
Cho biết thành phần theo khối lượng của một số hợp chất, hãy tìm công thức hóa học của chúng: - Hợp chất A: 0,2 mol hợp chất có chứa 4,6g Na và 7,1g Cl. - Hợp chất B: 0,03 mol hợp chất có chứa 0,36g C và 0,96g O. - Hợp chất C: 0,02 mol hợp chất có chứa 4,14g Pb và 0,32g O. - Hợp chất D: 0,04 mol hợp chất có chứa 0,08 mol nguyên tử Fe và 0,12 mol nguyên tử O. - Hợp chất E: 0,02 mol hợp chất có 0,04 mol nguyên tử Na, 0,02mol nguyên tử C và 0,06 mol nguyên tử O.
Đọc tiếp
Cho biết thành phần theo khối lượng của một số hợp chất, hãy tìm công thức hóa học của chúng:
- Hợp chất A: 0,2 mol hợp chất có chứa 4,6g Na và 7,1g Cl.
- Hợp chất B: 0,03 mol hợp chất có chứa 0,36g C và 0,96g O.
- Hợp chất C: 0,02 mol hợp chất có chứa 4,14g Pb và 0,32g O.
- Hợp chất D: 0,04 mol hợp chất có chứa 0,08 mol nguyên tử Fe và 0,12 mol nguyên tử O.
- Hợp chất E: 0,02 mol hợp chất có 0,04 mol nguyên tử Na, 0,02mol nguyên tử C và 0,06 mol nguyên tử O.
- Hợp chất A:
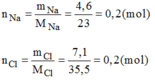
Cứ 0,2 mol hợp chất A có chứa 0,2 mol Na và 0,2 mol Cl.
Suy ra 1 mol hợp chất A có chứa 1 mol Na và 1 mol Cl.
Vậy công thức hóa học đơn giản của A là NaCl.
- Hợp chất B:
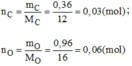
Vậy 0,03mol phân tử B có chứa 0,03 mol phân tử C và 0,06 mol nguyên tử O.
Suy ra 1 mol phân tử B có chứa 1 mol nguyên tử C và 2 mol nguyên tử O.
→Công thức hóa học của B là C O 2
- Hợp chất C:
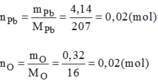
Vậy 0,02 mol phân tử C có chứa 0,02 mol nguyên tử Pb và 0,02 mol nguyên tử O.
Suy ra 1 mol phân tử C có chứa 1 mol nguyên tử Pb và 1 mol nguyên tử O.
→Công thức của phân tử C là: PbO.
- Hợp chất D:
Theo đề bài: 0,04 mol phân tử D có 0,08 mol Fe và 3 mol O.
Vậy 1 mol phân tử D có: 2 mol Fe và 0,12 mol O.
→ Công thức hóa học của D là F e 2 O 3
- Hợp chất E:
Cho biết: 0,02 mol phân tử E có 0,04 mol Na kết hợp 0,02 mol C và 0,06 mol nguyên tử O.
Vậy 1 mol phân tử E co 2 mol Na kết hợp 1 mol C và 3 mol O.
Công thức hóa học của E là N a 2 C O 3 .
Đúng 0
Bình luận (0)
Một hợp chất X có thành phần khối lượng của các nguyên tố là: 32,4% Na; 22,54%S và 45,1%O. Khối lượng mol của hợp chất bằng 142 gam. Hãy xác định công thức hóa học của hợp chất X
Gọi CTHH là \(Na_xS_yO_z\)
\(x:y:z=\dfrac{\%Na}{23}:\dfrac{\%S}{32}:\dfrac{\%O}{16}=\dfrac{32,4}{23}:\dfrac{22,54}{32}:\dfrac{45,1}{16}=1,41:0,74:2,82=2:1:4\)Vậy CTĐGN(công thức đơn giản nhất) là \(Na_2SO_4\)
Lại có: \(M_X=142đvC\)\(\Rightarrow\left(Na_2SO_4\right)_n=142\Rightarrow n=1\)
Vậy CTHH là \(Na_2SO_4\)
Đúng 1
Bình luận (0)
Một hợp chất khí có thành phần phần trăm theo khối lượng là 82,35% N và 17,65% H. Em hãy cho biết: Số mol nguyên tử của nguyên tố có trong 0,5 mol hợp chất.
Trong 0,5 mol N H 3 có: 0,5 mol nguyên tử N
0,5x3=1,5 mol nguyên tử H.
Đúng 0
Bình luận (0)


























