Cho 6,08g hỗn hợp NaOH và KOH tác dụng hết với dd HCl tạo ra 8,30g hỗn hợp muối clorua.Số gam mỗi hidroxit trong hỗn hợp?

Những câu hỏi liên quan
Cho 6,08 gam hỗn hợp NaOH và KOH tác dụng hết với dung dịch HCl tạo ra 8,30 gam hỗn hợp muối clorua. Số gam mỗi hiđroxit trong hỗn hợp lần lượt là ?
Goi x la so mol NaOH y la so mol KOH Ta co pt khoi luong 40x + 56y = 6.08
58.5x +74.5y = 8.3
=> x = 0.04 y = 0.08 => m NaOH = 0.04*40= 1.6 g m Koh = 4.48 g
Đúng 1
Bình luận (0)
cho 23,6g hỗn hợp gồm NAOH và CU(OH)2 tác dụng vừa đủ với dd HCL thu được 32,85g các muối clorua. tính khối lượng mỗi hidroxit trong hỗn hợp
Gọi nNaOH = a (mol); nCu(OH)2 = b (mol)
=> 40a + 98b = 23,6 (1)
PTHH:
NaOH + HCl -> NaCl + H2O
a ---> a ---> a
Cu(OH)2 + 2HCl -> CuCl2 + 2H2O
b ---> 2b ---> b
=> 58,5a + 135b = 32,85 (2)
Từ (1)(2) => a = 0,1 (mol); b = 0,2 (mol)
mNaOH = 0,1 . 40 = 4 (g)
mCu(OH)2 = 23,6 - 4 = 19,6 (g)
Đúng 4
Bình luận (0)
Gọi a (mol) và b (mol) lần lượt là số mol của NaOH và Cu(OH)2 trong hỗn hợp ban đầu.
Ta có: 40a+98b=23,6 (1).
Lại có: 58,5a+135b=32,85 (2) (muối clorua gồm NaCl và CuCl2).
Giải hệ phương trình gồm (1) và (2), ta suy ra a=0,1 (mol) và b=0,2 (mol).
Khối lượng mỗi hidroxit trong hỗn hợp ban đầu là:
mNaOH=0,1.40=4 (g).
m\(Cu\left(OH\right)_2\)=0,2.98=19,6 (g).
Đúng 0
Bình luận (0)
Cho 3,04 gam hỗn hợp NaOH và KOH tác dụng với dung dịch axit HCl thu được 4,15 gam hỗn hợp muối clorua. Khối lượng hidroxit trong hỗn hợp là
A. 1,17 g và 2,98 g
B. 1,12 g và 1,6 g
C. 1,12 g và 1,92 g
D. 0,8 g và 2,24 g
Gọi số mol của NaOH và KOH lần lượt là x và y (mol)
PTHH:
NaOH + HCl → NaCl + H2O
x x (mol)
KOH + HCl → KCl + H2O
y y (mol)
\(\left\{{}\begin{matrix}\text{mhh=40x+56y=3,04}\\\text{mmuối=58,5x +74,5y=4,15}\end{matrix}\right.\)⇒\(\left\{{}\begin{matrix}\text{x=0,02}\\\text{y=0,04}\end{matrix}\right.\)
⇒ mNaOH = 40. 0,02= 0,8 (g)
mKOH = 56.0,04= 2,24 (g)
Đúng 0
Bình luận (0)
Cho 6,08g hỗn hợp gồm Natri Hidroxit(NaOH) và Kali Hidroxit(KOH) tác dụng vừa đủ với HCl thu được 8,3g hỗn hợp các muối
a)Tính mAxit đã pứ
b)Tính m từng muối sau pứ
Ta có
NaOH + HCl \(\rightarrow\) NaCl + H2O
x..............x.............x.........x
KOH + HCl \(\rightarrow\) KCl + H2O
y.............y...........y.........y
=> \(\left\{{}\begin{matrix}40x+56y=6,08\\58,5x+74,5y=8,3\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,04\\y=0,08\end{matrix}\right.\)
=> mHCl = ( 0,04 + 0,08 ) . 36,5 = 4,38 ( gam )
=> mNaCl = 58,5 . 0,04 = 2,34 ( gam )
=> mKOH = 6,08 - 2,34 = 3,74 ( gam )
Đúng 1
Bình luận (0)
Cho 6,08g hỗn hợp gồm Natri Hidroxit(NaOH) và Kali Hidroxit(KOH) tác dụng vừa đủ với HCl thu được 8,3g hỗn hợp các muối
a)Tính mAxit đã pứ
b)Tính m từng muối sau pứ
Gọi số mol của NaOH là x, số mol của KOH là y ta có PTHH:
NaOH + HCl --------> NaCl + H2O
x x
KOH + HCl --------> KCl + H2O
y y
Theo đề ra, ta có: 40x+56y=6,08g
58,5x+74,5y=8,3g
=> x=0,04mol y=0,08mol
nHCl=0,04+0,08=0,12mol
a)mHCl=0,12.36,5=4,38g
b)mNaCl=0,04.58,5=2,34g
mKCl=0,08.74,5=5,96g
Đúng 0
Bình luận (0)
Cho 3,04 gam hỗn hợp NaOH và KOH tác dụng với dung dịch axit HCl thu được 4,15 gam hỗn hợp muối clorua. Khối lượng hidroxit trong hỗn hợp là:
A. 1,17 g và 2,98 g
B. 1,12 g và 1,6 g
C. 1,12 g và 1,92 g
D. 0,8 g và 2,24 g
Đáp án D.
NaOH + HCl → NaCl + H2O
x(mol) x(mol)
KOH + HCl → KCl + H2O
y(mol) y(mol)
gọi x, y lần lượt là số mol NaOH và KOH
theo bài ra ta có hệ pt
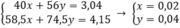
mNaOH = 0,02.40 = 0,8 (g)
mKOH = 0,04.56 = 2,24 (g)
Đúng 0
Bình luận (0)
Cho 3,04 hỗn hợp NaOH,KOH tác dụng dd HCl thu đc 4,15g muối clorua .Tính %khối lượng mỗi chất trong hỗn hợp ban đầu
PT: \(NaOH+HCl\rightarrow NaCl+H_2O\)
\(KOH+HCl\rightarrow KCl+H_2O\)
Gọi: \(\left\{{}\begin{matrix}n_{NaOH}=x\left(mol\right)\\n_{KOH}=y\left(mol\right)\end{matrix}\right.\) ⇒ 40x + 56y = 3,04 (1)
Theo PT: \(\left\{{}\begin{matrix}n_{NaCl}=n_{NaOH}=x\left(mol\right)\\n_{KCl}=n_{KOH}=y\left(mol\right)\end{matrix}\right.\) ⇒ 58,5x + 74,5y = 4,15 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,04\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{NaOH}=\dfrac{0,02.40}{3,04}.100\%\approx26,3\%\\\%m_{KOH}\approx73,7\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
PTHH :
\(NaOH+HCl\rightarrow NaCl+H_2O\)
x x
\(KOH+HCl\rightarrow KCl+H_2O\)
y y
\(\left\{{}\begin{matrix}40x+56y=3,04\\58,5x+74,5=4,15\end{matrix}\right.\)
\(\Rightarrow x=0,02;y=0,04\)
\(\%m_{NaOH}=\dfrac{0,02.40}{2,04}.100\%\approx26,32\%\%\)
\(\%m_{KOH}=100\%-26,32\%=73,68\%\)
Đúng 1
Bình luận (0)
Cho 3,04 gam hỗn hợp NaOH và KOH tác dụng vừa đủ với dung dịch HCl thu được 4,15g các muối clorua
Tính khối lượng của mỗi chất trong hỗn hợp ban đầu
Gọi $n_{NaOH} = a(mol) ; n_{KOH} = b(mol)$
Suy ra : $40a + 56b = 3,04(1)$
$NaOH + HCl \to NaCl + H_2O$
$KOH + HCl \to KCl + H_2O$
Theo PTHH, ta có :
$m_{muối} = 58,5a + 74,5b = 4,15(2)$
Từ (1)(2) suy ra a = 0,02 ; b = 0,04
$m_{NaOH} = 0,02.40 = 0,8(gam)$
$m_{KOH} = 0,04.56 = 2,24(gam)$
Đúng 3
Bình luận (2)
Đặt \(\left\{{}\begin{matrix}n_{NaOH}=a\left(mol\right)\\n_{KOH}=b\left(mol\right)\end{matrix}\right.\)
\(PTHH:NaOH+HCl\rightarrow NaCl+H_2O\\ PTHH:KOH+HCl\rightarrow KCl+H_2O\)
Theo đề bài ta có hpt:
\(\left\{{}\begin{matrix}40a+56b=3,04\\58,5a+74,5b=4,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,02\\b=0,04\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}m_{NaOH}=0,8\left(g\right)\\m_{KOH}=2,24\left(g\right)\end{matrix}\right.\)
Đúng 4
Bình luận (2)
Cho m gam hỗn hợp Al và Fe tác dụng vừa đủ với dd HCl 2M, thu đc dd muối A và 1,456lits H2 ở đktc. Mặt khác cho lượng hỗn hợp trên tác dụng với dd NaOH dư, thu đc 1,12 g chất rắn không tan.
a) tính khối lượng và% khối lượng mỗi chất trong hỗn hợp nói trên
b) tính khối lượng muối thu đc trong ddA
a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ 2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
Cho hỗn hợp tác dụng với NaOH, chất rắn không tan là Fe
=> mFe= 1,12 (g) \(\Rightarrow n_{Fe}=0,02\left(mol\right)\)
Ta có: \(n_{H_2\left(2\right)}=n_{Fe}=0,02\left(mol\right)\)
=> \(n_{H_2\left(1\right)}=\Sigma n_{H_2}-n_{H_2\left(2\right)}=0,065-0,02=0,045\left(mol\right)\)
\(\Rightarrow n_{Al}=\dfrac{2}{3}n_{H_2\left(1\right)}=0,03\left(mol\right)\)
\(\Rightarrow m_{Al}=0,03.27=0,81\left(g\right)\)
\(\Rightarrow\%m_{Al}=41,97\%,\%m_{Fe}=58,03\%\)
b) \(m_{FeCl_2}=0,02.127=2,54\left(g\right)\\ m_{AlCl_3}=0,03.133,5=4,005\left(g\right)\)
Đúng 0
Bình luận (0)





























