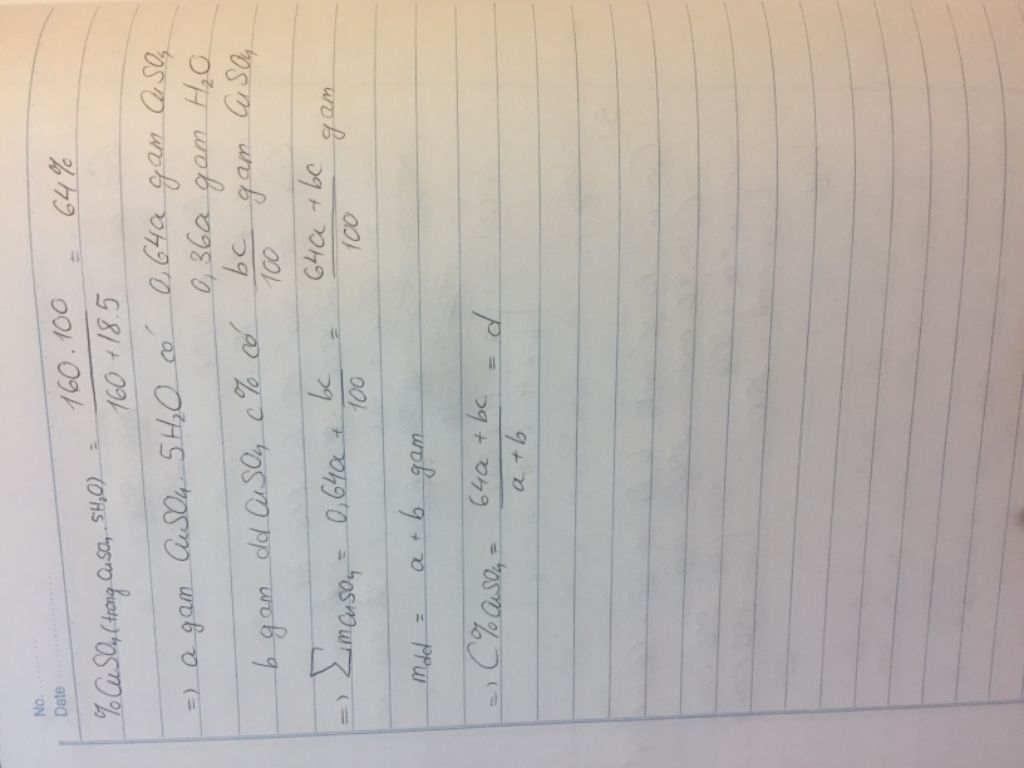hòa tan a gam tinh thể cuso4 5h2o vào b gam dung dịch cuso4 c% thu được dung dịch cu so4 d%.lập biểu thức a,b,c,d

Những câu hỏi liên quan
hòa tan a gam tinh thể cuso4 5h2o vào b gam dung dịch cuso4 c% thu được dung dịch cu so4 d%.lập biểu thức a,b,c,d
a)
hòa tan 6g CuSO4 vào nước thì được dung dịch CuSO4 15%.tính thể tích dung dịch biết D dung dịch CuSO4 = 1,15 g/ml
b) hòa tan 6,9g Na vào 150g nước thì thu đc dung dịch bazo kiềm . nồng độ phần trăm của dung dịch này là :)
c) hòa tan 75 g tinh thể CuSO4 ngậm 5H2O được 900ml dung dịch H2SO4. Tính nồng đôh mol của dung dịch này
Tính C% của dung dịch thu được khi hòa tan 25 gam CuSO4 .5H2O vào 375 gam nước
Ta có: \(n_{CuSO_4}=n_{CuSO_4.5H_2O}=\dfrac{25}{250}=0,1\left(mol\right)\)
m dd sau hòa tan = 25 + 375 = 400 (g)
\(\Rightarrow C\%_{CuSO_4}=\dfrac{0,1.160}{400}.100\%=4\%\)
Đúng 1
Bình luận (0)
Hòa tan 75g tinh thể CUSO4 .5H2O vào thu được 900 ml dung dịch Cuso4 .Tính CM dung dịch này
\(n_{CuSO_4}=n_{CuSO_4.5H_2O}=\dfrac{75}{250}=0,3\left(mol\right)\\ \rightarrow C_{M\left(CuSO_4\right)}=\dfrac{0,3}{0,9}=\dfrac{1}{3}M\)
Đúng 1
Bình luận (0)
bài toán tính nồng độ%
a) tính nồng độ phần trăm của dung dịch natri clorua khi hòa tan 20 gam muối natri clorua vào 180 gam nước
b) hòa tan 16 gam CuSO4 vào nước thu được dung dịch Cu SO4 20%. Hãy tính khối lượng dung dịch thu được và khối lượng nước cần dùng ?
a)
Khối lượng của dung dịch:
\(m_{dd}=m_{ct}+m_{dm}=20+180=200\left(g\right)\)
Nồng độ phần trăm của dung dịch:
\(C\%=\dfrac{m_{ct}}{m_{dd}}.100\%=\dfrac{20}{200}.100\%=10\%\)
b) đề sai nha bạn
Đúng 1
Bình luận (0)
Tính khối lượng tinh thể CuSO4.5H2O cần dùng hòa tan hoàn toàn vào 400 gam dung dịch CuSO4 2% để thu được dung dịch CuSO4 1M ( D = 1,1 g/ml).
Gọi số mol CuSO4.5H2O cần lấy là x (mol) => nCuSO4 = x (mol)
Khối lượng CuSO4 2% có trong 400 gam dung dịch là:
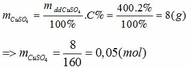
Tổng số mol CuSO4 sau khi hòa tan là: x + 0,05 (mol)
=> thể tích dung dịch sau khi hòa tan:

Từ (1) và (2)
=> (x+ 0,05).1000
=> 1100x + 55 = 160x + 400
=> 850x = 345
=> x ≈0, 406 (mol)
=> mCuSO4.5H2O = 0,406.250 = 101,47 (g)
Đúng 1
Bình luận (0)
khi làm lạnh 232,765 gam dung dịch bão hòa CuSO4 từ 80 độ C xuống 12 độ C thì có bao nhiêu gam tinh thể CuSO4 .5H2O tánh ra khỏi dung dịch biết độ tan của CuSO4 ở 80 đọ C và 12 đọ C lần lượt là 83,8 và 32 gam
\(m_{H_2O}=\dfrac{232,765}{83,8+100}.100=126,64\left(g\right)\\ m_{CuSO_4\left(tách.ra\right)}=\dfrac{126,64}{100}.\left(83,8-32\right)=65,6\left(g\right)\\ \Rightarrow m_{CuSO_4.5H_2O\left(tách.ra\right)}=\dfrac{65,6}{160}.250=102,5\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn a mol cuo bằng một lượng vừa đủ dung dịch h2so4 10% đun nóng , thu được dung dịch x . làm lạnh x đến 10c thì có 1,472 gam tinh thể cuso4 . 5h2o tách ra . biệt ở 10c , cứ 100 gam h2o hòa tan tối đa 17,4 gam cuso. tìm giá trị của a.
Hòa tan a gam tinh thể CuSO4.5H2O vào 250 gam dung dịch CuSO4 4%, thu được dung dịch mới có nồng độ 17,846%. Tìm a.
Giả sử có x mol CuSO4.5H2O
=> \(n_{CuSO_4\left(thêm\right)}=x\left(mol\right)\)
mdd sau khi hòa tan = 250 + 250x (g)
\(m_{CuSO_4\left(bd\right)}=\dfrac{250.4}{100}=10\left(g\right)\)
mCuSO4 (sau khi hòa tan) = 10 + 160x (g)
Có: \(C\%_{dd.sau.khi.hòa.tan}=\dfrac{10+160x}{250+250x}.100\%=17,846\%\)
=> x = 0,3 (mol)
=> a = 0,3.250 = 75 (g)
Đúng 2
Bình luận (0)