Đốt cháy hoàn toàn ankan A thu được 8,96 lít khí CO2 ( đktc ) và 9 gam nước. Tìm công thức phân tử của A. Viết công thức cấu tạo của A và tên gọi

Những câu hỏi liên quan
Bài 3: Đốt cháy hoàn toàn 6,72 lít (đktc) một hiđrôcacbon A bằng không khí. Sau phản ứng thu được 26,4 gam CO2 và 5,4 gam nước.
a) Viết phương trình phản ứng
b) Tìm công thức phân tử, viết công thức cấu tạo, gọi tên hiđrôcacbon A.
c) Tính thể tích không khí cần dùng (đktc). Biết không khí đã dùng dư 20% so với lượng phản ứng.
a) 2CxHy + \(\dfrac{4x+y}{2}\)O2 --to--> 2xCO2 + yH2O
b) \(n_A=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\)
=> nC = 0,6 (mol)
Số nguyên tử C = \(\dfrac{0,6}{0,3}=2\) (nguyên tử)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
=> nH = 0,6 (mol)
Số nguyên tử H = \(\dfrac{0,6}{0,3}=2\) (nguyên tử)
=> CTPT: C2H2 (axetilen)
CTCT: \(CH\equiv CH\)
c)
PTHH: 2C2H2 + 5O2 --to--> 4CO2 + 2H2O
0,3--->0,75
=> VO2(lý thuyết) = 0,75.22,4 = 16,8 (l)
=> Vkk(lý thuyết) = 16,8.5 = 84 (l)
=> \(V_{kk\left(thực.tế\right)}=\dfrac{84.120}{100}=100,8\left(l\right)\)
Đúng 4
Bình luận (0)
Bài 1: Đốt cháy hoàn toàn 5,6 gam một anken sau khi phản ứng hoàn toàn thì thu được 8,96 lít khí CO2 (đktc). A. Xác định công thức phân tử của anken. B. Viết đồng phân có thể có và gọi tên của anken đó.
nCO2 = 0,4 mol
CnH2n + \(\dfrac{3n}{2}\)O2 \(\underrightarrow{t^o}\) nCO2 + nH2O
\(\dfrac{0,4}{n}\) .0,4
ta có : MCnH2n = \(\dfrac{5,6n}{0,4}\) = 14n
↔ n=1(loại)
do n≥ 2
Đúng 0
Bình luận (1)
Đốt cháy hiđrocacbon A thu được 8,96 lít CO2 (đktc) và 10,8 gam H2O. Tỉ khối của A so với khí hiđro là 15. Tìm công thức phân tử (CTPT) và viết CT cấu tạo của A.
Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2.\dfrac{10,8}{18}=1,2\left(mol\right)\)
\(M_A=15.2=30\left(\dfrac{g}{mol}\right)\)
CTPT của A có dạng CxHy
=> x : y = 0,4 : 1,2 = 1 : 3
=> (CH3)n = 30
=> n = 2
CTPT: C2H6
CTCT: CH3-CH3
Đúng 1
Bình luận (0)
Bài 1: Đốt cháy hoàn toàn 5,6 gam một anken sau khi phản ứng hoàn toàn thì thu được 8,96 lít khí CO2 (đktc). a. Xác định công thức phân tử của anken. b. Viết đồng phân có thể có và gọi tên của anken đó. Bài 2: Cho 2,8g ankin A tác dụng hết với dd AgNO3/NH; dư thấy tạo ra 10,29g kết tủa. a. Xác định CTCT và gọi tên A. b. Tính thể tích dd AGNO3 0,5M cần dùng
Đốt cháy hoàn toàn 1,12 lít hỗn hợp khí X gồm ankin A và hiđrocacbon B thu được 2,912 lít CO2 và 2,52 gam H2O. Xác định công thức phân tử, viết công thức cấu tạo và gọi tên A, B. Biết rằng các thể tích khí đo ở điều kiện tiêu chuẩn
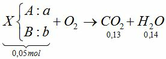
Đốt cháy ankin => nCO2 > nH2O mà theo bài ra nCO2 < nH2O
=> B là ankan nCO2 < nH2O
Nhận xét:
Đốt ankin: – nankin = nH2O – nCO2
Đốt ankan: nankan = nH2O – nCO2
=> b – a = 0,01 và b + a = 0,05
=> a = 0,02 và b = 0,03
=> số C trung bình = 2,6 và số H trung bình = 5,6
TH1: số C trong ankin < 2,6 => A là C2H2: 0,02 và B: 0,03
=> B: 44 (C3H8)
TH2: số C trong ankan < 2,6 => A : 0,02 và CH4: 0,03
=> A: 68 (C5H8) loại do hh khí
TH3: số C trong ankan < 2,6 => A: 0,02 và C2H6: 0,03
=> A: 47 (lẻ) => loại
Vậy A là C2H2 (axetilen/ etin) và B là C3H8 (propan)
Đúng 0
Bình luận (0)
Khi đốt cháy hoàn toàn hỗn hợp 2 ankan là đồng đẳng kế tiếp thu được 7,84 lít khí CO2 (đktc) và 9 gam H2O. Công thức phân tử của 2 ankan là A. CH4 và C2H6 B. C2H6 và C3H8 C. C3H8 và C4H10 D. C4H10 và C5H12
Đọc tiếp
Khi đốt cháy hoàn toàn hỗn hợp 2 ankan là đồng đẳng kế tiếp thu được 7,84 lít khí CO2 (đktc) và 9 gam H2O. Công thức phân tử của 2 ankan là
A. CH4 và C2H6
B. C2H6 và C3H8
C. C3H8 và C4H10
D. C4H10 và C5H12
Hỗn hợp khí A chứa một ankan và một anken, Khối lượng hỗn hợp A là 9 gam và thể tích là 8,96 lít. Đốt cháy hoàn toàn A, thu được 13,44 lít C O 2 . Các thể tích được đo ở đktc.
Xác định công thức phân tử và phần trăm thể tích từng chất trong A.
Khối lượng trung bình của 1 mol A :
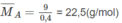
Trong hỗn hợp A phải có chất có M < 22,5 ; chất đó chỉ có thể là C H 4 .
Sau đó giải hệ 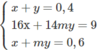
Ta tìm được m = 3; x = 0,3; y = 0,1.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 5,6 gam chất hữu cơ A thu được 8,96 lít khí CO2 (đktc) và 7,2g H2O. a) Tìm công thức đơn giản nhất của A? b) Tìm công thức phân tử của A? (Biết tỉ khối hơi của A so với hiđro bằng 28).
\(n_C=n_{CO_2}=0,4\left(mol\right);n_H=2.n_{H_2O}=2.0,4=0,8\left(mol\right)\\ m_C+m_H=0,4.12+0,8.1=5,6=m_A\)
=> A là hidrocacbon: A chỉ có 2 nguyên tố là C và H
\(a,n_C:n_H=0,4:0,8=1:2\\ \Rightarrow A.có.CTĐG:CH_2\\ b,Đặt.CTTQ:\left(CH_2\right)_a\left(a:nguyên,dương\right)\\ M_{\left(CH_2\right)_a}=28\\ \Leftrightarrow14a=28\\ \Leftrightarrow a=2\\ \Rightarrow CTPT:C_2H_4\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ X thu được 11,2 lít CO2 (đktc) và 10,8 gam nước. Biết rằng 7,2 gam X có số mol bằng số mol của 3,2 gam khí oxi.
a) Xác định công thức phân tử của X.
b) Viết tất cả các công thức cấu tạo có thể có của X.
Đọc tiếp
Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ X thu được 11,2 lít CO2 (đktc) và 10,8 gam nước. Biết rằng 7,2 gam X có số mol bằng số mol của 3,2 gam khí oxi.
a) Xác định công thức phân tử của X.
b) Viết tất cả các công thức cấu tạo có thể có của X.
\(n_C=n_{CO_2}=0,5\left(mol\right);n_H=2.n_{H_2O}=2.\dfrac{10,8}{18}=1,2\left(mol\right)\\ m_C+m_H=0,5.12+1,2.1=7,7,2\\ \Rightarrow X.ko.có.oxi\left(O\right)\\ \Rightarrow CTTQ:C_xH_y\left(x,y:nguyên,dương\right)\\ x:y=n_C:n_H=0,5:1,2=5:12\\a, \Rightarrow x=5;y=12\Rightarrow CTPT.X:C_5H_{12}\\ b,CH_3-CH_2-CH_2-CH_2-CH_3\\ CH_3-CH\left(CH_3\right)-CH_2-CH_3\\ CH_3-C\left(CH_3\right)_2-CH_3\)
Đúng 0
Bình luận (0)
đốt cháy 5,8 gam một hợp chất A thu được 8,96 lít khí H2 (dktc) và 9 gam nước .Tìm công thức phân tử của A,biết 1 phân tử A nặng 58 đvc.Viết các công thức cấu tạo có thể có ở A.Phản ứng đặc trưng của A là gì ?.viết PTHH?
Sửa đề: 8,96 (l) H2 → 8,96 (l) CO2.
Ta có: \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{9}{18}=0,5\left(mol\right)\Rightarrow n_H=0,5.2=1\left(mol\right)\)
⇒ mC + mH = 0,4.12 + 1.1 = 5,8 (g) = mA
→ A chỉ có C và H.
Gọi CTPT của A là CxHy.
⇒ x:y = 0,4:1 = 2:5
→ A có CTPT dạng (C2H5)n
Mà: MA = 58 (g/mol)
\(\Rightarrow n=\dfrac{58}{12.2+5}=2\)
Vậy: A là C4H10
CTCT: \(CH_3-CH_2-CH_2-CH_3\)
\(CH_3-CH\left(CH_3\right)-CH_3\)
- Pư đặc trưng của A là pư thế halogen.
PT: \(C_4H_{10}+Cl_2\underrightarrow{as}C_4H_9Cl+HCl\)
Đúng 1
Bình luận (1)


















