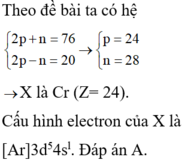Nguyên tử X có tổng số hạt là 34, số hạt không mang điện chiếm 35.3%.Viết cấu hình e của nguyên tử X

Những câu hỏi liên quan
Nguyên tử của nguyên tố X có tổng số hạt p,n,e là 34. Trong hạt nhân , số hạt không mang điện nhiều hơn số hạt mang điện là 1 .
a) viết kí hiệu của nguyên tử x
b) viết cấu hình và cho biết x thuộc phi kim , kim loại hay khí hiếm.
Xem chi tiết
Gọi :
Số hạt proton = Số hạt electron = p
Số hạt notron = n
Ta có :
- Tổng số hạt :2p + n = 34 (1)
- Trong hạt nhân(gồm hai loại hạt : proton và notron) ,hạt không mang điện nhiều hơn mang điện là 1 : n - p = 1(2)
Từ (1)(2) suy ra p = 11 ; n = 12
a) Kí hiệu : Na ( Natri)
b) Cấu hình electron :1s22s22p63s1
X có 1 electron ở lớp ngoài cùng (3s1) nên X là kim loại.
Đúng 0
Bình luận (0)
Nguyên tử X có tổng số hạt là 34, số hạt không mang điện nhiều hơn số hạt mang điện dương là 1. Xác định cấu tạo hạt (tìm số e, số p, số n), viết kí hiệu nguyên tử X.
Theo đề bài ta có: p+e+n=34
\(\Rightarrow2p+n=34\)
Mà \(n=1+p\)
\(\Rightarrow3p+1=34\Rightarrow p=11\)
\(\Rightarrow\left\{{}\begin{matrix}e=p=11\\n=12\end{matrix}\right.\)
Vậy X là Na
Đúng 2
Bình luận (0)
Nguyên tố X có tổng số hạt cơ bản là 34, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10
a) Hãy viết kí hiệu nguyên tử của ngtố X
b) Việt cấu hình electron nguyên tử, cấu hình electron theo orbital của X
c) Từ cấu hình electron, dự đoán tính chất hoá học
d) Xác đinh vị trí của X trong bảng tuần hoàn
a, Ta có: P + N + E = 34
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 34 (1)
Theo đề, số hạt mang điện nhiều hơn số hạt không mang điện là 10.
⇒ 2P - N = 10 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=11=Z\\N=12\end{matrix}\right.\) ⇒ A = 11 + 12 = 23
→ KH: \(^{23}_{11}X\)
b, Cấu hình e: 1s22s22p63s1
Cấu hình e theo orbital:
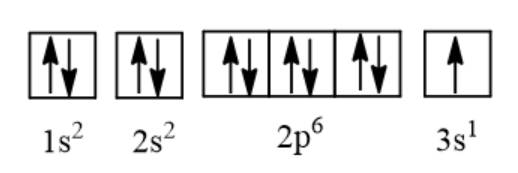
c, X có 1 e hóa trị → tính kim loại
d, - Z = 11 → ô số 11
- Có 3 lớp e → chu kỳ 3
- e cuối cùng phân bố ở phân lớp s, có 1 e hóa trị → nhóm IA
Vậy: X thuộc ô số 11, chu kỳ 3, nhóm IA
Đúng 0
Bình luận (0)
Nguyên tử X có tổng các hạt là 52 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt . Hãy xác định số p,n,e , viết kí hiệu nguyên tử , viết cấu hình electron của X
\(\left\{{}\begin{matrix}2Z+N=52\\2Z-N=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z=17\\N=18\end{matrix}\right.\)
p=e=17
n=18
Cấu hình là: \(1s^22s^22p^63s^23p^5\)
Đúng 1
Bình luận (0)
Nguyễn Lê Phước Thịnh CTV : bạn có thế làm hẳn ra 1 tí nữa được không chứ tắt quá mình không hiểuu =))
Đúng 0
Bình luận (0)
Nguyên tử X có tổng các hạt mang điện và không mang điện là 86 và hiệu các hạt mang điện và không mang điện là 26. a. Tìm số e, số p, số n và số khối của nguyên tử X b. X là nguyên tố nào c. Viết kí hiệu nguyên tử của X d. Viết cấu hình electron của X và của X2+
Một nguyên tử X có tổng số hạt p,n,e là 34. Số hạt mang điện nhiều hơn số hạt không mang điện là 10. Tìm tên nguyên tử X.Vẽ sơ đồ cấu tạo của nguyên tử X và ion được tạo ra từ nguyên tử X
Theo đề ta có: p+e+n=34 →2p+n=34 (vì p=e) (1)
Mặt khác ta lại có:(p+e)-n=10 →2p-n=10 (vì p=e) (2)
Công (1) và (2) vế theo vế có
4p=44 →p=e=11
nguyên tử X là nguyên tử nguyên tố Natri (Na)
Đúng 2
Bình luận (0)
Ta có: p + e + n = 34.
Vì số p = số e nên: 2p + n = 34 (1)
Mà (p + e) - n = 10 \(\Rightarrow\)2p - n = 10 (2)
Từ (1) và (2) \(\Rightarrow\) 4p = 44 \(\Rightarrow\) p = e = 11
Vậy: X là natri, kí hiệu: Na
Sơ đồ cấu tạo nguyên tử:
Đúng 0
Bình luận (0)
Nguyên tử nguyên tố X có tổng số hạt (p, n, e) là 76, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 20 hạt. Cấu hình electron nguyên tử của nguyên tố X là A. [Ar] 3d54s1. B. [Ar] 3d44s2. C. [Ar] 4s13d5. D. [Ar] 4s23d4.
Đọc tiếp
Nguyên tử nguyên tố X có tổng số hạt (p, n, e) là 76, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 20 hạt. Cấu hình electron nguyên tử của nguyên tố X là
A. [Ar] 3d54s1.
B. [Ar] 3d44s2.
C. [Ar] 4s13d5.
D. [Ar] 4s23d4.
Đáp án A
Theo đề bài ta có hệ
2
p
+
n
=
76
2
p
-
n
=
20
→
p
=
4
n
=
28
→ X là Cr (Z= 24). Cấu hình electron của X là [Ar]3d54s1. Đáp án A.
Đúng 0
Bình luận (0)
Nguyên tử nguyên tố X có tổng số hạt (p, n, e) là 76, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 20 hạt. Cấu hình electron nguyên tử của nguyên tố X là A. [Ar] 3d54s1. B. [Ar] 3d44s2. C. [Ar] 4s13d5. D. [Ar] 4s23d4
Đọc tiếp
Nguyên tử nguyên tố X có tổng số hạt (p, n, e) là 76, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 20 hạt. Cấu hình electron nguyên tử của nguyên tố X là
A. [Ar] 3d54s1.
B. [Ar] 3d44s2.
C. [Ar] 4s13d5.
D. [Ar] 4s23d4
Đáp án A
Theo đề bài ta có hệ 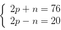 →
→ ![]()
→ X là Cr (Z= 24). Cấu hình electron của X là [Ar]3d54s1. Đáp án A.
Đúng 0
Bình luận (0)
Nguyên tử nguyên tố X có tổng số hạt (p, n, e) là 76, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 20 hạt. Cấu hình electron nguyên tử của nguyên tố X là A. [Ar]3d54s1 B. [Ar]3d44s2 C. [Ar]4s13d5 D. [Ar]4s23d4
Đọc tiếp
Nguyên tử nguyên tố X có tổng số hạt (p, n, e) là 76, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 20 hạt. Cấu hình electron nguyên tử của nguyên tố X là
A. [Ar]3d54s1
B. [Ar]3d44s2
C. [Ar]4s13d5
D. [Ar]4s23d4