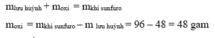Bài 3: Người ta đốt cháy lưu huỳnh trong bình chứa 15 gam oxi. Sau phản ứng thu được 19,2 gam khí sunfurơ (SO2)
a) Tính số gam lưu huỳnh đã cháy
b) Tính số gam oxi còn dư sau phản ứng cháy
Người ta đốt cháy lưu huỳnh trong bình chứa 15 gam oxi. Sau phản ứng thu được 19,2 gam khí sunfurơ (SO2)
a. Tính số gam lưu huỳnh đã cháy
b. Tính số gam oxi còn dư sau phản ứng cháy
Bài làm
S + O2 ---to---> SO2
a) nSO2 = 19,2 : ( 32 + 32 ) = 0,3 ( mol )
Theo phương trình nS = nSO2 = 0,3 mol
=> mS = 0,3 . 32 = 9,6 ( g )
b) nO2 = 15 : 32 = 0,46875 ( mol )
Xét tỉ lệ: \(\frac{n_{O2}}{1}=0,46875>\frac{n_S}{1}=0,3\)
=> O2 dư, S hết.
=> Bài toán tính theo S.
Theo phương trình:
nO2 = nS = 0,3 ( mol )
=> nO2 sau phản ứng = nO2 ban đầu - nO2 vừa tìm được
Hay nO2 sau phản ứng = 0,46875 - 0,3 = 0,16875 ( mol )
=> mO2 sau phản ứng = 0,16875 . 32 = 5,4 ( g )
# Học tốt #
a) \(PT:S+O_2\rightarrow SO_2\)
\(n_{SO_2}=\frac{m}{M}=\frac{19,2}{64}=0,3\)
\(\)Theo pt: \(n_S=n_{SO_2}=0,3\)
\(\Rightarrow m_s=0,3.32=9,6\)
b, Ta có: \(n_{O_2}=\frac{m}{M}=\frac{15}{32}=0,46875\)
Theo pt: \(n_{O_{2\left(pư\right)}}=n_S=0,3\)
\(\Rightarrow n_{O_{2\left(dư\right)}}=n_{O_2}-n_{O_{2\left(pư\right)}}=0,4875-0,3=0,1875\)
\(\Rightarrow m_{O_{2\left(dư\right)}}=n_{O_{2\left(dư\right)}}.M_{O_2}=0,1875.32=6\)
nO=\(\frac{15}{32}\)= 0,4
nSO2= \(\frac{19,2}{64}=0,3\)
PTHH : S + O2 = SO2
Đề bài 0,4 0,3
Tỉ lệ 0,3 0,3
a, mS = 0,3.32=9,6g
Số gam õi còn dư là 0,4 - 0,3 = 0,1 gam
người ta đốt cháy lưu huỳnh trong bình chứa 15g oxi.. sau pư thu đc 19,2g khí sunfurơ (SO2)
a) Tính số gam lưu huỳnh đã cháy
b) Tính số gam oxi còn dư sau phản ứng cháy
b)
\(n_{O_2}=\dfrac{15}{32}=0.46875\left(mol\right)\)
\(n_{SO_2}=\dfrac{19.2}{64}=0.3\left(mol\right)\)
\(S+O_2\underrightarrow{t^0}SO_2\)
\(0.3...0.3....0.3\)
\(m_S=0.3\cdot32=9.6\left(g\right)\)
\(m_{O_2\left(dư\right)}=\left(0.46875-0.3\right)\cdot32=5.4\left(g\right)\)
Bài 5: Người ta đốt cháy lưu huỳnh trong bình chứa 15 gam oxi. Sau phản ứng thu được 19,2 gam khí sunfurơ (SO2)
a. Tính số gam lưu huỳnh đã cháy
b. Tính số gam oxi còn dư sau phản ứng cháy
a) \(nSO_2=\frac{m}{M}=\frac{19.2}{32+16,2}=0,3\left(mol\right),nO_2=0,46875\left(mol\right)\)
PTHH : \(S+O_2\rightarrow SO_2\)
\(\Rightarrow O_2\)dư S , hết
Theo PTHH : \(n_{O_2pu}+n_{Spu}=n_{SO2}\)
\(\Rightarrow nS=n_{SO2}=0,3\left(mol\right)=Ms=9,6\left(g\right)\)
b) \(n_{O2}\)phản ứng \(=n_{SO2}=0,3\left(mol\right)\rightarrow n_{O2_{dư}}=0,46875-0,3=0,16875\)
\(\Rightarrow m_{O2_{dư}}=5,4\left(g\right)\)
Vì số mol của O2 ban đầu đề bài cho là 0,46875 mol, mà số mol O2 phản ứng = nSO2 = 0,3 Cho nên số mol O2 dư = nO2 ban đầu - nO2 phản ứng
a) S+O2--->SO2
a) Ta có
n SO2=19,2/64=0,3(mol)
n O2=15/32=0,46875(mol)
-->O2 dư
Theo pthh
nS=n SO2=0,3(mol)
m S=0,3.32=9,6(g)
b) n O2=n SO2=0,3(mol)
n O2 dư=0,46875-0,3=0,16875(mol)
m O2 dư=0,16875.32=5,4(g)
Pt: S + O2 ------> SO2
0,3. 0,3 0,3
Ta có : nO2= 15/32=0,46875 mol ; nSO2=19,2/64=0,3 mol
A) mS= 0,3 x 32= 9,6g
B) nO2 dư = 0,46875 -0,3=0,16875 => mO2 dư =0,16875 x 32=5,4g
Người ta đốt cháy lưu huỳnh trong bình chứa 15 gam oxi. Sau phản ứng thu được 19,2 gam khí sunfurơ (SO2)
a) Tính số gam lưu huỳnh đã cháy.
b) Tính số gam oxi còn dư sau phản ứng cháy.
Sao tui ko đc GP nhỉ chán vái:https://hoidap247.com/cau-hoi/226802
Người ta đốt cháy lưu huỳnh trong bình chứa 15 gam oxi. Sau phản ứng thu được 19,2 gam khí sunfurơ (SO2)
a) Tính số gam lưu huỳnh đã cháy.
b) Tính số gam oxi còn dư sau phản ứng cháy.
------
a) nO2= 15/32= 0,46875(mol)
nSO2= 19,2/64= 0,3(mol)
PTHH: S + O2 -to-> SO2
0,3<-------0,3<-------0,3(mol)
Ta có: 0,46875/1 > 0,3/1
=> O2 dư. Tính theo nSO2
=> mS= 3,2. 0,3= 9,6(g)
b) mO2(dư)= (0,46875-0,3).32= 5,4(g)
Đốt cháy 3,2 gam lưu huỳnh cháy trong không khí thu được 6,4 gam lưu huỳnh đioxit SO2. Tính khối lượng oxi đã tham gia phản ứng? Biết lưu huỳnh cháy là tham gia phản ứng với khí oxi.
Định luật bảo toàn khối lượng :
\(m_S+m_{O2}=m_{SO2}\)
3,2 + \(m_{O2}\) = 6,4
⇒ \(m_{O2}=6,4-3,2=3,2\left(g\right)\)
Chúc bạn học tốt
\(BTKL: \\ m_S+m_{O_2}=m_{SO_2}\\ 3,2+m_{O_2}=6,4\\ m_{O_2}=6,4-3,2=3,1(g)\)
Lưu huỳnh cháy theo sơ đồ phản ứng sau: Lưu huỳnh + khí oxi → Lưu huỳnh đioxit Nếu đốt cháy 48 gam lưu huỳnh và thu được 96 gam lưu huỳnh đioxit thì khối lượng oxi đã tham gia vào phản ứng là bao nhiêu?
Theo ĐLBT KL, có: mS + mO2 = mSO2
⇒ mO2 = mSO2 - mS = 96 - 48 = 48 (g)
Lưu huỳnh cháy theo sơ đồ phản ứng sau: Lưu huỳnh + khí oxi → Lưu huỳnh đioxit Nếu đốt cháy 48 gam lưu huỳnh và thu được 96 gam lưu huỳnh đioxit thì khối lượng oxi đã tham gia vào phản ứng là bao nhiêu?
Đốt cháy 3,2 gam lưu huỳnh trong bình chứa 1,12 lít khí oxi a) Viết phương trình phản ứng b) chất nào dư sau phản ứng ? dư bao nhiêu gam ? c) tính thể tích khí sinh ra ?
\(n_S=\dfrac{3,2}{32}=0,1\left(mol\right)\\
n_{O_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\\
pthh:S+O_2\underrightarrow{t^o}SO_2\\
LTL:\dfrac{0,1}{1}>\dfrac{0,05}{1}\)
=> S dư
\(n_{S\left(P\text{Ư}\right)}=n_{SO_2}=n_{O_2}=0,05\left(mol\right)\\
m_S=\left(0,1-0,05\right).32=1,6\left(g\right)\\
V_{SO_2}=0,05.22,4=1,12\left(l\right)\)
Bài 1 : Viết PTHH phản ứng cháy của các chất sau trong oxi : H2 , Mg , Cu , S ; Al ; C và P
Bài 2: Cacbon cháy trong bình đựng khí oxi tạo thành khí cacbonic . Viết PTHH và tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau
a. Khi có 6,4 g khí oxi tham gia phản ứng
b. Khi có 0,3 mol cacbon tham gia phản ứng
c. Khi đốt 0,3 mol cacbon trong bình đựng 0,2 mol khí oxi
Bài 3: Khi đốt khí metan ( CH4 ) ; khí axetilen ( C2H2 ) , rượu etylic ( C2H6O ) đều cho sản phẩm là khí cacbonic và hơi nước . Hãy viết PTHH phản ứng cháy của các phản ứng trên
Bài 4: Tính khối lượng oxi cần dùng để đốt cháy hết :
a. 46,5 gam photpho b. 30 gam cacbon
c. 67,5 gam nhôm d. 33,6 lít hidro
Bài 5: Người ta đốt cháy lưu huỳnh trong bình chứ 15g oxi . Sau phản ứng thu được 19,2 gam khí sunfuro ( SO2 )
a. Tính số gam lưu huỳnh đã cháy
b. Tính số gam oxi còn dư sau phản ứng cháy
Bài 6: Một bình phản ứng chứa 33,6 lít khí oxi (đktc) với thể tích này có thể đốt cháy :
a. Bao nhiêu gam cacbon ?
b. Bao nhiêu gam hidro
c. Bao nhiêu gam lưu huỳnh
d. Bao nhiêu gam photpho
Bài 7: Hãy cho biết 3 . 1024 phân tử oxi có thể tích là bao nhiêu lít ?
Bài 8: Tính thể tích oxi (đktc) cần dùng để đốt cháy hoàn toàn 1 kg than đá chứa 96% cacbon và 4% tạp chất không cháy
Bài 9: Đốt cháy 6,2 gam photpho trong bình chứa 6,72 khí lít oxi (đktc) tạo thành điphotpho pentaoxi
a. Chất nào còn dư sau phản ứng , với khối lượng là bao nhiêu ?
b. Tính khối lượng sản phẩm tạo thành
\(1,2H_2+O_2\underrightarrow{t}2H_2O\)
\(2Mg+O_2\underrightarrow{t}2MgO\)
\(2Cu+O_2\underrightarrow{t}2CuO\)
\(S+O_2\underrightarrow{t}SO_2\)
\(4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(C+O_2\underrightarrow{t}CO_2\)
\(4P+5O_2\underrightarrow{t}2P_2O_5\)
\(2,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(a,n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(b,n_C=0,3\left(mol\right)\Rightarrow n_{CO_2}=0,3\left(mol\right)\Rightarrow m_{CO_2}=13,2\left(g\right)\)
c, Vì\(\frac{0,3}{1}>\frac{0,2}{1}\)nên C phản ửng dư, O2 phản ứng hết, Bài toán tính theo O2
\(n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(3,PTHH:CH_4+2O_2\underrightarrow{t}CO_2+2H_2O\)
\(C_2H_2+\frac{5}{2}O_2\underrightarrow{t}2CO_2+H_2O\)
\(C_2H_6O+3O_2\underrightarrow{t}2CO_2+3H_2O\)
\(4,a,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_P=1,5\left(mol\right)\Rightarrow n_{O_2}=1,2\left(mol\right)\Rightarrow m_{O_2}=38,4\left(g\right)\)
\(b,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_C=2,5\left(mol\right)\Rightarrow n_{O_2}=2,5\left(mol\right)\Rightarrow m_{O_2}=80\left(g\right)\)
\(c,PTHH:4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(n_{Al}=2,5\left(mol\right)\Rightarrow n_{O_2}=1,875\left(mol\right)\Rightarrow m_{O_2}=60\left(g\right)\)
\(d,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(TH_1:\left(đktc\right)n_{H_2}=1,5\left(mol\right)\Rightarrow n_{O_2}=0,75\left(mol\right)\Rightarrow m_{O_2}=24\left(g\right)\)
\(TH_2:\left(đkt\right)n_{H_2}=1,4\left(mol\right)\Rightarrow n_{O_2}=0,7\left(mol\right)\Rightarrow m_{O_2}=22,4\left(g\right)\)
\(5,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=0,46875\left(mol\right)\)
\(n_{SO_2}=0,3\left(mol\right)\)
Vì\(0,46875>0,3\left(n_{O_2}>n_{SO_2}\right)\)nên S phản ứng hết, bài toán tính theo S.
\(a,\Rightarrow n_S=n_{SO_2}=0,3\left(mol\right)\Rightarrow m_S=9,6\left(g\right)\)
\(n_{O_2}\left(dư\right)=0,16875\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=5,4\left(g\right)\)
\(6,a,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_C=1,5\left(mol\right)\Rightarrow m_C=18\left(g\right)\)
\(b,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_{H_2}=0,75\left(mol\right)\Rightarrow m_{H_2}=1,5\left(g\right)\)
\(c,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_S=1,5\left(mol\right)\Rightarrow m_S=48\left(g\right)\)
\(d,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_P=1,2\left(mol\right)\Rightarrow m_P=37,2\left(g\right)\)
\(7,n_{O_2}=5\left(mol\right)\Rightarrow V_{O_2}=112\left(l\right)\left(đktc\right)\);\(V_{O_2}=120\left(l\right)\left(đkt\right)\)
\(8,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(m_C=0,96\left(kg\right)\Rightarrow n_C=0,08\left(kmol\right)=80\left(mol\right)\Rightarrow n_{O_2}=80\left(mol\right)\Rightarrow V_{O_2}=1792\left(l\right)\)
\(9,n_p=0,2\left(mol\right);n_{O_2}=0,3\left(mol\right)\)
\(PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
Vì\(\frac{0,2}{4}< \frac{0,3}{5}\)nên P hết O2 dư, bài toán tính theo P.
\(a,n_{O_2}\left(dư\right)=0,05\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=1,6\left(g\right)\)
\(b,n_{P_2O_5}=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=14,2\left(g\right)\)
đủ cả 9 câu bạn nhé,
Lưu huỳnh cháy theo sơ đồ phản ứng sau :
Lưu huỳnh + khí oxi → khí sunfuro
Nếu đốt cháy 48 gam lưu huỳnh và thu được 96 gam khí sunfuro thì khối lượng của oxi tham gia phản ứng là bao nhiêu?
Áp dụng định luật bảo toàn khối lượng, ta có :