Nung nóng thủy ngân ( II ) oxit HgO thì được thủy ngân và oxi . Hãy tính thể tích khí oxi thu được khi nung 54,25g HgO

Những câu hỏi liên quan
Khử 21.7g thủy ngân (ii) oxit (HgO) bằng khí H2 thì số gam thủy ngân thu được là bao nhiêu?
PTHH: HgO + \(H_2\) ---> Hg + \(H_2O\)
0,1 mol 0,1 mol 0,1 mol 0,1 mol
+ Số mol của HgO:
\(n_{HgO}\) = \(\dfrac{m}{M}\) = \(\dfrac{21,7}{217}\) = 0,1 (mol)
+ Số g thủy ngân (Hg) thu được:
\(m_{Hg}\) = n . M = 0,1 . 201 = 20,1 (g)
Vậy: thu được 20,1 g Hg (thủy ngân)
Đúng 1
Bình luận (0)
\(n_{HgO}=\dfrac{m_{HgO}}{M_{HgO}}=\dfrac{21,7}{217}=0,1\left(mol\right)\)
\(HgO+H_2\underrightarrow{t^0}H_2O+Hg\)
Theo PT: 1mol _ 1mol _ 1mol _ 1mol
Theo đề: 0,1 mol _ 0,1 mol _ 0,1 mol _ 0,1 mol
\(m_{Hg}=n_{Hg}.M_{Hg}=0,1.201=20,1\left(g\right)\)
Đúng 0
Bình luận (0)
Ở nhiệt độ cao , thủy ngân oxit HgO bị phân hủy cho thủy ngân Hg và khí O2 theo phản ứng : 2HgO-) 2hg + O2
a)Tính khối lượng oxit thu được nếu có 0,15mol HgO bị phân hủy
2HgO -t--> 2Hg + O2
0,15-------------->0,75 (mol)
=> mO2 = 0,75 . 32 = 24 (g)
Đúng 3
Bình luận (0)
Bài 1: Cho sơ đồ phản ứng phân hủy thủy ngân oxit như sau: HgO ---- Hg + O2a) Tính thể tích khí O2 (đktc) sinh ra khi có 0,1 mol HgO phân hủy.b) Tính khối lượng thủy ngân sinh ra khi có 43,4 gam HgO phân hủy.c) Tính khối lượng thủy ngân oxit đã phân hủy khi có 14,07 gam thủy ngân sinh ra. Bài 2: Lập phương trình hóa học của phản ứng giữa axit clohidric tác dụng với kẽm theo sơ đồ sau: Zn + HCl ---- ZnCl2 + H2Biế...
Đọc tiếp
Bài 1: Cho sơ đồ phản ứng phân hủy thủy ngân oxit như sau:
HgO ----> Hg + O2
a) Tính thể tích khí O2 (đktc) sinh ra khi có 0,1 mol HgO phân hủy.
b) Tính khối lượng thủy ngân sinh ra khi có 43,4 gam HgO phân hủy.
c) Tính khối lượng thủy ngân oxit đã phân hủy khi có 14,07 gam thủy ngân sinh ra.
Bài 2: Lập phương trình hóa học của phản ứng giữa axit clohidric tác dụng với kẽm theo sơ đồ sau:
Zn + HCl ----> ZnCl2 + H2
Biết rằng, sau phản ứng thu được 0,3 mol khí hidro H2, hãy tính:
a) Khối lượng kẽm Zn đã phản ứng.
b) Khối lượng axit clohidric HCl đã phản ứng.
Bài 1:
\(PTHH:2HgO\underrightarrow{Phân.hủy}2Hg+O_2\\ á,Theo.PTHH:n_{O_2}=\dfrac{1}{2}.n_{HgO}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\\ V_{O_2\left(đktc\right)}=n.22,4=0,05.22,4=1,12\left(l\right)\)
\(b,n_{HgO}=\dfrac{m}{M}=\dfrac{43,4}{217}=0,2\left(mol\right)\\ Theo.PTHH:n_{Hg}=n_{HgO}=0,2\left(mol\right)\\ m_{Hg}=n.M=0,2.201=40,2\left(g\right)\)
\(c,n_{Hg}=\dfrac{m}{M}=\dfrac{14,07}{201}=0,07\left(mol\right)\\ Theo.PTHH:n_{HgO}=n_{Hg}=0,07\left(mol\right)\\ m_{HgO}=n.M=0,07.217=15,19\left(g\right)\)
Câu 2:
\(a,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ Theo.PTHH:n_{Zn}=n_{H_2}=0,3\left(mol\right)\\ m_{Zn}=n.M=0,3.65=19,5\left(g\right)\\ b,Theo.PTHH:n_{HCl}=2.n_{Zn}=2.0,3=0,6\left(mol\right)\\ m_{HCl}=n.M=0,6.36,5=21,9\left(g\right)\)
Đúng 2
Bình luận (1)
nung thủy ngân oxit thu được thủy ngân và oxi
viết PTHH và thuộc loại nào
2Hg + O2 → 2HgO
Phản ứng trên thuộc loại phản ứng hóa hợp
Đúng 0
Bình luận (0)
PTHH : 2Hg + O2 → 2HgO
- Đây là phản ứng hóa hợp
Đúng 0
Bình luận (0)
Nung 22,7 g thủy ngân . Tính thể tích oxi ( điều kiện tiêu chuẩn) và khối lượng thủy ngân thu đc
Xem chi tiết
\(n_{Hg}=\dfrac{m}{M}=\dfrac{227}{2006}\left(mol\right)\)
\(PTHH:2Hg+O_2\rightarrow2HgO\)
\(.................\dfrac{227}{2006}.........\dfrac{227}{4012}............\dfrac{227}{2006}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{HgO}=n.M=~24,5\left(g\right)\\V_{O_2}=n.22,4=~1,27\left(l\right)\end{matrix}\right.\)
Vậy ...
Đúng 0
Bình luận (1)
*Nung thủy ngân oxit:
nHgO = m/M = 22,7/217 ≃ 0,1 (mol)
PT:
2HgO --to--> 2Hg + O2
0,1 ----------> 0,1 --> 0,05 (mol)
Từ phương trình ta có:
VO2 = nO2 . 22,4 = 0,05 . 22,4 = 1,12 (l)
mHg = nHg . MHg = 0,1 . 201 = 20,1 (g)
Đúng 0
Bình luận (0)
câu 1 một bình chứa 33,6 lít khí oxi (điều kiện tiêu chuẩn) với thể tích này có thể đốt cháy: a) bao nhiêu game cacbon và tạo ra bao nhiêu lít cacbon dioxit b) bao nhiêu gam lưu huỳnh và tạo ra bao nhiêu lít lưu huỳnh dioxit c) bao nhiêu gam P và tạo ra bao nhiêu gam diphotpho pentaoxitcâu 2 nung thủy ngân oxit thu được thủy ngân và oxit a) viêt phương trình hóa học của phản ứng b) phản úng trên thuộc loại phản ứng nào c) nung 21,7 gam thủy ngân oxit thính thể tích oxi ( điều kiện...
Đọc tiếp
câu 1 một bình chứa 33,6 lít khí oxi (điều kiện tiêu chuẩn) với thể tích này có thể đốt cháy:
a) bao nhiêu game cacbon và tạo ra bao nhiêu lít cacbon dioxit
b) bao nhiêu gam lưu huỳnh và tạo ra bao nhiêu lít lưu huỳnh dioxit
c) bao nhiêu gam P và tạo ra bao nhiêu gam diphotpho pentaoxit
câu 2 nung thủy ngân oxit thu được thủy ngân và oxit
a) viêt phương trình hóa học của phản ứng
b) phản úng trên thuộc loại phản ứng nào
c) nung 21,7 gam thủy ngân oxit thính thể tích oxi ( điều kiện tiêu chuẩn) và khối lượng thủy ngân thu được
câu 3 tính thẻ tích oxi thu được
a) khi phân hủy 9,8 gam kali clorat trong PTN
b) khi điện phân 36 Kg H2O trong công nghiệp
MN ơi giúp mik với mik đang cần gấp thanks trước
câu 1 một bình chứa 33,6 lít khí oxi (điều kiện tiêu chuẩn) với thể tích này có thể đốt cháy:
a) bao nhiêu game cacbon và tạo ra bao nhiêu lít cacbon dioxit
b) bao nhiêu gam lưu huỳnh và tạo ra bao nhiêu lít lưu huỳnh dioxit
c) bao nhiêu gam P và tạo ra bao nhiêu gam diphotpho pentaoxit
Khử 21,7 gam thủy ngân(II) oxit bằng hiđro. Hãy:
a) Tính số gam thủy ngân thu được.
b) Tính số mol và thể tích khí hiđro (đktc) cần dùng.
nHgO = 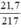 = 0,1 mol.
= 0,1 mol.
Phương trình hóa học của phản ứng khử HgO:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1 .201 = 20,1g.
nH2 = 0,1 mol.
VH2 = 0,1 .22,4 =2,24l.
Đúng 0
Bình luận (0)
Nung nóng HgO thu được Hg và O2. Hãy tính thể tích của O2 thu được ở ĐKTC khi nung 54,25g HgO
2HgO \(\rightarrow\) 2Hg + O2
nHgO = m/M = 54,25/217 = 0,25(mol)
Theo PT => nO2 = 1/2 . nHgO = 1/2 x 0,25 = 0,125(mol)
=> VO2 = n x 22,4 = 0,125 x 22,4 = 2,8(l)
Đúng 0
Bình luận (0)
Lời giải:
PTHH: 2HgO =(nhiệt)=> 2Hg + O2
Ta có: nHgO = \(\dfrac{54,25}{217}=0,25\left(mol\right)\)
Theo phương trình, nO2 = \(\dfrac{1}{2}n_{HgO}=\dfrac{0,25}{2}=0,125\left(mol\right)\)
=> Thể tích Oxi thu được: VO2(đktc) = \(0,125\cdot22,4=2,8\left(l\right)\)
Đúng 0
Bình luận (0)
PTHH :2HgO-------->2Hg+O2
nHgO=\(\dfrac{54,25}{217}=0,25\)(mol)
theo PT:nO2=0,5nHgO=0,5.0,25=0,125(mol)
VO2(đktc)=0,125.22,4=2,8(l)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Phân hủy 2,17g HgO thu được 0,112lít khí O2(đktc).Tính khối lượng thủy ngân thu được
Xem chi tiết
nHgO=2,17/217=0,01(mol)
nO2=0,112/22,4=0,005(mol)
PTHH: 2 Hg + O2 -to-> 2 HgO
Ta có: 0,01/2 = 0,005
=>P.ứ xảy ra hết.
=> nHg=nHgO=0,01(mol)
=>mHg=0,01.201=2,01(g)
Đúng 4
Bình luận (0)
\(n_{HgO}=\dfrac{2,17}{217}=0,01\left(mol\right)\)
\(n_{O_2}=\dfrac{0,112}{22,4}=0,005\left(mol\right)\)
PTHH : \(2HgO\rightarrow2Hg+O_2\)
0,01 0,0025 0,005 (mol)
\(m_{Hg}=0,0025.201=0,5025\left(g\right)\)
Đúng 1
Bình luận (0)































