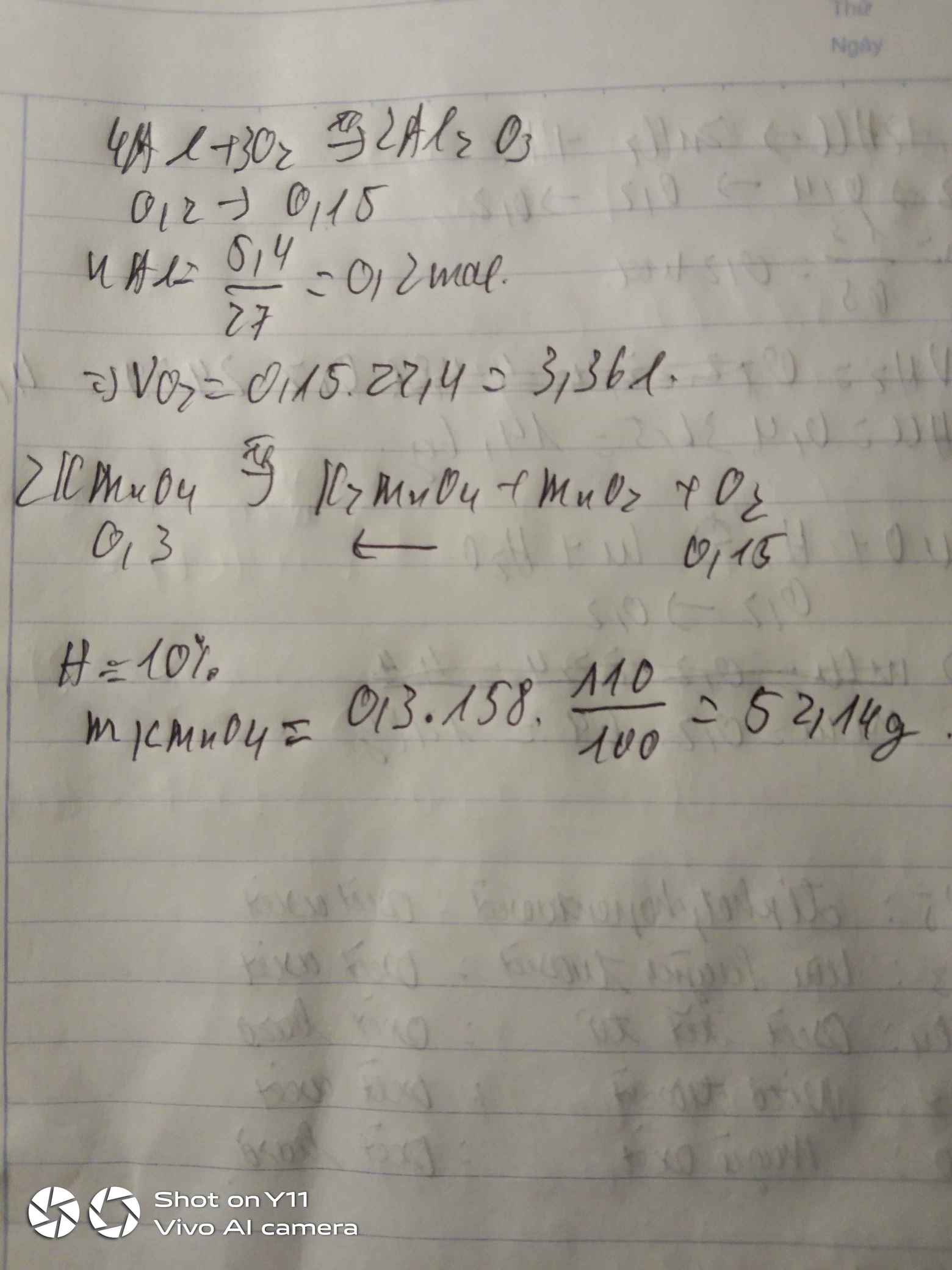Cần đem phân hủy mấy gam Kalipemanganat để sau khi điều chế thu được 144cm3 khí oxi, biết khi thu khí oxi bị hao hụt 40%.

Những câu hỏi liên quan
Bài 6. Cần đem phân hủy mấy gam Kalipenmanganat để sau khi điều chế thì thu được vào các bình 2880 ml khí Oxi, biết khi thu khí Oxi bị hao hụt 20%.
b- Đem phân huỷ hết 2,45gam Kaliclorat để sau khi điều chế khí oxi thu vào đầy 8bình có dung tích 72ml, cho biết khi thu oxi bị hao hụt mấy %?. Các thể tích đo đkt.
Bài 6:
a) \(n_{O_2\left(tt\right)}=\dfrac{2,88}{24}=0,12\left(mol\right)\)
=> \(n_{O_2\left(PTHH\right)}=\dfrac{0,12.100}{80}=0,15\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3<--------------------------------0,15
=> \(m_{KMnO_4}=0,3.158=47,4\left(g\right)\)
b) \(n_{KClO_3}=\dfrac{2,45}{122,5}=0,02\left(mol\right)\)
\(V_{O_2\left(tt\right)}=8.0,072=0,576\left(l\right)\)
=> \(n_{O_2\left(tt\right)}=\dfrac{0,576}{24}=0,024\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,02---------------->0,03
=> nO2(hao hụt) = 0,03 - 0,024 = 0,006 (mol)
=> %O2 bị hao hụt = \(\dfrac{0,006}{0,03}.100\%=20\%\)
Đúng 2
Bình luận (0)
Bài 4 .Đem nung 7 gam kaliclorat sau một thời gian điều chế được 1344ml khí Oxi và còn lại chất rắn X. Khí đo ở ĐKTC.
a) Thu được bao nhiêu ml khí Oxi vào bình, biết khi thu bị hao hụt 15%.
b) Bao nhiêu gam Kaliclorat bị phân hủy?
c) Tính thành phần khối lượng chất rắn X.
Câu 1: Trong số các hợp chất sau, hợp chất nào là oxit axit, hợp chất nào là oxit bazơ: K2O; KCl; FeO; Fe2O3; N2O5; SO3; CO2; CaO; H2SO4; Ba(OH)2
Câu 2: Đốt cháy 5,4 g nhôm trong bình chứa 6,72 lít oxi (ĐKTC) sau phản ứng xảy ra xong thì:
a. Chất nào hết, chất nào dư, mấy gam?
b. Tính khối lượng sản phẩm tạo ra.
Câu 3: a. Cần đem phân hủy mấy gam kalipemanganat để sau khi điều chế thu được 144cm3 khí oxi, biết khi thu khí oxi bị hao hụt 40%.
b.Cần đem phân hủy mấy gam KClO3 để sau...
Đọc tiếp
Câu 1: Trong số các hợp chất sau, hợp chất nào là oxit axit, hợp chất nào là oxit bazơ: K2O; KCl; FeO; Fe2O3; N2O5; SO3; CO2; CaO; H2SO4; Ba(OH)2
Câu 2: Đốt cháy 5,4 g nhôm trong bình chứa 6,72 lít oxi (ĐKTC) sau phản ứng xảy ra xong thì:
a. Chất nào hết, chất nào dư, mấy gam?
b. Tính khối lượng sản phẩm tạo ra.
Câu 3: a. Cần đem phân hủy mấy gam kalipemanganat để sau khi điều chế thu được 144cm3 khí oxi, biết khi thu khí oxi bị hao hụt 40%.
b.Cần đem phân hủy mấy gam KClO3 để sau khi điều chế khí oxi thu vào đầy 6 bình có dung tích 120ml; biết khi thu oxi bị hao hụt 20%. Các thể tích đó ở đkt.
Câu 1:
Oxxit axit : N2O5, SO2, CO3, CO2
Oxxit bazo: K2O , FeO, Fe2O3 , CaO
Câu 2:
\(4Al+3O2-->2Al2O3\)
a)\(n_{Al}=\frac{5,4}{27}=0,2\left(mol\right)\)
n\(_{O2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{Al}\left(\frac{0,2}{4}\right)< nO2\left(\frac{0,3}{3}\right)\Rightarrow O2dư\)
n\(_{O2}=\frac{3}{4}n_{Al}=0,15\left(mol\right)\)
\(n_{O2}dư=0,3-0,15=0,15\left(mol\right)\)
m\(_{O2}dư=0,15.32=4,8\left(g\right)\)
b) \(n_{Al2O3}=\frac{1}{2}n_{Al}=0,15\left(mol\right)\)
\(m_{Al2O3}=0,15.102=15,3\left(g\right)\)
khi đốt cháy sắt trong khí oxi thu được oxit sắt từ Fe3O4
a.Tính số gam sắt và số gam oxi cần dùng điều chế 46,4g oxit sắt từ.
b.Tính số gam kalipemanganat KMnO4 cần điều chế lượng khí oxi nói trên
Khi đốt cháy sắt trong khí oxi thu đc oxit sắt từ Fe3O4
a)Tính số gam sắt và số gam oxi cần dùng để điều chế 4,64g Fe3O4
b)Tính số gam kalipemanganat KClO3 cần dùng để điều chế lượng khí ôxi nói trên
a, PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Ta có: \(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{Fe}=3n_{Fe_3O_4}=0,06\left(mol\right)\\n_{O_2}=2n_{Fe_3O_4}=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Fe}=0,06.56=3,36\left(g\right)\)
\(m_{O_2}=0,04.32=1,28\left(g\right)\)
b, Phần này đề bài cho là KMnO4 hay KClO3 vậy bạn?
Đúng 3
Bình luận (1)
a)
nFe3O4 = 4.64/232 = 0.02 (mol)
3Fe + 2O2 -to-> Fe3O4
0.06__0.04______0.02
mFe = 0.06*56 = 3.36 (g)
Ủa kali pemanganat là KMnO4 mà ta ?
2KMnO4 -to-> K2MnO4 + MnO2 + O2
0.08_________________________0.04
mKMnO4 = 0.08*158 = 12.64 (g)
Đúng 1
Bình luận (0)
Để chuẩn bị cho thực hành cần cho 10 lọ khí oxi.Mỗi lọ có dung tích 112ml. a)giả sử điều chế khí oxi bằng KMnO4 tính khối lượng KMnO4 phải dùng biết oxi thu dcj ở ĐKTC là hao hụt 20 phần trăm . b)vẫn dcj khí oxi như trên đem oxinhoas hết sắt thì khối lượng oxi thu dcj là bao nhiêu
Trong phòng thí nghiệm cần dùng 28 bình chứa khí oxi để làm thí nghiệm, mỗi bình có dung tích là 100ml. Tính khối lượng thuốc tím (KMnO4) cần dùng để khi nhiệt phân thu đc đủ lượng khí oxi trên, biết khi thu lượng khí oxi bị hao hụt mất 20%
Giúp mik vs ạ mik cám ơn trc :33
\(V_{O_2\left(thu.được\right)}=28=0,1=2,8\left(l\right)\)
=> \(V_{O_2\left(sinh.ra\right)}=\dfrac{2,8.100}{80}=3,5\left(l\right)\)
=> \(n_{O_2\left(sinh.ra\right)}=\dfrac{3,5}{22,4}=0,15625\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3125<------------------------0,15625
=> mKMnO4 = 0,3125.158 = 49,375 (g)
Đúng 2
Bình luận (0)
Để điều chế oxi trong phòng thí nghiệm người ta phân hủy kali clorat (KClO3) thu được kali clorua (KCl ) và khí oxi (O2).a. Tính thể tích khí oxi (đktc) thu được khi phân hủy 12,25 gam KClO3.b. Tính thể tích không khí chứa lượng oxi trên biết rằng c. Dùng toàn bộ lượng oxi trên cho tác dụng với 28 gam sắt. Sau phản ứng chất nào còn dư ? (Cho biết:K 39; Cl 35,5 ; O 16; Fe 56) Bài làm:
Đọc tiếp
Để điều chế oxi trong phòng thí nghiệm người ta phân hủy kali clorat (KClO3) thu được kali clorua (KCl ) và khí oxi (O2).
a. Tính thể tích khí oxi (đktc) thu được khi phân hủy 12,25 gam KClO3.
b. Tính thể tích không khí chứa lượng oxi trên biết rằng ![]() =
= ![]()
c. Dùng toàn bộ lượng oxi trên cho tác dụng với 28 gam sắt. Sau phản ứng chất nào còn dư ?
(Cho biết:K = 39; Cl = 35,5 ; O = 16; Fe = 56)
Bài làm:
a.\(n_{KClO_3}=\dfrac{m_{KClO_3}}{M_{KClO_3}}=\dfrac{12,25}{122,5}=0,1mol\)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
2 2 3 ( mol )
0,1 0,15
\(V_{O_2}=n_{O_2}.22,4=0,15.22,4=3,36l\)
b.\(V_{kk}=V_{O_2}.5=3,36.5=16,8l\)
c.\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{28}{56}=0,5mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
3 2 1 ( mol )
0,5 > 0,15 ( mol )
0,225 0,15 ( mol )
\(m_{Fe\left(du\right)}=n_{Fe\left(du\right)}.M_{Fe}=\left(0,5-0,225\right).56=15,4g\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 5,4g nhôm. Tính :
a. Thể tích khí O2 (đktc) cần dùng ?
b. Số gam KMnO4 cần dùng để điều chế lượng khí O2 trên giả sử quá trình thu khí oxi bị hao hụt 10% ?
\(n_{Al}=\dfrac{5.4}{27}=0,2mol\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,2 0,15 0,1
a)\(V_{O_2}=0,15\cdot22,4=3,36l\)
b)\(n_{O_2}=0,15\cdot10\%=0,015mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,03 0,015
\(m_{KMnO_4}=0,03\cdot158=4,74g\)
Đúng 1
Bình luận (0)