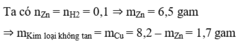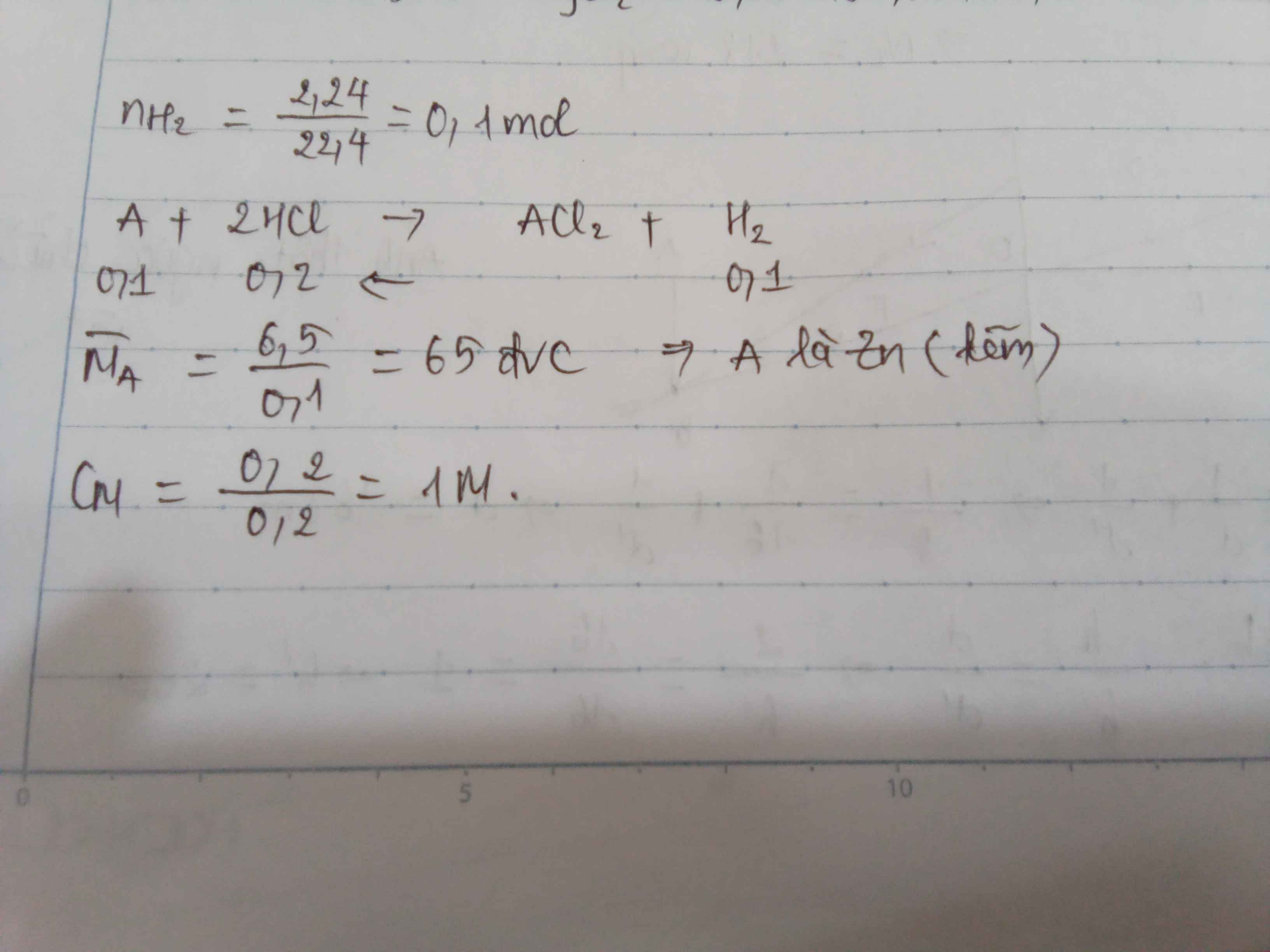Cho 6,5 gam kim loại vào 150ml dung dịch HCl 2M. Sau khi phản ứng xong thu được 2,24 lít khí H2 (đktc).Xác định kim loại nói trên.

Những câu hỏi liên quan
Cho 3,84 gam kim loại M ( hóa trị II không đổi ) hòa tan trong V (ml) dung dịch HCL 2M. Sau phản ứng thu được 3.584 lít khí H2 (ở đktc)a, Xác định kim loại Mb, Nếu cho kim loại M như trên vào dung dịch HNO3 loãng thì thu được sản phẩm gồm muối A, H2O, 1344ml hỗn hợp khí N2, và NO (ở đktc). Viết phương trình hóa học xảy ra và tính thể tích các khí thu được
Đọc tiếp
Cho 3,84 gam kim loại M ( hóa trị II không đổi ) hòa tan trong V (ml) dung dịch HCL 2M. Sau phản ứng thu được 3.584 lít khí H2 (ở đktc)
a, Xác định kim loại M
b, Nếu cho kim loại M như trên vào dung dịch HNO3 loãng thì thu được sản phẩm gồm muối A, H2O, 1344ml hỗn hợp khí N2, và NO (ở đktc). Viết phương trình hóa học xảy ra và tính thể tích các khí thu được
a)
M + 2HCl → MCl2 + H2
nH2 = \(\dfrac{3,584}{22,4}=\)0,16 mol => nM = 0,16 mol
<=> MM = \(\dfrac{3,84}{0,16}\)= 24 (g/mol) => M là magie (Mg).
b) 8Mg + 20HNO3 → 8Mg(NO3) + 2NO + N2 + 10H2O
Từ tỉ lệ phương trình , gọi số mol N2 là x => nNO = 2x mol
=> V(NO + N2) =3x.22,4 =1,344
<=> x =0,02
=> VN2 = 0,02.22,4 =0,448 lít , VNO= 0,04.22,4 = 0,896 lít
Đúng 0
Bình luận (0)
Cho 6,5 gam một oxit kim loại hoá trị II vào 150 ml dung dịch HCl 2M. Sau khi phản ứng xong thu được 2,24 lít khí H2(đktc). Xác định kim loại nói trên.
Gọi CTHH của kim loại là R
R + 2HCl -> RCl2 + H2 (1)
nH2=0,1(mol)
nHCl=0,3(mol)
=>nHCl dư
Từ 1:
nR=nH2=0,1(mol)
MR=6,5:0,1=65
=>R là Zn
Đúng 0
Bình luận (0)
Cho 2,4 gam kim loại hóa trị II tác dụng với dung dịch HCl lấy dư , sau khi phản ứng kết thúc thu được 2,24 lít H2 (đktc) . Xác định kim loại ?
PTHH: \(R+2HCl\rightarrow RCl_2+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_R\)
\(\Rightarrow M_R=\dfrac{2,4}{0,1}=24\) (Magie)
Đúng 5
Bình luận (1)
cho 2,4g kim loại hóa trị II tác dụng với dung dịch HCl lấy dư, sau khi phản ứng kết thức thu được 2,24 lít khí H2 (ở đktc) xác định tên kim loại?
cho 2,7g kim loại hóa trị III tác dụng với dung dịch H2SO4 lấy dư, sau khi phản ứng kết thúc thu được 3,36 lí khia H2 (ở đktc) xác định tenn kim loại?
Bài 1 :
$R + 2HCl \to RCl_2 + H_2$
n R = n H2 = 2,24/22,4 = 0,1(mol)
M R = 2,4/0,1 = 24(Mg) - Magie
Bài 2 :
$2R + 6HCl \to 2RCl_3 + 3H_2$
n H2 = 3,36/22,4 = 0,15(mol)
n R = 2/3 n H2 = 0,1(mol)
M R = 2,7/0,1 = 27(Al) - Nhôm
Đúng 3
Bình luận (0)
Cho 4,8 gam kim loại M vào 50 gam dung dịch HCl nồng độ 36,5 % , phản ứng xong thu được 4,48 lít khí H2 , ( ở đktc ) và dung dịch X. Xác định kim loại M và tính nồng độ phần trăm các chất trong X.
PTHH: \(2M+2xHCl\rightarrow2MCl_x+xH_2\uparrow\) (x là hóa trị của M)
Tính theo sản phẩm
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow n_M=\dfrac{0,4}{x}\left(mol\right)\) \(\Rightarrow M=\dfrac{4,8}{\dfrac{0,4}{x}}=12x\)
Ta thấy với \(x=2\) thì \(M=24\) (Magie)
Mặt khác: \(n_{HCl}=\dfrac{50\cdot36,5\%}{36,5}=0,5\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\\n_{HCl\left(dư\right)}=0,1\left(mol\right)\end{matrix}\right.\)
Ta lại có: \(m_{dd\left(sau.p/ứ\right)}=m_{Mg}+m_{ddHCl}-m_{H_2}=4,8+50-0,2\cdot2=54,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,2\cdot95}{54,4}\cdot100\%\approx34,93\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,1\cdot36,5}{54,4}\cdot100\%\approx6,71\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Cho 8,2 gam hỗn hợp kim loại Zn và Cu vào dung dịch HCl (dư). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít khí
H
2
(ở đktc) và m gam kim loại không tan. Giá trị của m là A. 6,4. B. 1,7. C. 1,8. D. 6,5.
Đọc tiếp
Cho 8,2 gam hỗn hợp kim loại Zn và Cu vào dung dịch HCl (dư). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít khí H 2 (ở đktc) và m gam kim loại không tan. Giá trị của m là
A. 6,4.
B. 1,7.
C. 1,8.
D. 6,5.
Cho 8,2 gam hỗn hợp kim loại Zn và Cu vào dung dịch HCl (dư). Sau khi phản ứng xảy ra hoàn toàn, thu được 2,24 lít khí H2 (ở đktc) và m gam kim loại không tan. Giá trị của m là
A. 6,4.
B. 1,7.
C. 1,8.
D. 6,5.
Chọn đáp án B
Ta có nZn = nH2 = 0,1 ⇒ mZn = 6,5 gam
⇒ mKim loại không tan = mCu = 8,2 – mZn = 1,7 gam
Đúng 0
Bình luận (0)
2/ Cho 6,5 gam kim loại A hóa trị II vào 200ml HCl thu được 2,24 lít khí và dung dịch X. Tìm kim loại A và nồng độ dung dịch sau phản ứng
Hòa tan hoàn toàn 6,5 gam một kim loại A chưa rõ hóa trị vào dung dịch HCl thì thu được 2,24 lít khí hidro(đktc) . Xác định kim loại A
Gọi hóa trị của kim loại A là x
\(n_{H_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH : 2A + 2xHCl -----> 2AClx + xH2
0,2/x mol 0,1mol
Áp dụng m = n.M , ta có : \(A.\frac{0,2}{x}=6,5\Rightarrow A=32,5x\)
Do x là hóa trị của kim loại nên x chỉ có thể là I , II hoặc III
Nếu x = 1 thì A = 32,5 (loại)
Nếu x = 2 thì A = 65 (nhận)
Nếu x = 3 thì A = 97,5 (loại)
Vậy A là kim loại Kẽm (Zn)
Đúng 2
Bình luận (2)
nH2= 0,1 (mol)
2A + 2nHCl -> 2ACln + nH2
Theo PTHH
=> \(\frac{6,5}{A}=\frac{2}{n}\cdot0,1\)
=> 6,5n = 0,2A
=> 32,5n =A
Với A là kim loại tác dụng được vs HCl => hóa trị chỉ có thể từ 1 tới 3
Thay vào ...
=> n= 2
A = 65
=> A là Zn
Đúng 0
Bình luận (1)