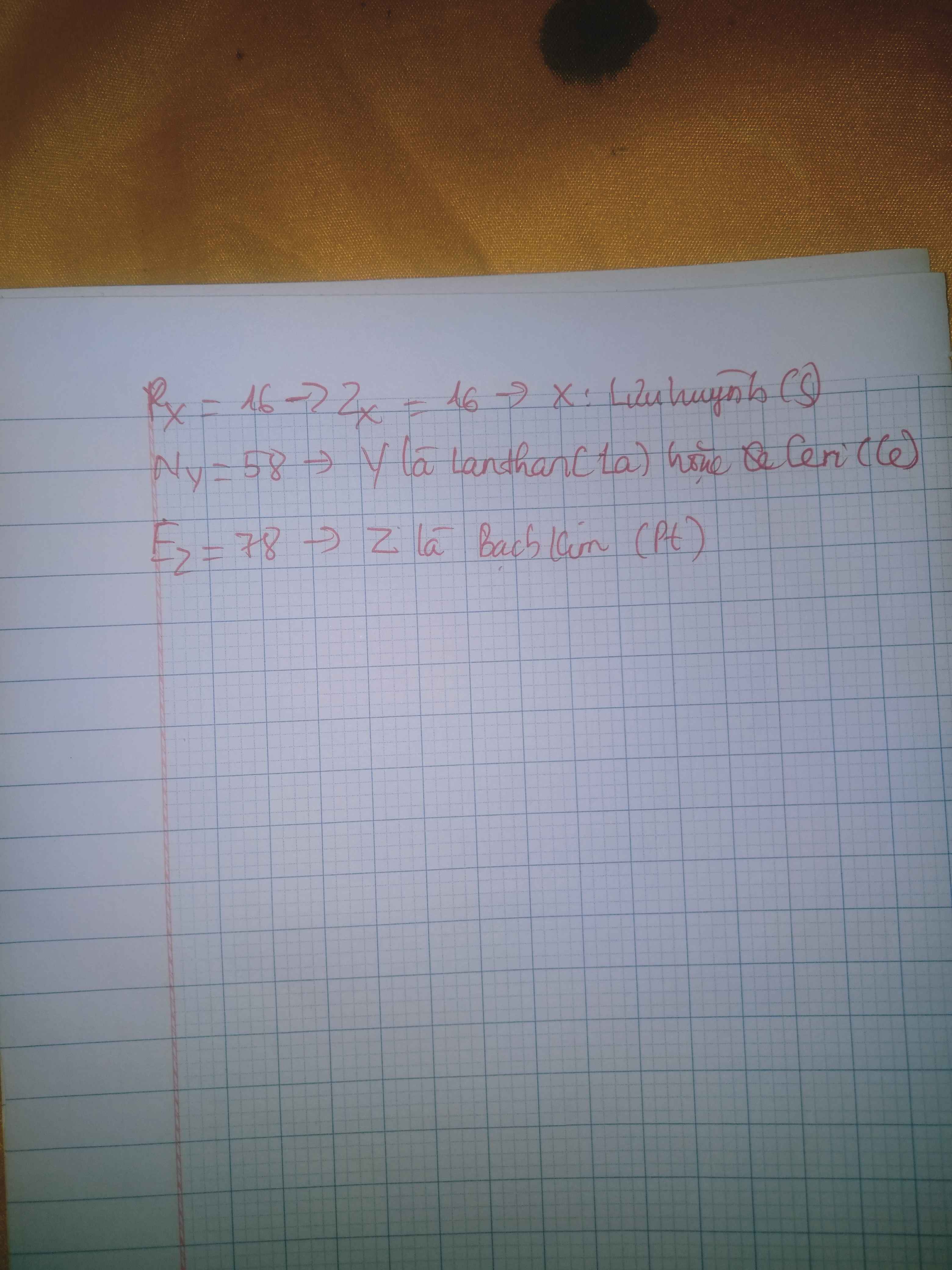Cho các nguyên tố X,Y,Z có số hiệu nguyên tử lần lượt là 6,10,20. Viết cấu hình e của nguyên tử các nguyên tố X,Y,Z. Xác định vị trí của các nguyên tố đó trong bảng tuần hoàn( do hỏi không xuống dòng nên thông cảm như bài trước)

Những câu hỏi liên quan
Bài 7: Cho các nguyên tố X,Y, Z. Tổng số hạt p,n,e trong các nguyên tử lần lượt là 16, 58,78. Số nơtron trong hạt nhân và số hiệu nguyên tử của mỗi nguyên tố khác nhau không quá 1 đơn vị. Hãy xác định các nguyên tố và viết kí hiệu các nguyên tố.
Cation X2+, nguyên tử Y và anion Z- đều có cấu hình electron lớp ngoài cùng là 2s22p6.
a) Viết cấu hình electron của các nguyên tử X, Y, Z.
b) Xác định vị trí của X, Y, Z trong bảng tuần hoàn các nguyên tố hóa học. Giải thích.
1. Oxit cao nhất của nguyên tố R có dạng R2O7. Sản phẩm khí của R với hidro chứa 2,74% hidro về khối lượng. Tìm R?
2. Cho các nguyên tố X, Y, Z có số hiệu nguyên tử lần lượt là 9, 16,17:
a) Xác định vị trí của chúng trong BTH.
b) Sắp xếp các nguyên tố đó theo thứ tự tính phi kim tăng dần.
1 viết kí hiệu nguyên tử của các nguyên tố có Z lần lượt là 2,4,8,11,21
2 viết cấu hình e của các nguyên tố có Z lần lượt là 8,11,20,15
-cho bt số lớp và số phân lớp e của chúng
Cho các nguyên tố X, Y, Z. Tổng số hạt p, n và e trong các nguyên tử lần lượt là 16, 58 và 60. Số notron trong hạt nhân và số hiệu nguyên tử của mỗi nguyên tố khác nhau không quá 1 đơn vị. Các nguyên tố X, Y, Z lần lượt là:
A. K, Na, Ca.
B. Na, K, Ca.
C. Na, Ca, K.
D. Ca, K, Na
Bài 1. Có các nguyên tố có kí hiệu lần lượt là: 7A; 13B; 16G; 20D; 18E. a) Viết cấu hình electron nguyên tử các nguyên tố đó. b) Cho biết đâu là nguyên tố s, đâu là nguyên tố p. c) Xác định vị trí các nguyên tố này trên bảng HTTH. d) Nêu tính chất hóa học cơ bản của nguyên tố? (kim loại, phi kim, khí hiếm)Bài 2*. Cho các nguyên tố sau: X có tổng số hạt mang điện là 18; Y có tổng số electron trên phân lớp s là 6. T có 7 electron thuộc lớp M. R có phân mức năng lượng cao nhất là 4s1. a) Viết cấu h...
Đọc tiếp
Bài 1. Có các nguyên tố có kí hiệu lần lượt là: 7A; 13B; 16G; 20D; 18E. a) Viết cấu hình electron nguyên tử các nguyên tố đó. b) Cho biết đâu là nguyên tố s, đâu là nguyên tố p. c) Xác định vị trí các nguyên tố này trên bảng HTTH. d) Nêu tính chất hóa học cơ bản của nguyên tố? (kim loại, phi kim, khí hiếm)
Bài 2*. Cho các nguyên tố sau: X có tổng số hạt mang điện là 18; Y có tổng số electron trên phân lớp s là 6. T có 7 electron thuộc lớp M. R có phân mức năng lượng cao nhất là 4s1. a) Viết cấu hình electron nguyên tử các nguyên tố đó. b) Xác định vị trí các nguyên tố này trên bảng HTTH. c) Nêu tính chất hóa học cơ bản của chúng.
Giúp mình với mình cần gấp ạ. Cảm ơn mng
Cấu hình electron nguyên tử của các nguyên tố X, Y, Z, T như sau:
X
:
1
s
2
2
s
2
2
p
6
3
s
2
3
p
6
4
s
2
Y
:
1
s
2
2
s
2
2
p
6
3
s
2...
Đọc tiếp
Cấu hình electron nguyên tử của các nguyên tố X, Y, Z, T như sau:
X : 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 4 s 2 Y : 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 3 d 5 4 s 2 Z : 1 s 2 2 s 2 2 p 5 T : 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2
Số electron hóa trị trong nguyên tử của các nguyên tố X, Y, Z, T lần lượt là
A. 2; 7; 7; 12.
B. 8; 7; 7; 2.
C. 2; 2; 5; 2
D. 2; 7; 7; 2
Chọn D
Electron hóa trị là những electron có khả năng tham gia hình thành liên kết hóa học. Chúng thường nằm ở lớp ngoài cùng hoặc ở cả phân lớp sát lớp ngoài cùng nếu phân lớp đó chưa bão hòa.
→ X có 2e hóa trị; Y có 7e hóa trị; Z có 7e hóa trị; T có 2e hóa trị.
Đúng 0
Bình luận (0)
Có các nguyên tố có kí hiệu lần lượt là: 7A; 13B; 16G; 20D; 18E.
a) Viết cấu hình electron nguyên tử các nguyên tố đó.
b) Cho biết đâu là nguyên tố s, đâu là nguyên tố p.
c) Xác định vị trí các nguyên tố này trên bảng HTTH.
d) Nêu tính chất hóa học cơ bản của nguyên tố? (kim loại, phi kim, khí hiếm)
Giúp mình với. mình cảm ơn mng
Viết cấu hình electron nguyên tử, xác định vị trí của chúng trong bảng tuần hoàn và dự đoán tính chất của các nguyên tố có số hiệu nguyên tử sau: a) Na (Z 11) b) Al (Z 13) c) S (Z 16) d) Cl (Z 17)
Đọc tiếp
Viết cấu hình electron nguyên tử, xác định vị trí của chúng trong bảng tuần hoàn và dự đoán tính chất của các nguyên tố có số hiệu nguyên tử sau:
a) Na (Z = 11) b) Al (Z = 13)
c) S (Z = 16) d) Cl (Z = 17)
Na(Z=11) 1s2 2s2 2p6 3s1 thuộc ô thứ 11, chu kì 3, nhóm IA
Al(Z=13) 1s2 2s2 2p6 3s2 3p1 thuộc ô thứ 13, chu kì 3, nhóm IIIA
S(Z=16) 1s2 2s2 2p6 3s2 3p4 thuộc ô thứ 16, chu kì 3
Nhóm VIA
Cl(Z=17) 1s2 2s2 2p6 3s2 3p5 thuộc ô thứ 17, chu kì 3,
Nhóm VIIA
Đúng 1
Bình luận (0)
Cho nguyên tử nguyên tố X(z=14) Y(z=15) Z(z=16) T(z=17). A, viết cấu hình e nguyên tử của X. Xác định vị trí của X trong bản tuần hoàn. B, viết công thức oxit cao nhất, hợp chất khí với hiđro của X
Xem chi tiết
a.
14X : 1s22s22p63s23p2
Vị trí X trong BTH : ô số 14 , chu kỳ 3 ( vì có 3 lớp e ) ,nhóm IVA ( vì có 4e lớp ngoài cùng ).
b.
Hợp chất oxit cao nhất là SiO2 và hợp chất khí với hidro là SiH4
Đúng 1
Bình luận (0)