Cho 4,48 lít khí N2 (đktc) tác dụng với H2 dư thu được 1,7 gam NH3. tính H% PHẢN ỨNG
Cho 4,48 lít khí N² ( đktc ) tác dụng với H² dư thứ được 1,7 gam NH³. Tính hiệu suất của phản ứng
\(n_{N_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(N_2+3H_2\underrightarrow{t^o}2NH_3\)
Theo PT: \(n_{NH_3\left(LT\right)}=2n_{N_2}=0,4\left(mol\right)\)
\(\Rightarrow m_{NH_3\left(LT\right)}=0,4.17=6,8\left(g\right)\)
\(\Rightarrow H=\dfrac{1,7}{6,8}.100\%=25\%\)
Cho lượng dư N2 tác dụng với 6,72 lít khí H2(đktc). Biết hiệu suất của phản ứng là 25%, thu được m(gam) NH3. Giá trị của m
$n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
$n_{H_2\ pư} = 0,3.25\% = 0,075(mol)$
\(N_2 + 3H_2 \buildrel{xt,t^,p}\over\rightleftharpoons 2NH_3\)
Theo PTHH :
$n_{NH_3} = \dfrac{2}{3}n_{H_2\ pư} = 0,05(mol)$
$m = 0,05.17 = 0,85(gam)$
Cho lượng dư N2 tác dụng với 10,08 lít khí H2(đktc). Biết hiệu suất của phản ứng là 37%, thu được V lít NH3(đktc). Giá trị của m
$n_{H_2} = \dfrac{10,08}{22,4} = 0,45(mol)$
$n_{H_2\ pư} = 0,45.37\% = 0,1665(mol)$
$N_2 + 3H_2 \buildrel{xt,t^,p}\over\rightleftharpoons 2NH_3$
$n_{NH_3} = \dfrac{3}{2}n_{H_2}= 0,111(mol)$
$V = 0,111.22,4 = 2,4864(lít)$
Cho 8,96 lít N2 (đktc) tác dụng với 20,16 lít H2 (đktc), thu được 3,4 gam NH3. Hiệu suất của phản ứng
$n_{N_2} = 0,4(mol) ; n_{H_2} = 0,9(mol) ; n_{NH_3} = 0,2(mol)$
$N_2 + 3H_2 \buildrel{xt,t^,p}\over\rightleftharpoons 2NH_3$
Ta thấy :
$n_{N_2} : 1 > n_{H_2} : 3$ do đó hiệu suất tính theo số mol Hidro
$n_{H_2\ pư} = \dfrac{3}{2}n_{NH_3} = 0,3(mol)$
$H = \dfrac{0,3}{0,9}.100\% = 33,33\%$
Cho 4,06 gam anđehit X, mạch hở tác dụng với lượng dư dung dịch AgNO3/NH3. Toàn bộ lượng Ag thu được cho tác dụng hết với dung dịch HNO3 đặc, nóng dư thu được 3,248 lít khí (đktc). Mặt khác cho 4,06 gam X tác dụng với H2 dư (Ni, to) thu được m gam chất hữu cơ Y (Biết các phản ứng xảy ra hoàn toàn, dX/N2 < 4). Giá trị của m là
A. 4,205
B. 4,2
C. 4,35
D. 8,7
Đáp án C
Cho Ag thu được tác dụng với HNO3 đặc nóng dư thu được 0,145 mol khí NO2.
→ n A g = 0,145
Ta có: M X < 112
Nếu X là HCHO thì n x = 0 , 126875 → n A g = 0 , 5075 (loại).
Gọi x là số nhóm CHO trong X → n x = 0 , 145 2 x → M x = 56 x
thỏa mãn x=1 thì X là CH2=CH-CHO
→ m = 4,06 + 0,145.2 = 4,35 gam
Cho 4,06 gam anđehit X, mạch hở tác dụng với lượng dư dung dịch AgNO3/NH3. Toàn bộ lượng Ag thu được cho tác dụng hết với dung dịch HNO3 đặc, nóng dư thu được 3,248 lít khí (đktc). Mặt khác cho 4,06 gam X tác dụng với H2 dư (Ni, to) thu được m gam chất hữu cơ Y (Biết các phản ứng xảy ra hoàn toàn, dX/N2 < 4). Giá trị của m là
A. 4,205
B. 4,2
C. 4,35
D. 8,7
Đáp án C
Cho Ag thu được tác dụng với HNO3 đặc nóng dư thu được 0,145 mol khí NO2

Cho 4,06 gam anđehit X, mạch hở tác dụng với lượng dư dung dịch AgNO3/NH3. Toàn bộ lượng Ag thu được cho tác dụng hết với dung dịch HNO3 đặc, nóng dư thu được 3,248 lít khí (đktc). Mặt khác cho 4,06 gam X tác dụng với H2 dư (Ni, to) thu được m gam chất hữu cơ Y (Biết các phản ứng xảy ra hoàn toàn, dX/N2 < 4). Giá trị của m là
A. 4,205
B. 4,2
C. 4,35
D. 8,7
Giải thích: Đáp án C
Cho Ag thu được tác dụng với HNO3 đặc nóng dư thu được 0,145 mol khí NO2.
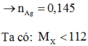
Nếu X là HCHO thì ![]()
Gọi x là số nhóm CHO trong X ![]()
thỏa mãn x=1 thì X là CH2=CH-CHO
![]()
Thực hiện phản ứng giữa H 2 và N 2 trong bình kín có xúc tác thu được 1,7 gam NH 3 với hiệu suất phản ứng là 80%. Thể tích H 2 (đktc) cần dùng cho phản ứng là (Cho: N = 14, H = 1)
A. 4,2 lít.
B. 2,4 lít.
C. 4 lít.
D. 5lít.
Chọn A
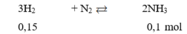
Do hiệu suất phản ứng là 80% nên thể tích H 2 cần dùng là:
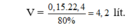
Cho 5 lít khí N2 tác dụng với 5 lít khí H2 ở nhiệt độ cao, xúc tác thích hợp để tổng hợp khí NH3. Sau phản ứng thu được 7 lí hỗn hợp khí X gồm N2, H2, NH3. Tính thể tích mỗi khí trong hỗn hợp X thu được và hiệu suất phản ứng tổng hợp NH3. Biết các khí đo ở cùng điều kiện nhiệt độ và áp suất
N2 + 3H2 \(\overset{t^o,p,xt}{⇌}\) 2NH3.
Cứ 1 lít N2 tác dụng với 3 lít H2 tạo ra 2 lít NH3. Vậy a lít N2 tác dụng với 3a lít H2 tạo ra 2a lít NH3, thu được (5-a)+(5-3a)+2a=7 (lít), suy ra a=1,5 (lít).
Thể tích mỗi khí trong hỗn hợp X gồm khí N2 (5-1,5=3,5 (lít)), khí H2 (5-3.1,5=0,5 (lít)) và khí NH3 (2.1,5=3 (lít)).
Hiệu suất phản ứng là H=(5-0,5)/5.100%=90% (hiệu suất tính theo H2 do H2 thiếu).