Cho hông hợp gồm 2,3g Na và 13,7g Ba vào nước dư thu được 200ml dd X.
a) tính Cm chất tan trong dd X
b)cho dd X tác dụng với 500ml dd CuSO4 1,5M thu được kết tủa Y và dung dịch Z. Tính m Y và Cm chất tan trong Z

Những câu hỏi liên quan
cho dd NaOH 2M tác dụng vừa đủ với 200ml dd FeCl3 1,5M. Sau khi phản ứng kết thúc thu được kết tủa X và dung dịch A. Lọc kết tủa X và nung đến khối lượng không đổi thu được chất rắn Y.
a) Viết các phản ứng đã xảy ra
b) Tính thể tích dung dịch natri hidroxit đã dùng và nồng độ mol của dd A. Cho rằng thể tích dd thay đổi ko đáng kể khi phản ứng
c) Tính khối lượng kết tủa X và chấ t rắn Y
Đọc tiếp
cho dd NaOH 2M tác dụng vừa đủ với 200ml dd FeCl3 1,5M. Sau khi phản ứng kết thúc thu được kết tủa X và dung dịch A. Lọc kết tủa X và nung đến khối lượng không đổi thu được chất rắn Y. a) Viết các phản ứng đã xảy ra b) Tính thể tích dung dịch natri hidroxit đã dùng và nồng độ mol của dd A. Cho rằng thể tích dd thay đổi ko đáng kể khi phản ứng c) Tính khối lượng kết tủa X và chấ t rắn Y
\(a,PTHH:3NaOH+FeCl_3\rightarrow3NaCl+Fe\left(OH\right)_3\downarrow\\ 2Fe\left(OH\right)_3\rightarrow^{t^o}Fe_2O_3+3H_2O\uparrow\\ b,n_{FeCl_3}=1,5\cdot0,2=0,3\left(mol\right)\\ \Rightarrow n_{NaOH}=3n_{FeCl_3}=0,9\left(mol\right)\\ \Rightarrow V_{dd_{NaOH}}=\dfrac{0,9}{2}=0,45\left(l\right)\)
Theo đề: \(\left\{{}\begin{matrix}X:Fe\left(OH\right)_3\\A:NaCl\\Y:Fe_2O_3\end{matrix}\right.\)
Theo PT: \(n_{NaCl}=3n_{FeCl_3}=0,9\left(mol\right)\)
\(\Rightarrow C_{M_{NaCl}}=\dfrac{0,9}{0,45+0,2}\approx1,4M\)
\(c,\) Theo PT: \(n_{Fe\left(OH\right)_3}=n_{FeCl_3}=0,3\left(mol\right);n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe\left(OH\right)_3}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_X=m_{Fe\left(OH\right)_3}=0,3\cdot107=32,1\left(g\right)\\m_Y=m_{Fe_2O_3}=0,15\cdot160=24\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp gồm Mg và Fe2O3 trong dđ HCl thu được dd X và thoát ra 3,36 lít H2 (đkc). Cho dung dịch X tác dụng với dd KOH dư thu được kết tủa Y. Nung Y đến khối lượng không đổi được 22 gam chất rắn. a) Viết các PTHH xảy ra. b) Tính % khối lượng Mg và Fe2O3 ban đầu.
a)
Mg + 2HCl --> MgCl2 + H2
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
MgCl2 + 2KOH + 2KCl + Mg(OH)2
FeCl3 + 3KOH --> 3KCl + Fe(OH)3
Mg(OH)2 --to--> MgO + H2O
2Fe(OH)3 --to--> Fe2O3 + 3H2O
b) Gọi số mol Mg, Fe2O3 là a, b (mol)
Theo PTHH: \(a=n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PTHH: \(n_{MgO}=n_{Mg}=a=0,15\left(mol\right)\)
=> \(n_{Fe_2O_3\left(chất.rắn.sau.khi.nung\right)}=\dfrac{22-0,15.40}{160}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Fe_2O_3\left(bđ\right)}=n_{Fe_2O_3\left(chất.rắn.sau.khi.nung\right)}=0,1\left(mol\right)\)
=> b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,15.24}{0,15.24+0,1.160}.100\%=18,37\%\\\%m_{Fe_2O_3}=\dfrac{0,1.160}{0,15.24+0,1.160}.100\%=81,63\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho m(g) hỗn hợp X gồm Al,Na,Na2O,Cu vào nước dư.Sau phản ứng thu được 3,024l khí(đktc),dd Y và 2,46 chất rắn ko tan Z.Cho toàn bộ Z tác dụng dd h2so4 dư thu được 0,672l khí(đktc).Cho 110ml dd HCl 1M vào Y thấy tạo 5,46 g kết tủa.Viết pthh và tính%m nhôm trong X<giúp mình với>
Z tác dụng với $H_2SO_4$ tạo khí suy ra Z có Al,Cu
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$n_{Al} = \dfrac{2}{3}n_{H_2} = 0,02(mol)$
$m_{Cu} = 2,46 - 0,02.27=1,92(gam)$
$n_{Al(OH)_3} = 0,07(mol) ; n_{HCl} = 0,11(mol)$
NaAlO2 + HCl + H2O → Al(OH)3 + NaCl
a................a........................a...............................(mol)
Al(OH)3 + 3HCl → AlCl3 + 3H2O
a - 0,07......3a-0,21..............................(mol)
Suy ra: a + 3a - 0,21 = 0,11
Suy ra: a = 0,08
$2Na + 2H_2O \to 2NaOH + H_2$
$Na_2O + H_2O \to 2NaOH$
$2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
Ta có : $n_{H_2} = 0,5n_{Na} + 1,5n_{NaAlO_2} \Rightarrow n_{Na} = \dfrac{0,135 - 1,5.0,08}{0,5} = 0,03(mol)$
Bảo toàn Na,Al
$n_{Na_2O} = \dfrac{0,08 - 0,03}{2} = 0,025(mol)$
$n_{Al} = 0,08 + 0,02 = 0,1(mol)$
$\%m_{Al} = \dfrac{0,1.27}{0,1.27 + 0,025.62 + 0,03.23 + 1,92}.100\% = 39,36\%$
Đúng 3
Bình luận (2)
Hòa tan hoàn toàn m g hỗn hợp X gồm CuSO4, FeSO4 và Fe2(SO4)3 vào nước thu được dung dịch Y. Thành phần phần trăm khối lượng lưu huỳnh trong X là 21,62%. Cho dd Y tác dụng với 1 lượng dư dd NaOH, lọc thu được kết tủa Z. Nung kết tủa Z trong không khí đến khối lượng không đổi thu được chất rắn R. Cho một luồng khí CO đi qua ống sứ đựng R thu được 8,32 g hỗn hợp kim loại . Các phản ứng xảy ra hoàn toàn. Tìm giá trị của m
Đọc tiếp
Hòa tan hoàn toàn m g hỗn hợp X gồm CuSO4, FeSO4 và Fe2(SO4)3 vào nước thu được dung dịch Y. Thành phần phần trăm khối lượng lưu huỳnh trong X là 21,62%. Cho dd Y tác dụng với 1 lượng dư dd NaOH, lọc thu được kết tủa Z. Nung kết tủa Z trong không khí đến khối lượng không đổi thu được chất rắn R. Cho một luồng khí CO đi qua ống sứ đựng R thu được 8,32 g hỗn hợp kim loại . Các phản ứng xảy ra hoàn toàn. Tìm giá trị của m
Hòa tan hoàn toàn 19,2 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 trong 400 ml dung dịch HNO3 3M (dư) đun nóng, thu được dung dịch Y và khí NO (NO là sản phẩm khử duy nhất của NO3-). Cho dd Y tác dụng hết với 650 ml dung dịch NaOH 2M được m gam kết tủa. Lọc bỏ kết tủa được dd Z. Cô cạn dd Z thu được 97 gam chất rắn. Giá trị của m là: A. 42,8g B. 24,0g C. 32,1g D. 21,4g
Đọc tiếp
Hòa tan hoàn toàn 19,2 gam hỗn hợp X gồm Fe, FeO, Fe3O4 và Fe2O3 trong 400 ml dung dịch HNO3 3M (dư) đun nóng, thu được dung dịch Y và khí NO (NO là sản phẩm khử duy nhất của NO3-). Cho dd Y tác dụng hết với 650 ml dung dịch NaOH 2M được m gam kết tủa. Lọc bỏ kết tủa được dd Z. Cô cạn dd Z thu được 97 gam chất rắn. Giá trị của m là:
A. 42,8g
B. 24,0g
C. 32,1g
D. 21,4g
Định hướng tư duy giải :
Ta cùng nhau phân tích bài toán này chút các bạn nhé !
Vì HNO3 dư → NaOH sẽ tác dụng với (H+; Fe3+).Nhưng cuối cùng Na cũng biến thành NaNO3 và có thể có NaOH dư. Ta có ngay:
nNaOH = 1,3
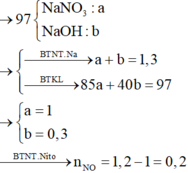
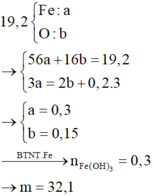
Đúng 0
Bình luận (0)
Trộn 2 dd H2SO4 2M với HCl 1,5M với nhau theo tỉ lệ thể tích 1:1 thu được dd X. Hoà tan hoàn toàn 5,1g hỗn hợp Y gồm Mg và Al trong 200ml dd X thu được 5,6 lít H2 (đktc) và dung dịch Z. a. CMR : dd Z còn dư axit b. Cho 300ml dd B gồm Ba(OH)2 0,6M và NaOH 1M vào dd Z. Tính khối lượng kết tủa thu được sau phản ứng.
Theo gt ta có: $n_{H_2SO_4}=0,2(mol);n_{HCl}=0,15(mol);n_{H_2}=0,25(mol)$
a, Bảo toàn H ta có: $n_{H^+/pu}=0,5(mol)< 0,55(mol)$
Do đó axit còn dư
b, Ta có: $n_{Ba(OH)_2}=0,18(mol);n_{NaOH}=0,3(mol)$
Gọi số mol Mg và Al lần lượt là a;b(mol)
$\Rightarrow 24a+27b=5,1$
Bảo toàn e ta có: $2a+3b=0,5$
Giải hệ ta được $a=b=0,1$
Lượng $OH^-$ tạo kết tủa là $0,18.2+0,3-0,05=0,61(mol)$
Kết tủa gồm 0,18 mol $BaSO_4$; 0,1 mol $Mg(OH)_2$ (Do Al(OH)3 tạo ra bị hòa tan hết)
$\Rightarrow m_{kt}=47,74(g)$
Đúng 2
Bình luận (0)
Bt2. Hòa tan 6,45 g hh bột X gồm Al và Mg vào 200ml dd chứa CuSO4 1M và FeSO4 1M. Sau khi các phản ứng xảy ra hoàn toàn thu đc dd Y gồm ba muối và m gam chất rắn Z. Cho Y tác dụng với lượng dư dd Ba(OH)2, sau khi kết thúc các pư thu đc 105,75 gam chất kết tủa . a. Tính phần trăm khối lượng mỗi kl trong Xb. Tính m
Đọc tiếp
Bt2. Hòa tan 6,45 g hh bột X gồm Al và Mg vào 200ml dd chứa CuSO4 1M và FeSO4 1M. Sau khi các phản ứng xảy ra hoàn toàn thu đc dd Y gồm ba muối và m gam chất rắn Z. Cho Y tác dụng với lượng dư dd Ba(OH)2, sau khi kết thúc các pư thu đc 105,75 gam chất kết tủa .
a. Tính phần trăm khối lượng mỗi kl trong X
b. Tính m
Cho 9,2 g bột x gồm Mg và Fe vào 200 ml dd CuSO4 1M. Sau phản ứng xảy ra hoàn toàn thu được dung dịch y và 15,6 g chất rắn
a) tính khối lượng mỗi kim loại trong x
b) Cho y tác dụng với lượng dư dung dịch naoh tính khối lượng kết tủa thu được khi kết thúc các phản ứng
\(Mg>Fe\) => `Mg` phản ứng trước
\(Mg+Cu^{2+}\rightarrow Mg^{2+}+Cu^o\)
x----->x-------------------->x
\(Fe+Cu^{2+}\rightarrow Fe^{2+}+Cu^o\)
y----->y----------------->y
Giả sử nếu \(Cu^{2+}\) chuyển hết thành \(Cu^o\)
\(\Rightarrow n_{Cu^o}=n_{Cu^{2+}}=n_{kt}\)
Có \(n_{Cu^{2+}}=0,2.1=0,2\left(mol\right)\)
\(n_{kt}=\dfrac{15,6}{64}=0,24375\left(mol\right)>0,2\left(mol\right)\)
\(\Rightarrow\)Giả sử sai, kim loại Fe trong hỗn hợp X còn dư
Theo đề có: \(m_{Fe.dư}=m_{kt}-m_{Cu}=15,6-0,2.64=2,8\left(g\right)\)
Ta có hệ phương trình:
\(\left\{{}\begin{matrix}24x+56y=9,2-2,8=6,4\\x+y=0,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,15\\y=0,05\end{matrix}\right.\)
a. Trong X có:
\(\left\{{}\begin{matrix}m_{Mg}=24.0,15=3,6\left(g\right)\\m_{Fe}=56.0,05+2,8=5,6\left(g\right)\end{matrix}\right.\)
b
Y: \(\left\{{}\begin{matrix}n_{MgSO_4}=x=0,15\left(mol\right)\\n_{FeSO_4}=y=0,05\left(mol\right)\end{matrix}\right.\)
\(MgSO_4+2NaOH\rightarrow Mg\left(OH\right)_2+Na_2SO_4\)
0,15--------------------->0,15
\(FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_2+Na_2SO_4\)
0,05-------------------->0,05
\(m_{kt}=m_{Mg\left(OH\right)_2}+m_{Fe\left(OH\right)_2}=0,15.58+0,05.90=13,2\left(g\right)\)
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 16,4gam hh X gồm MgO và MgCO3 trong dd H2SO4. sau PƯ thu đc dd A và 2,24l khí CO2 ở đktc. cho 300ml dd Ba(OH)2 1,5M vào A thu đc 110,6g kết tủa và 500ml dd B l. tính CM của dd B
MgO+H2SO4 → MgSO4+H2O(1)
MgCO3+H2SO4 → MgSO4+ CO2+H2O (2)
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT (2): nMgCO3=nCO2=0,1mol
=> mMgCO3=0,1.84=8,4g
mMgO=16,4-8,4=8g
=> nMgO=\(\dfrac{8}{40}\) = 0,2mol
Theo PT (1,2) ta có:nMgSO4=nMgO+nMgCO3=0,1+0,2=0,3 mol
nBa(OH)2=0,3.1,5 = 0,45 mol
Gọi x là số mol H2SO4 còn dư sau phản ứng (1,2).
H2SO4+Ba(OH)2→BaSO4↓+2H2O(3)
MgSO4+Ba(OH)2→BaSO4↓+Mg(OH)2↓(4)
Kết tủa tạo thành gồm BaSO4 và Mg(OH)2
Do đó dd B thu được là Ba(OH)2 dư
Ta có: 233x + 233.0,3 + 58.0,3 =110,6
=>x=0,1mol
Theo PT (3,4): nBa(OH)2 pứ=nH2SO4+nMgSO4=0,1+0,3=0,4mol
nBa(OH)2(dư)=0,45−0,4=0,05mol
CMBa(OH)2=\(\dfrac{0,05}{0,5}\)=0,1M
Đúng 1
Bình luận (0)
























