Cho 20g hỗn hợp X gồm zn fe cu vào dd Hcl dư đến khi pư xảy ra hoàn toàn thu được dd Y;5.6 lít khỉ ở đktc và còn lại 5,1 g chất rắn Z
a,viết các pt pư xảy ra
b,tính % kluong mỗi kloai trong hỗn hợp X
Cho hh gồm Fe và Zn vào dd AgNO3 đến khi các pư xảy ra hoàn toàn, thu được dd X gồm hai muối và chất rắn Y gồm hai kim loại. Hai muối trong X là
A. Fe(NO3)3 và Zn(NO3)2.
B. Zn(NO3)2 và Fe(NO3)2.
C. AgNO3 và Zn(NO3)2.
D. Fe(NO3)2 và AgNO3.
Đáp án B
Hai muối tạo ra phải là muối của kim loại mạnh Zn và Fe
Hai kim loại tạo ra phải 1à 2 kim 1oại yếu 1à Ag và Fe => Fe dư => Muối thu được là muối Fe(NO3)2
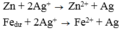
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dd HCl 2M vừa đủ để phản ứng với chất rắn X là:
A. 600 ml
B. 200 ml
C. 800 ml
D. 400 ml
nHCl = nCl- = 2nO = (23,2 - 16,8).2 : 18 = 0,8-> V = 400ml
=> Đáp án A
Một hỗn hợp Y có khối lượng m gam gồm 3 kim loại Mg , Zn ,Fe biết tỉ lệ số mol của Mg ,Zn ,Fe trong hỗn hợp Y lần lượt là 1:2:3. Cho hỗn hợp Y vào dd HCl dư đến phản ứng xảy ra hoàn toàn thấy khối lượng dd HCl tăng thêm (m-2,4) gam. Tính giá trị m.
Mong mọi người giải thích kĩ giùm mình!
\(m_{H_2} = m -(m-2,4) = 2,4(gam)\\ \Rightarrow n_{H_2} = \dfrac{2,4}{2} = 1,2(mol)\\ Gọi : n_{Mg} = a ;n_{Zn} = 2a;n_{Fe}= 3a(mol)\\ Mg + 2HCl \to MgCl_2 + H_2\\ Zn + 2HCl \to ZnCl_2 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = n_{Mg} + n_{Zn} + n_{Fe} = a + 2a + 3a = 1,2(mol)\\ \Rightarrow a = 0,2;\\ \Rightarrow m = 0,2.24 + 0,2.2.65 + 0,2.3.56 = 64,4(gam)\)
Một hỗn hợp Y có khối lượng m gam gồm 3 kim loại Mg , Zn ,Fe biết tỉ lệ số mol của Mg ,Zn ,Fe trong hỗn hợp Y lần lượt là 1:2:3. Cho hỗn hợp Y vào dd HCl dư đến phản ứng xảy ra hoàn toàn thấy khối lượng dd HCl tăng thêm (m-2,4) gam. Tính giá trị m.
Gọi x, 2x, 3x tương ứng là số mol của Mg, Zn và Fe: 24x + 65.2x + 56.3x = m ---> m = 322x.
Khối lượng dd tăng = khối lượng kim loại - mH2
m - 2,4 = m - (2x + 4x + 9x) ---> 15x = 2,4 hay x = 0,16 mol.
Thay vào trên thu được: m = 322.0,16 = 51,52 gam.
Nung nóng m gam hỗn hợp X gồm Mg Al và Cu trong O2 dư thu được 15,8 gam hh Y gồm các oxit . Hòa tan hết Y bằng lượng vừa đủ dd gồm HCl 1M và H2SO4 0,5M thu được dd chứa 42,8 gam hỗn hợp muối trung hòa . Biết các pư xảy ra hoàn toàn . Tìm giá trị m ? Giúp em với ạ
Lấy 1,6(g) hỗn hợp A gồm Fe,Mg cho vào 200ml dd HCl, sau pư xảy ra hoàn toàn, cô cạn dd (trong đk có oxi) thì thu được 2,31g chất rắn. tính thể tích khí hydro bay ra (đktc)
Gọi $n_{H_2} = a(mol) \Rightarrow n_{HCl} = 2a(mol)$
Bảo toàn khối lượng :
$m_A + m_{HCl} = m_{muối} + m_{H_2}$
Suy ra : $1,6 + 2a.36,5 = 2,31 + 2a$
Suy ra : $a = 0,01$
$V_{H_2} = 0,01.22,4 = 0,224(lít)$
Đốt cháy 8,6 gam hỗn hợp gồm Fe, Zn, Al và Mg trong khi oxi dư, thu được 13,72 gam hỗn hợp X. Toàn bộ X phản ứng vừa đủ với V ml dd HCl 2M. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là:
A. 320
B. 480
C. 160.
D. 240
Đốt cháy 8,6 gam hỗn hợp gồm Fe, Zn, Al và Mg trong khi oxi dư, thu được 13,72 gam hỗn hợp X. Toàn bộ X phản ứng vừa đủ với V ml dd HCl 2M. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là:
A. 320.
B. 480.
C. 160.
D. 240.
a) PTHH: 2Al + 6 HCl -> 2 AlCl3 + 3 H2
x___________3x______________1,5x(mol)
Fe +2 HCl -> FeCl2 + H2
y___2y____y______y(mol)
b) Ta có: m(rắn)= mCu=0,4(g)
=> m(Al, Fe)=1,5-mCu=1,5-0,4=1,1(g)
nH2= 0,04(mol)
Ta lập hpt:
\(\left\{{}\begin{matrix}27x+56y=1,1\\1,5x+y=0,04\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,01\end{matrix}\right.\)
=> mAl=27.0,02=0,54(g)
mFe=56.0,01=0,56(g)