Cho Cu có 2 đồng vị 63Cu và ?Cu biết đồng vị ?Cu chiếm 25% nguyên tử khối trung bình của Cu là 63,5 (u)
Xác định số khối của đồng vị ?Cu
Tìm phần trăm khối lượng của 63Cu trong hợp chất Cu2O
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. biết nguyên tử khối trung bình của Cu là 63,54. Phần trăm khối lượng của 63Cu trong Cu2O là?
A. 73%.
B. 64,29%.
C. 35,71%.
D. 27%.
Đáp án B
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
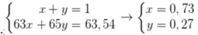
Phần trăm khối lượng của 63Cu trong Cu2O là
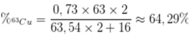
Trong tự nhiên Cu có hai loại đồng vị là 63Cu và 65Cu. Khối lượng nguyên tử trung bình của Cu là 63,54. Hỏi đồng vị 63Cu chiếm bao nhiêu % về khối lượng trong tinh thể CuSO4.5H2O?
A. 18,59 %
B. 27%
C. 73%
D. 18,43%
Gọi x là số phần trăm của đồng vị 63Cu
Suy ra phần trăm đồng vị 65Cu là 100 – x
M = [63.x + 65(100 – x)]/100 = 63,546
<=> x = 72,7%
Từ đây dễ dàng tìm được % của 63Cu trong tinh thể CuSO4.5H2O là 18,43%
=> Đáp án D
Nguyên tử khối trung bình của Cu là 63,54. Đồng có 2 đồng vị, biết đồng vị thứ nhất là 63cu chiếm 73%. a) Tìm đồng vị thứ 2 của đồng. b) Khi có 81 nguyên tử đồng vị thứ 2 thì có bao nhiêu nguyên tử 63cu? c) Tính % khối lượng đồng vị 63cu có trong phân tửCu2o (cho O = 16).
a), Đặt đồng vị thứ 2 của đồng là A2.
\(\overline{NTK}_{Cu}=63,54\\ \Leftrightarrow\dfrac{63.73\%+A_2.27\%}{100\%}=63,54\\ \Leftrightarrow A_2=65\left(đ.v.C\right)\)
b, Khi có 81 nguyên tử đồng vị thứ 2 thì số nguyên tử 63Cu là:
\(\dfrac{81.73}{27}=219\left(nguyên.tử\right)\)
c) Phần trăm khối lượng đồng vị 63Cu có trong phân tử Cu2O là:
\(73\%.\dfrac{63,54.2}{63,54.2+16}\approx64,837\%\)
Trong tự nhiên Cu có 2 đồng vị bền là 63Cu và 65Cu. Nguyên tử khối trung bình của Cu là 63,54 đvC. Thành phần phần trăm tổng số nguyên tử của 63Cu là
A. 73%.
B. 27%.
C. 54%.
D. 50%.
trong tự nhiên đồng có 2 đồng vị 63cu và 65cu .Nguyên tử khối trung bình của Cu là 63,54. a,Tính phần trăm số nguyên tử mỗi loại đồng vị b.Tính thành phần phần trăm theo khối lượng của 65Cu trong CuSO
a)
Gọi thành phần phần trăm của hai đồng vị 63Cu ,65Cu lần lượt là a,b
Ta có :
a + b = 100%
63a + 65b = 63,54
Suy ra a = 0,73 = 73% ; b = 0,27 = 27%
b) Thành phần phần trăm khối lượng của 65Cu trong CuSO4 là :
\(\dfrac{65.27\%}{63,54 + 32 + 16.4 }.100\% = 11\%\)
Gọi :
Phần trăm số nguyên tử của đồng vị 63Cu là a
Phần trăm số nguyên tử của đồng vị 65Cu là b
Ta có :
\(a + b = 100\%\\ 63.a\% + 65.b\% = 63,54\)
Suy ra : a = 73% ; b = 27%
\(\)Phần trăm khối lượng của 63Cu trong Cu(NO3)2 là :
\(\dfrac{63.73\%}{63,54+ 14.2 + 16.6}.100\% = 24,52\%\)
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của Cu là 63,54. Tính thành phần % khối lượng của 63Cu trong CuSO4?
A. 28,83%.
B. 10,97%
C. 11,00%.
D. 28,74%.
Đáp án A
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
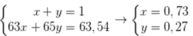
Phần trăm khối lượng của 63Cu trong CuSO4 là
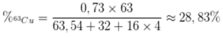
Trong tự nhiên Cu có hai đồng vị: 63Cu và 65Cu. Khối lƣợng nguyên tử trung bình của Cu là 63,54. Thành phần % về khối lƣợng của 63Cu trong CuCl2 là? Biết MCl = 35,5
\(\overline{NTK}_{Cu}=63,54\\ \Leftrightarrow\dfrac{63.x+65.\left(100\%-x\right)}{100\%}=63,54\\ \Leftrightarrow x=73\%\\ \Rightarrow\%m_{\dfrac{^{63}Cu}{CuCl_2}}=73\%.\dfrac{63,54}{63,54+35,5.2}.100\approx34,476\%\)
Trong tự nhiên Cu có 2 đồng vị là "Cu và Cu, trong đó Cu chiếm 73%
a. Xác định số khối A của đồng vị thứ 2. Biết nguyên tử khối trung bình của Cu là 63,54.
b. Tính % khối lượng của 6 Cu trong phân tử muối ngậm nước CUSO4.5H2O.