Đáp án B
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
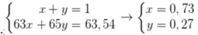
Phần trăm khối lượng của 63Cu trong Cu2O là
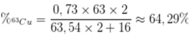
Đáp án B
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
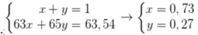
Phần trăm khối lượng của 63Cu trong Cu2O là
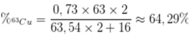
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của Cu là 63,54. Tính thành phần % khối lượng của 63Cu trong CuSO4?
A. 28,83%.
B. 10,97%
C. 11,00%.
D. 28,74%.
Bài 1: Trong tự nhiên , đồng có 2 đồng vị 65Cu và ACu, trong đó đồng vị 65Cu chiếm 27% về số nguyên tử. Nguyên tử khối trung bình của đồng là 63,54.
a.Tính A.
b.Tính phần trăm khối lượng của 63Cu trong kim loại đồng tự nhiên.
Bài 2: Nguyên tử nguyên tố A có phân mức năng lượng cao nhất là 3s1. Nguyên tử nguyên tố B có cấu hình electron phân lớp ngoài cùng là 3p4. Nguyên tử nguyên tố tố C có tổng số electron ở phân lớp p là 11. Viết cấu hình electron đầy đủ của A, B, C và xác định vị trí của chúng trong bảng tuần hoàn.
Bài 3: Cation X+ và anion Y2- có cấu hình electron ở phân lớp ngoài cùng là 3p6. Hãy xác định vị trí của X ,Y trong bảng tuần hoàn. Hãy cho biết tính chất cơ bản của X,Y: Tính kim loại hay phi kim? Công thức oxit cao nhất? Tính chất (axit hay bazơ) của oxit? Hợp chất khí hidro (nếu có)? Công thức hidroxit tạo nên từ nguyên tố X, Y. Tính chất (axit hay bazơ) của hidroxit? Bài 4: Oxit trong đó nguyên tố R có hóa trị cao nhất là R2O5. R chiếm 91,176% khối lượng trong hợp chất khí với hiđro. Xác định tên nguyên tố R?
Bài 5: X tạo hợp chất khí với hidro là H2X. Trong oxit cao nhất, X chiếm 40% về khối lượng. Xác định tên X.
Giải giúp mình với ạ.
Mình đang cần gấp ạ.
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của đồng là 63,54. Thành phần % khối lượng của 63Cu trong CuCl2 là (cho Cl = 35,5)
A. 12,64%.
B. 26,77%.
C. 27,00%.
D. 34,18%.
Nguyên tử khối trung bình của Cu là 63,54. Đồng có 2 đồng vị, biết đồng vị thứ nhất là 63cu chiếm 73%. a) Tìm đồng vị thứ 2 của đồng. b) Khi có 81 nguyên tử đồng vị thứ 2 thì có bao nhiêu nguyên tử 63cu? c) Tính % khối lượng đồng vị 63cu có trong phân tửCu2o (cho O = 16).
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu trong đó đồng vị 65Cu chiếm 27% về số nguyên tử. Phần trăm khối lượng của 65Cu trong CuSO4.5H2O là
A. 7,03.
B. 73.
C. 27.
D. 18,43.
Nguyên tử khối trung bình của Cu là 63,54. Cu có 2 đồng vị: 63 29Cu và 65 29Cu . Phần trăm khối lượng của 63 29Cu trong Cu2O là ? A. 64,29%. B. 65,33%. C. 32,14%. D. 65,34%.
Trong tự nhiên, đồng có 2 đồng vị 63Cu và 65Cu, trong đó đồng vị 65Cu chiếm khoảng 27% về số nguyên tử. Phần trăm khối lượng của 63Cu trong CuCl2
Trong tự nhiên, đồng có 2 đồng vị 63Cu và 65Cu, trong đó đồng vị 65Cu chiếm khoảng 27% về số nguyên tử. Phần trăm khối lượng của 63Cu trong CuCl2
Nguyên tử khối trung bình của đồng KL là 63,546. Đồng tồn tại trong tự nhiên với 2 đồng vị 63Cu và 65Cu. Thành phần phần trăm theo số nguyên tử của 65Cu là?
A. 23,7%
B. 76,3%
C. 72,7%
D. 27,3%