Để khử hoàn toàn 23,2 gam một oxit kim loại, cần dùng 8,96 lít H2 (đktc). Kim loại đó là
A. Mg. B. Cu.
C. Fe. D. Cr.
Để khử hoàn toàn 23,2 gam một oxit kim loại cần dùng 8,96 lít H2 (đktc). Khim loại đó là kim loại nào sau đây?
B. Cu.
C. Fe.
D. Cr.
Đáp án C.
Gọi công thức của oxit kim loại là MxOy
Số mol H2 là nH2 = 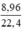 = 0,4(mol)
= 0,4(mol)
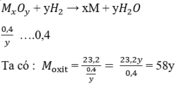
Như vậy :
Mx + 16y = 58y
Mx = 42y
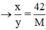
Giá trị thỏa mãn : M = 56; x = 3; y = 4
Kim loại là Fe và công thức oxit là Fe3O4
Để khử hoàn toàn 23,2 gam một oxit kim loại, cần dùng 8,96 lít H2 (đktc). Kim loại đó là
A. Mg
B. Cu
C. Fe
D. Cr
MxOy + yH2 → xM + yH2O (1)
=
= 0,4 (mol)
Theo (1), ta có số mol nguyên tử oxi trong oxit là 0,4 mol
Khối lượng kim loại M trong 23,2 gam oxit là: 23,2 - 0,4.16 = 16,8 (gam)
Chỉ có nguyên tử khối của M là 56 và số mol kim loại M là 0,3 mol mới phù hợp => Kim loại M là Fe.
Để khử hoàn toàn 23,2 gam một oxit kim loại, cần dùng 8,96 lít H2 (đktc). Kim loại đó là
A. Mg
B. Cu
C. Fe
D. Cr
Để khử hoàn toàn 23,2 gam một oxit kim loại, cần dùng 8,96 lít H2 (đktc). Kim loại đó là:
A. Mg. B. Cu.
C. Fe. D. Cr.
MxOy + yH2 → xM + yH2O (1)
=
= 0,4 (mol)
Theo (1), ta có số mol nguyên tử oxi trong oxit là 0,4 mol
Khối lượng kim loại M trong 23,2 gam oxit là: 23,2 - 0,4.16 = 16,8 (gam)
Chỉ có nguyên tử khối của M là 56 và số mol kim loại M là 0,3 mol mới phù hợp => Kim loại M là Fe.
. Để khử hoàn toàn 23,2 gam một oxit kim loại, cần dùng 8,96 lít H2 (đktc). Kim loại đó là:
A. Mg. B. Cu.
C. Fe. D. Cr.
MxOy + yH2 → xM + yH2O (1)
=
= 0,4 (mol)
Theo (1), ta có số mol nguyên tử oxi trong oxit là 0,4 mol
Khối lượng kim loại M trong 23,2 gam oxit là: 23,2 - 0,4.16 = 16,8 (gam)
Chỉ có nguyên tử khối của M là 56 và số mol kim loại M là 0,3 mol mới phù hợp => Kim loại M là Fe.
Để khử hoàn toàn 2,32 gam một oxit kim loại, cần dùng 0,896 lít khí H 2 ở đktc. Kim loại đó là
A. Mg.
B. Cu.
C. Fe.
D. Cr.
Để khử hoàn toàn 2,32 gam một oxit kim loại, cần dùng 0,896 lít khí H 2 ở đktc. Oxit kim loại là
A. MgO.
B. CuO.
C. F e 3 O 4 .
D. C r 2 O 3 .
Để khử hoàn toàn 8g một oxit kim loại cần 3,36 lít H2(đktc). Kim loại đó là?
Giả sử CTHH của oxit cần tìm là A2On
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PT: \(A_2O_n+nH_2\underrightarrow{t^o}2A+nH_2O\)
Theo PT: \(n_{A_2O_n}=\dfrac{1}{n}n_{H_2}=\dfrac{0,15}{n}\left(mol\right)\)
\(\Rightarrow M_{A_2O_n}=\dfrac{8}{\dfrac{0,15}{n}}=\dfrac{160}{3}n\left(g/mol\right)\)
\(\Rightarrow2M_A+16n=\dfrac{160}{3}n\Rightarrow M_A=\dfrac{56}{3}\left(g/mol\right)\)
Với n = 3, MA = 56 (g/mol) là thỏa mãn.
Vậy: KL đó là Fe.
Đốt cháy hoàn toàn 8,1 gam của một kim loại A hóa trị III cần dùng hết 5,04 lít khí Oxi ( đktc) ở nhiệt độ cao thu được một Oxit. Kim loại A là
A. Fe B. Al C. Cr D. Kết quả khác.
Đốt cháy hoàn toàn 8,1 gam của một kim loại A hóa trị III cần dùng hết 5,04 lít khí Oxi ( đktc) ở nhiệt độ cao thu được một Oxit. Kim loại A là
A. Fe B. Al C. Cr D. Kết quả khác.
Khử hoàn toàn 32 g một oxit kim loại M cần dùng tới 13,44 lít H2. Cho toàn bộ kim loại thu được tác dụng với dung dịch HCl dư thì thu được 8,96 lít H2. Xác định kim loại m và công thức hóa học của oxit. Giải dễ hiểu nhất dùm mình nhan!
\(n_{H_2thuđược}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{H_2cầndùng}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Ta có : Số mol Oxi/Oxit = n H2 dùng = 0,6 ( mol )
\(m_{\dfrac{O}{Oxit}}=0,6.16=9,6\left(g\right)\)
\(m_{\dfrac{M}{Oxit}}=32-9,6=22,4\left(g\right)\)
Gọi hóa trị M là n
PTHH :
\(2M+2nHCl\rightarrow2MCl_2+nH_2\uparrow\)
\(\dfrac{2}{n}.0,4\) 0,4
\(M_M=\dfrac{22,4}{\dfrac{2}{n}.0,4}=28.n\)
| n | 1 | 2 | 3 |
| M | 28 | 56 | 84 |
| Dk | (L) | T/M (Fe) | (L) |
Vậy kim loại M là Fe
\(\rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{\dfrac{22,4}{56}}{0,6}=\dfrac{2}{3}\)
Vậy CTPT của Oxit kim loại M là Fe2O3 .