Cho 5,12 gam kim loại R có hóa trị II không đổi tác dụng vừa đủ với 16g dung dịch H2SO4 98 % thấy thoát ra khí SO2 .
a . Viết PTHH của phản ứng đã xảy ra .
b . Tìm kim loại R .
Cho 20 gam kim loại R có hóa trị II tác dụng hoàn toàn với nước ở nhiệt độ thường , sau phản ứng thu được dung dịch base và thấy có 11,2 lít khí hydrogen thoát ra ngoài .
a. Viết PTHH của phản ứng
b. Xác định kim loại R. Biết thể tích các khí đo ở đktc
\(a.R+2H_2O\rightarrow R\left(OH\right)_2+H_2\\
b.n_{H_2}=\dfrac{11,2}{22,4}=0,5mol\\
n_R=n_{H_2}=0,5mol\\
M_R=\dfrac{20}{0,5}=40g/mol\)
Vậy kim loại R là Ca
Cho 3,6 gam kim loại R hoá trị II tác dụng vừa đủ với 150 gam dung dịch HCl thấy thoát ra 3,36 lít khíH2 (ở đktc).a) R là kim loại gì?b) Tính C% của dung dịch axit đã dùng.c) Tính C% của chất tan trong dung dịch sau phản ứng.
a) nH2=0,15(mol)
PTHH: R + 2 HCl -> RCl2 + H2
0,15______0,3____0,15___0,15(mol)
M(R)=mR/nR=3,6/0,15= 24(g/mol)
=> R(II) cần tìm là Magie (Mg=24)
b) PTHH: Mg + 2 HCl -> MgCl2 + H2
mHCl=0,3.36,5=10,95(g)
=>C%ddHCl= (10,95/150).100= 7,3%
c) mH2= 0,15.2=0,3(g)
mddMgCl2= mMg + mddHCl - mH2= 3,6+ 150 - 0,3= 153,3(g)
mMgCl2=0,15.95=14,25(g)
=> \(C\%ddMgCl2=\dfrac{14,25}{153,3}.100\approx9,295\%\)
Cho 4,6 gam kim loại R có hóa trị I tác dụng hoàn toàn với nước ở nhiệt độ thường , sau phản ứng thu được 8 gam base và thấy có khí hydrogen thoát ra ngoài .
a. Viết PTHH của phản ứng
b. Xác định kim loại R
cho 30,4 gam Mg và kim loại A hóa trị II đứng sau H trong dãy hoạt động hóa học tác dụng với một lượng dư dung dịch H2SO4 loãng thấy thoát ra 4,48 lít khí. Phần không tan cho tác dụng với H2SO4 đặc nóng dư phản ứng hoàn toàn thì sinh ra 8,96 lít khí sunfurơ
a/ xác định A
b/ Nếu cho 2 kim loại trên tác dụng với 200 gam dung dịch H2SO4 đặc, nóng thì thu được bao nhiêu lít khí có mùi trứng thối? Tính C% của dung dịch sau khi phản ứng
Mg + H2SO4 -- > MgSO4 + H2
1 1 1 1 (mol)
0,2 0,2 0,2 0,2 (mol)
nH2 = 4,48 / 22,4 = 0,2 (mol)
A + 2H2SO4 ( đặc nóng ) --> ASO4 + SO2 + 2H2O
1 2 1 1 2 (mol)
0,4 0,4 (mol)
nSO2 = 8,96 / 22,4 = 0,4 (mol)
Theo đề ta có :
24.0,2 + A.0,4 = 30,4
=> A = 64 => kim loại A là Cu
Mg + 2H2SO4 ( đặc nóng )---> MgSO4 + SO2 + 2H2O
1 2 1 1 2 (mol)
0,2 0,2 (mol)
Cu + 2H2SO4 ( đặc nóng ) ---> CuSO4 + SO2 + 2H2O
1 2 1 1 2 (mol)
0,4 0,4 (mol)
nSO2 = 0,2+0,4 = 0,6 (mol)
= > VSO2 = 0,6 . 22,4 = 13,44 (l)
mMgSO4 = 0,2 . 120 = 24 (g)
mCuSO4 = 0,4.160 = 64 (g)
mSO2 (cả pứ ) = 0,6.64 = 38,4 (g)
mdd = mhhkl + mddH2SO4 - mSO2
= 30,4 + 200 - 38,4 = 192 (g)
=> \(C\%_{ddMgSO_4}=\dfrac{24.100}{192}=12,5\%\)
\(C\%_{ddCuSO_4}=\dfrac{64.100}{192}=33,33\%\)
Cho 7,8 gam hỗn hợp kim loại là R hóa trị II và Al tác dụng với dung dịch H2SO4 ( loãng dư) . Khi phản ứng kết thúc được dung dịch 2 muối và 8,96 lít khí
a, Viết phương trình phản ứng xảy ra
b,Tính khối lượng muối thu được sau thí nghiêm và tính thể tích dung dịch H2SO4 2M tối thiểu đã dùng
c, Xác định R biết rằng trong hỗn hợp ban đầu tỉ lệ số mol R : Al là 1:2
a, PT: \(R+H_2SO_4\rightarrow RSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b, Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(n_{H_2SO_4}=n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{0,4}{2}=0,2\left(l\right)\)
Theo ĐLBT KL, có: mKL + mH2SO4 = m muối + mH2
⇒ m muối = 7,8 + 0,4.98 - 0,4.2 = 46,2 (g)
c, Gọi: nR = x (mol) → nAl = 2x (mol)
Theo PT: \(n_{H_2}=n_R+\dfrac{3}{2}n_{Al}=x+\dfrac{3}{2}.2x=0,4\left(mol\right)\Rightarrow x=0,1\left(mol\right)\)
⇒ nR = 0,1 (mol)
nAl = 0,1.2 = 0,2 (mol)
⇒ 0,1.MR + 0,2.27 = 7,8 ⇒ MR = 24 (g/mol)
Vậy: R là Mg.
I Bài 6: Cho 8,4 gam kim loại R hóa trị II tác dụng vừa đủ với dung dịch acid HCI 15% thu được 3,36 lít khí hidro ( ở đktc). a. Xác định kim loại R. b. Tính khối lượng dung dịch acid cần dùng cho phản ứng.
a, \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: R + 2HCl → RCl2 + H2
Mol: 0,15 0,3 0,15
\(M_R=\dfrac{8,4}{0,15}=56\left(g/mol\right)\)
⇒ R là sắt (Fe)
b, \(m_{ddHCl}=\dfrac{0,3.36,5.100}{15}=73\left(g\right)\)
Cho 3,64 gam hỗn hợp E gồm một oxit, một hiđroxit và một muối cacbonat trung hòa của một kim loại M có hóa trị II tác dụng vừa đủ với 117,6 gam dung dịch H2SO4 10%. Sau phản ứng, thu được 0,448 lít khí (đktc) và dung dịch muối duy nhất có nồng độ 10,867% (khối lượng riêng là 1,093 gam/ml); nồng độ mol là 0,545M.
a) Viết các phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính % khối lượng của các chất có trong hỗn hợp E.
a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
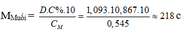
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
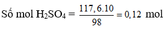
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%
cho 5,4g kim loại R có hóa trị n không đổi tác dụng vừa đủ vs V ml dung dịch H2SO4 loãng 24,5% ( KLR d= 1,08g/ml), sau phản ứng thu được dung dịch A và 6,72l khí H2 ở đktc. Xác định kim loại R, tính V và % khối lượng chất tan trong dung dịch A
Hòa tan hoàn toàn m gam Mg vào 100ml HCl 2M. phản ứng xảy ra hoàn toàn thu được chất khí không màu
a. Viết PTHH của PƯ
b. tính m gam và thể tích khí thoát ra ở đktc?
c. người ta cho một kim loại M (không rõ hóa trị) tác dụng vừa đủ với lượng axit HCl trên, sau PƯ thấy tạo thành 12,7 gam muối của kim loại M. Xác định kim loại M.
\(n_{HCl}=0.1\cdot2=0.2\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.1.......0.2.........................0.1\)
\(m_{Mg}=0.1\cdot24=2.4\left(g\right)\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(.........0.2.......\dfrac{0.2}{n}\)
\(M_{MCl_n}=\dfrac{12.7}{\dfrac{0.2}{n}}=63.5n\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow M+35.5n=63.5n\)
\(\Rightarrow M=28n\)
\(BL:n=2\Rightarrow M=56\)
\(M:Fe\)
a) Mg + 2HCl → MgCl2 + H2
b) n HCl = 0,1.2 = 0,2(mol)
n Mg = n H2 = 1/2 n HCl = 0,1(mol)
Suy ra:
m = 0,1.24 = 2,4(gam)
V H2 = 0,1.22,4 = 2,24(lít)
c) Gọi n là hóa trị M
2M +2nHCl $\to$ 2MCln + nH2
Theo PTHH :
n MCln = 1/n x n HCl = 0,2/n(mol)
Suy ra :
$\dfrac{0,2}{n}(M + 35,5n) = 12,7$
=> M = 28n
Với n = 2 thì M = 56(Fe)