Đốt cháy hoàn toàn 1,5lit (ở đktc) khí CH4 cần dùng hết bao nhiêu lít khí oxi (ở đktc)

Những câu hỏi liên quan
Đốt cháy hoàn toàn 4,48 lít khí metan CH4 (ở đktc) trong bình chứa khí oxi. Thể tích khí oxi (ở đktc) cần dùng là bao nhiêu
Ta có: \(n_{CH_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
____0,2___0,4 (mol)
\(\Rightarrow V_{O_2}=0,4.22,4=8,96\left(l\right)\)
Bạn tham khảo nhé!
Đúng 8
Bình luận (0)
nCH4 = 4,48/22,4 = 0,2 (mol)
PTHH: CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,2 ---> 0,4
VO2 = 0,4 . 22,4 = 8,96 (l)
Đúng 6
Bình luận (0)
Bài 1: Đốt cháy hoàn toàn 1,3 gam C2H2 cần dùng bao nhiêu lít khí oxi ở đktc ? bao nhiêu lít (đktc) không khí chứa 20% thể tích khí oxi
\(2C_2H_2+5O_2-^{t^o}\rightarrow4CO_2+2H_2O\\ n_{C_2H_2}=\dfrac{1,3}{26}=0,05\left(mol\right)\\ n_{O_2}=\dfrac{5}{2}n_{C_2H_2}=0,125\left(mol\right)\\ \Rightarrow V_{O_2}=2,8\left(l\right)\\ Vìtrongkhôngkhíchứa20\%O_2\\ \Rightarrow V_{kk}=\dfrac{2,8}{20\%}=14\left(l\right)\)
Đúng 3
Bình luận (0)
đốt cháy hoàn toàn 3 36 lít khí metan CH4 cần dùng bao nhiêu lít không khí(đktc). biết thể tích không khí gấp 5 lần thể tích khí oxi
PTHH: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Theo PTHH: \(V_{O_2}=2V_{CH_4}=6,72\left(l\right)\)
\(\Rightarrow V_{kk}=6,72\cdot5=33,6\left(l\right)\)
Đúng 1
Bình luận (0)
Phân hủy hoàn toàn 31,6g KMnO4 ( ở nhiệt độ cao )
1. Tính thể tích khí oxi tạo thành ( ở đktc )
2. Lượng oxi trên đủ đốt cháy hết bao nhiêu lít CH4 ( ở đktc )
3. Biết cứ 1 mol CH4 cháy hoàn toàn thì sinh ra 880KJ , hãy tính nhiệt lượng Q tạo ra hóa ra khí trên cháy hết
Biết K=39 , Mn=55, O=12, H=1, Mg=24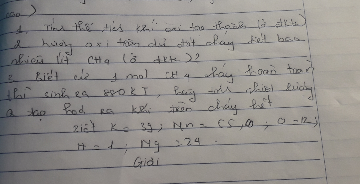
\(1) n_{KMnO_4}= \dfrac{31,6}{158} = 0,2(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{O_2} = \dfrac{1}{2}n_{KMnO_4} = 0,1(mol)\\ V_{O_2} = 0,1.22,4 = 2,24(lít)\\ 2) CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ V_{CH_4} = \dfrac{1}{2}V_{O_2} = 1,12(lít)\\ 3)n_{CH_4} = \dfrac{1,12}{22,4} = 0,05(mol)\\ \text{Nhiệt lượng tỏa ra = } = 0,05.880 = 44(KJ)\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 11,2 lít khí metan cần phải dùng: a/ Bao nhiêu lít khí oxi? b/ Bao nhiêu lít không khí chứa 20% thể tích oxi? (Thể tích các khí đo ở đktc)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Ta có: \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
a, Theo PT: \(n_{O_2}=2n_{CH_4}=1\left(mol\right)\)
\(\Rightarrow V_{O_2}=1.22,4=22,4\left(l\right)\)
b, \(V_{kk}=\dfrac{22,4}{20\%}=112\left(l\right)\)
Đúng 2
Bình luận (0)
BT2: Đốt cháy hoàn toàn 5,6 lít hh 2 khí CO và CH4 cần dùng 4,48 lít khí oxi. Tính % theo thể tích mỗi khí trong hh. Các thể tích khí đo ở đktc.
Gọi số mol CO, CH4 là a, b (mol)
=> \(a+b=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2CO + O2 --to--> 2CO2
a--->0,5a
CH4 + 2O2 --to--> CO2 + 2H2O
b--->2b
=> 0,5a + 2b = 0,2
=> a = 0,2 (mol); b = 0,05 (mol)
=> \(\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,2}{0,25}.100\%=80\%\\\%V_{CH_4}=\dfrac{0,05}{0,25}.100\%=20\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
\(n_{hh}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ 2CO+O_2\rightarrow\left(t^o\right)2CO_2\\ CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ Đặt:n_{CO}=a\left(mol\right);n_{CH_4}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}a+b=0,25\\0,5a+2b=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,05\end{matrix}\right.\\ \Rightarrow\%V_{\dfrac{CO}{hh}}=\%n_{\dfrac{CO}{hh}}=\dfrac{a}{a+b}.100\%=\dfrac{0,2}{0,25}.100=80\%;\%V_{CH_4}=100\%-80\%=20\%\)
Đúng 1
Bình luận (0)
Để đốt cháy 5,6 lít khí etilen cần phải dùng:
a) Bao nhiêu lít oxi?
b) Bao nhiêu lít không khí chứa 1/5 thể tích oxi? Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Hỗn hợp A gồm CH4 và C2H4. Đốt cháy hoàn toàn 3,36 lít hỗn hợp A (đktc) thì thu được 8,8g khí cacbonic. Hãy tính thành phần % thể tích của mỗi khí trong hỗn hợp.
Câu 1:
\(a,PTHH:C_2H_4+5O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(n_{C_2H_4}=\dfrac{V_{\left(đktc\right)}}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(Theo.PTHH:n_{O_2}=5.n_{C_2H_4}=5.0,25=1,25\left(mol\right)\\ V_{O_2\left(đktc\right)}=n.22,4=1,25.22,4=28\left(l\right)\)
\(b,\Rightarrow V_{kk\left(đktc\right)}=5.V_{O_2\left(đktc\right)}=5.28=140\left(l\right)\)
Đúng 0
Bình luận (1)
B1:
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
Vì số mol tỉ lệ thuận với thể tích, đồng thời nhìn PTHH, ta sẽ được:
\(a,V_{O_2\left(đktc\right)}=3.V_{C_2H_4\left(đktc\right)}=3.5,6=16,8\left(l\right)\)
\(b,V_{kk}=5.V_{O_2\left(đktc\right)}=16,8.5=84\left(l\right)\)
B2:
Đặt số mol metan, etylen lần lượt là a,b (mol) (a,b>0)
\(n_{hh}=n_{CH_4}+n_{C_2H_4}=a+b=\dfrac{3,36}{22,4}=0,15\left(1\right)\)
PTHH: CH4 +2 O2 -to-> CO2 +2 H2O
C2H4 +3 O2 -to-> 2CO2 + 2H2O
\(n_{CO_2\left(tổng\right)}=a+2b=\dfrac{8,8}{44}=0,2\left(mol\right)\left(2\right)\)
(1), (2) =>a=0,1; b=0,05
Số mol tỉ lệ tương ứng với thể tích. Nên:
\(\%V_{CH_4}=\%n_{CH_4}=\dfrac{0,1}{0,15}.100\approx66,667\%\\ \Rightarrow\%V_{C_2H_4}\approx33,333\%\)
Đúng 4
Bình luận (2)
13/Để đốt cháy hoàn toàn 11,2 lít khí CH4 cần phải dùng: a)bbao nhiêu lít khí O2 b) bao nhiêu lít không khí, biết O2 chiếm 1/5 thể tích không khí (viết thể tích các khí đó ở đktc)
a) \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,5--->1
=> VO2 = 1.22,4 = 22,4 (l)
b) Vkk = 22,4.5 = 112 (l)
Đúng 1
Bình luận (0)
a, Tính thể tích của oxi (đktc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
b, Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt chày hoàn toàn 9,6g lưu huỳnh trong lọ chưa khí Oxi
a) Tính khối lượng KClO₃ cần dùng để điểu chế khí Oxi cần dùng cho thí nghiệm trên
b) Nếu đốt cháy lượng lưu huỳnh trong bình chứa không khí thì phải cần bao nhiêu lít không khí ở đktc
\(a,PTHH:S+O_2\underrightarrow{t^o}SO_2\left(1\right)\)
\(n_S=\dfrac{m}{M}=\dfrac{9,6}{32}=0,3\left(mol\right)\)
\(Theo.PTHH\left(1\right):n_O=n_S=0,3\left(mol\right)\)
\(PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\\ Theo.PTHH\left(2\right):n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ m_{KClO_3}=n.M=0,2.122,5=24,5\left(g\right)\)
\(b,V_{O_2\left(đktc\right)}=n.22,4=0,2.22,4=4,48\left(l\right)\\ \Rightarrow V_{kk\left(đktc\right)}=5.V_{O_2}=5.4,48=22,4\left(l\right)\)
Đúng 1
Bình luận (0)






















