Cho 15 gam hợp kim nhôm - magie vào dung dịch HCI thu được 15,68 lít khí H2 ( đktc ) và 2,5 g một chất ko tan . Xác định thành phần % của hợp kim biết Cu không tác dụng với axit HCI

Những câu hỏi liên quan
Cho 12,7 gam hợp kim gồm Al, Cu và Mg vào dung dịch HCl dư. Sau phản ứng thu được 11,2 lít khí H 2 (ở đktc) và 2,5 gam chất không tan. Xác định thành phần phần trăm khối lượng của hợp kim.
Cu không tác dụng với axit HCl , do đó chất không tan là Cu và m Cu = 2,5 (gam).
Khối lượng Al và Mg bằng : 12,7 - 2,5 = 10,2 (gam)
Phương trình hoá học của phản ứng :
2Al + 6HCl → 2 AlCl 3 + 3 H 2
Mg + 2HCl → MgCl 2 + H 2
Theo phương trình hoá học trên và dữ kiện đề bài cho, ta có :
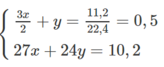
Giải ra, ta có : x = y = 0,2 mol
m Al = 0,2 x 27 = 5,4g
m Mg = 0,2 x 24 = 4,8g
% m Al = 5,4/12,7 .100% = 42,52%
% m Mg = 4,8/12,7 .100% = 37,8%
% m Cu = 100% - 42,52% - 37,8% = 19,68%
Đúng 0
Bình luận (0)
cho 12,7 gam hợp kim gồm Al, Cu, Mg vào dung dịch HCl dư. Sau phản ứng thu được 11,2 lít khí H2 (đktc) và 2,5 gam chất không tan. Xác định thành phần phần trăm khối lượng của hợp kim
PTHH: 2Al + 6HCl → 2AlCl3 + 3H2 ↑
Mg + 2HCl → MgCl2 + H2 ↑
Cu + HCl → Không phản ứng
%Cu trong hỗn hợp kim loại là: (2,5:12,7).100% = 19,7%
Khối lượng hỗn hợp Al và Mg là: 12,7 - 2,5 = 10,2 gam
Gọi số mol của Al là 2a , số mol của Mg là b
Số mol của H2 là: 11,2 : 22,4 = 0,5 mol
Ta có hệ pt:
27 . 2a + 24b = 10,23a + b = 0,5=> a = 0,1 mol ; b = 0,2 mol
Khối lượng Al là: 27 . 2a = 27 . 2 . 0,1 = 5,4 gam
% Al trong hỗn hợp KL là: (5,4:12,7).100% = 42,52%
%Mg trong hỗn hợp là: 100% - 42,52% - 19,7% = 37,78%
Đúng 1
Bình luận (0)
Hòa tan 6 gam hỗn hợp Al, Cu và Fe vào dung dịch HCl thu được 3,024 lít khí H2 ở đktc và còn lại 1,86 gam chất không tan. Xác định thành phần % theo khối lượng của các kim loại trong hỗn hợp ( Biết Cu không tan trong axit )
GIÚP MÌNH VỚI, MÌNH CẦN GẤP !!!!!
Ta có: mCu = 1,86 (g)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Có: mAl + mFe = 6 - 1,86 = 4,14 (g)
Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 56y = 4,14 (1)
Ta có: \(n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{3}{2}x+y\left(mol\right)\)
\(\Rightarrow\dfrac{3}{2}x+y=0,135\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,06\left(mol\right)\\y=0,045\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{1,86}{6}.100\%=31\%\\\%m_{Al}=\dfrac{0,06.27}{6}.100\%=27\%\\\%m_{Fe}=42\text{%}\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Chất rắn không tan sau phản ứng là Cu
=> m Cu = 1,86(gam)
Gọi n Al =a (mol) ; n Fe = b(mol) => 27a + 56b = 6 -1,86 = 4,14(1)
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
n H2 = 1,5a + b = 3,024/22,4 = 0,135(2)
Từ (1)(2) suy ra a = 0,06 ; b = 0,045
Vậy :
%m Cu = 1,86/6 .100% = 31%
%m Al = 0,06.27/6 .100% = 27%
%m Fe = 100% -31% -27% = 42%
Đúng 1
Bình luận (0)
Cho 15 gam hợp kim nhôm - magie vào dung dịch HCl có 15,68 lít hiđro bay ra (ở đktc). Xác định thành phần phần trăm khối lượng của nhôm, magie trong hợp kim.
Phương trình hoá học của phản ứng :
2Al + 6HCl → 2 AlCl 3 + 3 H 2
Mg + 2HCl → MgCl 2 + H 2
Gọi n Al = a mol
n Mg = b mol
Theo phương trình hoá học trên và dữ liệu đề bài, ta có :
27a + 24b = 15
3a/2 + b = 0,7
Giải ra, ta có a = 0,2 (mol); b = 0,4 (mol)
% m Al = 0,2x27/15 x 100% = 36%
% m Mg = 0,4 x 24/15 x 100% = 64%
Đúng 0
Bình luận (0)
Hòa tan 9 gam hợp kim nhôm- magie vào dung dịch H2SO4 dư thu được 10,08 lít khí H2 (đktc). Tính thành phần % khối lượng của nhôm và magie trong hợp kim.
Ta có: 27nAl + 24nMg = 9 (1)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Mg}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Mg}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{9}.100\%=60\%\\\%m_{Mg}=40\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
\(Đặt:n_{Al}=a\left(mol\right);n_{Mg}=b\left(mol\right)\left(a,b>0\right)\\ n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\\ PTHH:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ \Rightarrow\left\{{}\begin{matrix}27a+24b=9\\1,5a+b=0,45\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,15\end{matrix}\right.\\ \Rightarrow\%m_{Al}=\dfrac{0,2.27}{9}.100\%=60\%;\%m_{Mg}=\dfrac{24.0,15}{9}.100\%=40\%\)
Đúng 1
Bình luận (0)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45mol\\ n_{Al}=a,n_{Mg}=b\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ \Rightarrow\left\{{}\begin{matrix}24a+27b=9\\1,5a+b=0,45\end{matrix}\right.\\ \Rightarrow a=0,2;b=0,15\\ \%m_{Al}=\dfrac{0,2.27}{9}\cdot100=60\%\\ \%m_{Mg}=100-60=40\%\)
Đúng 1
Bình luận (0)
Cho 12,7 gam hợp kim gồm Al, Cu và Mg vào dung dịch HCl dư. Sau phản ứng thu được 11,2 lít khí H2 (ở đktc) và 2,5 gam chất rắn
không tan và 200 ml dung dịch X.
a) Xác định thành phần phần trăm khối lượng của hợp kim.
b) Tính nồng độ mol/l của các chất tan trong dd X.
Cho một lượng hỗn hợp gồm Zn và Cu tác dụng với lượng dư dung dịch axit HCL , thu được 4,48 lít khí H2 (đktc) . Sau phản ứng thấy còn 19,5 gam một chất rắn không tan. Tính thành phần % về khối lượng mỗi kim loại trong hỗn hợp.
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl -->ZnCl2 + H2
____0,2<----------------------0,2
=> mZn = 0,2.65 = 13 (g)
mCu = mrắn không tan = 19,5 (g)
\(\left\{{}\begin{matrix}\%Zn=\dfrac{13}{13+19,5}.100\%=40\%\\\%Cu=\dfrac{19,5}{13+19,5}.100\%=60\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
`n_(H_2)=4,48/22,4=0,2 (mol)`
Ta có PTHH: `Zn+2HCl --> ZnCl_2 +H_2`
Theo PT: `1`--------------------------------`1`
Theo đề: `0,2`------------------------------`0,2`
`m_(Zn)=0,2.65=13(g)`
Vì `Cu` không phản ứng với `HCl` nên `m_(chất rắn không tan)=m_(Cu)=19,5(gam)`
`%Zn=13/(13+19,5) .100%=40%`
`%Cu=100%-40%=60%`
Đúng 0
Bình luận (0)
Câu 6. Cho 12,7 gam hợp kim gồm Al, Cu và Mg vào dung dịch HCl dư. Sau phản ứng thu được 11,2 lít khí H2 (ở đktc) và 2,5 gam chất rắnkhông tan và 200 ml dung dịch X.a) Xác định thành phần phần trăm khối lượng của hợp kim.b) Tính nồng độ mol/l của các chất tan trong dd X.c) Cô cạn dung dịch X thu được m gam rắn khan. Tính m. (d) Nếu hoà tan hoàn toàn 12,7g hợp kim trên trong dung dịch H2SO4 đặc, nóng thì sau phản ứng thu được bao nhiêu lít khí SO2 (đktc)?e) Cho 25,4g hợp kim trên vào cố đựng dung...
Đọc tiếp
Câu 6. Cho 12,7 gam hợp kim gồm Al, Cu và Mg vào dung dịch HCl dư. Sau phản ứng thu được 11,2 lít khí H2 (ở đktc) và 2,5 gam chất rắn
không tan và 200 ml dung dịch X.
a) Xác định thành phần phần trăm khối lượng của hợp kim.
b) Tính nồng độ mol/l của các chất tan trong dd X.
c) Cô cạn dung dịch X thu được m gam rắn khan. Tính m. (
d) Nếu hoà tan hoàn toàn 12,7g hợp kim trên trong dung dịch H2SO4 đặc, nóng thì sau phản ứng thu được bao nhiêu lít khí SO2 (đktc)?
e) Cho 25,4g hợp kim trên vào cố đựng dung dịch NaOH loãng, dư thì sau phản ứng thu được bao nhiêu lít khí (đktc)?
Câu 6. Cho 12,7 gam hợp kim gồm Al, Cu và Mg vào dung dịch HCl dư. Sau phản ứng thu được 11,2 lít khí H2 (ở đktc) và 2,5 gam chất rắnkhông tan và 200 ml dung dịch X.a) Xác định thành phần phần trăm khối lượng của hợp kim.b) Tính nồng độ mol/l của các chất tan trong dd X.c) Cô cạn dung dịch X thu được m gam rắn khan. Tính m. (d) Nếu hoà tan hoàn toàn 12,7g hợp kim trên trong dung dịch H2SO4 đặc, nóng thì sau phản ứng thu được bao nhiêu lít khí SO2 (đktc)?e) Cho 25,4g hợp kim trên vào cố đựng dung...
Đọc tiếp
Câu 6. Cho 12,7 gam hợp kim gồm Al, Cu và Mg vào dung dịch HCl dư. Sau phản ứng thu được 11,2 lít khí H2 (ở đktc) và 2,5 gam chất rắn
không tan và 200 ml dung dịch X.
a) Xác định thành phần phần trăm khối lượng của hợp kim.
b) Tính nồng độ mol/l của các chất tan trong dd X.
c) Cô cạn dung dịch X thu được m gam rắn khan. Tính m. (
d) Nếu hoà tan hoàn toàn 12,7g hợp kim trên trong dung dịch H2SO4 đặc, nóng thì sau phản ứng thu được bao nhiêu lít khí SO2 (đktc)?
e) Cho 25,4g hợp kim trên vào cố đựng dung dịch NaOH loãng, dư thì sau phản ứng thu được bao nhiêu lít khí (đktc)?



















